- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме Железо
Содержание
- 1. Презентация по теме Железо
- 2. Соединения железа.Цель: изучение соединений железа.Задачи: исследовать свойства
- 3. Соединения железа.
- 4. Не в количестве знаний
- 5. Эксперимент – основа познания.Лабораторный опыт №1. Получение
- 6. Вывод по лабораторному опыту:Fe(OH)2 – основные свойства,
- 7. «Нет искусства столь же трудного, как искусство
- 8. Лабораторный опыт:
- 9. Роль cоединений железа в жизни живых организмов
- 10. Для нормального роста и
- 11. Значение железа для организма
- 12. Слайд 12
- 13. Слайд 13
- 14. В организм человека ионы
- 15. Слайд 15
- 16. Слайд 16
- 17. Следите за сбалансированностью своего питания, будьте здоровы!
- 18. Исследовательская работа. Определение содержания железа в продуктах питания.
- 19. Цель: Обнаружение ионов железа в продуктах питания.
- 20. Оборудование:
- 21. Исследуемые продукты питания:1) Гречка2) Пшено3) Мука пшеничная4) Ржаной хлеб
- 22. Ход работы: 1. Взяла
- 23. Ход работы: 3. Измельчила золу до
- 24. Ход работы:6. собрала прибор для фильтрования.7. профильтровала содержимое пробирок.8. 5 мл каждого фильтрата перелила в пробирку.
- 25. Ход работы:9. К фильтратам добавила раствор роданида калия - KSCN.10. Закрыла пробкой и интенсивно перемешала встряхиванием.
- 26. Результаты исследования: Сравнила интенсивность цвета анализируемых растворов.
- 27. ВЫВОДЫ:1. Все исследуемые продукты питания содержат железо.2. Самое большое содержание железа в ржаном хлебе.
- 28. Итог урока.Изучили соединения железа: оксиды и гидроксиды
- 29. То, что не
- 30. Домашнее задание: 1. параграф №14, упр. 5.
- 31. Не в
- 32. Спасибо за урок.
Соединения железа.Цель: изучение соединений железа.Задачи: исследовать свойства гидроксидов железа (II) и (III) ; научиться распознавать ионы Fe2+ и Fe3+.
Слайд 2Соединения железа.
Цель: изучение соединений железа.
Задачи:
исследовать свойства
гидроксидов железа (II)
и (III) ;
научиться распознавать ионы
Fe2+ и Fe3+.
научиться распознавать ионы
Fe2+ и Fe3+.
Слайд 3Соединения железа.
План
урока.
1. Гидроксиды железа (II) и (III): получение и свойства. (Л/О).
2. Качественные реакции на ионы Fe2+ и Fe3+. (Л/О).
3. Значение соединений железа в природе и в жизни человека (сообщение).
4. Исследование продуктов питания на содержание в них железа. ( исследовательская работа).
5. Проверочный тест.
1. Гидроксиды железа (II) и (III): получение и свойства. (Л/О).
2. Качественные реакции на ионы Fe2+ и Fe3+. (Л/О).
3. Значение соединений железа в природе и в жизни человека (сообщение).
4. Исследование продуктов питания на содержание в них железа. ( исследовательская работа).
5. Проверочный тест.
Слайд 4 Не в количестве знаний заключается образование, а в
полном понимании и искусном применении всего того, что знаешь.
Дистервег.
Дистервег.
Слайд 5Эксперимент – основа познания.
Лабораторный опыт №1. Получение и изучение свойств гидроксидов
железа (II) и (III).
Внимание! Соблюдайте правила по технике безопасности:
Во время проведения эксперимента не отвлекайтесь;
Все опыты проводите над лотком;
Берите необходимое количество веществ;
Не нюхайте и не пробуйте вещества на вкус;
С едкими веществами (кислотами и щелочами) работайте предельно осторожно;
Пузырьки с растворами веществ после использования обязательно закрывайте пробками;
По окончании работы приведите свое рабочее место в порядок.
Внимание! Соблюдайте правила по технике безопасности:
Во время проведения эксперимента не отвлекайтесь;
Все опыты проводите над лотком;
Берите необходимое количество веществ;
Не нюхайте и не пробуйте вещества на вкус;
С едкими веществами (кислотами и щелочами) работайте предельно осторожно;
Пузырьки с растворами веществ после использования обязательно закрывайте пробками;
По окончании работы приведите свое рабочее место в порядок.
Слайд 6Вывод по лабораторному опыту:
Fe(OH)2 – основные свойства, взаимодействует с кислотами.
Fe(OH)3 -
слабовыраженные амфотерные свойства ( с преобладанием основных), т.е. легко реагирует с кислотами, но трудно со щелочами.
Нерастворимое основание можно получить взаимодействием растворимой соли этого металла со щелочью.
Нерастворимое основание можно получить взаимодействием растворимой соли этого металла со щелочью.
Слайд 7«Нет искусства столь же трудного, как искусство наблюдения».
Лабораторный опыт №2. Качественные
реакции на ионы Fe2+ и Fe3+.
Внимание! Соблюдайте правила по технике безопасности:
Во время проведения эксперимента не отвлекайтесь;
Все опыты проводите над лотком;
Берите необходимое количество веществ;
Не нюхайте и не пробуйте вещества на вкус;
С едкими веществами (кислотами, солями и щелочами) работайте предельно осторожно;
Пузырьки с растворами веществ после использования обязательно закрывайте пробками;
По окончании работы приведите свое рабочее место в порядок.
Внимание! Соблюдайте правила по технике безопасности:
Во время проведения эксперимента не отвлекайтесь;
Все опыты проводите над лотком;
Берите необходимое количество веществ;
Не нюхайте и не пробуйте вещества на вкус;
С едкими веществами (кислотами, солями и щелочами) работайте предельно осторожно;
Пузырьки с растворами веществ после использования обязательно закрывайте пробками;
По окончании работы приведите свое рабочее место в порядок.
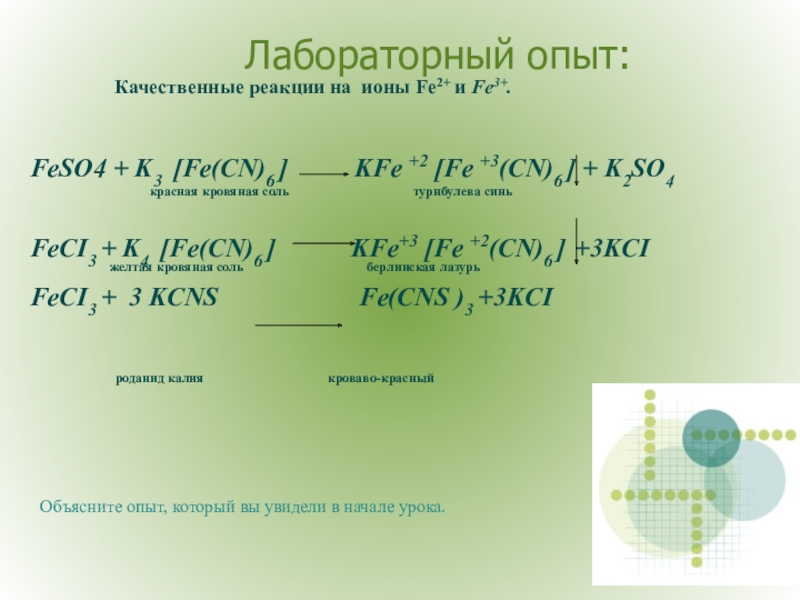
Слайд 8Лабораторный опыт:
Качественные
реакции на ионы Fe2+ и Fe3+.
FeSO4 + K3 [Fe(CN)6 ] KFe +2 [Fe +3(CN)6 ] + K2SO4
красная кровяная соль турнбулева синь
FeCI3 + K4 [Fe(CN)6 ] KFe+3 [Fe +2(CN)6 ] +3KCI
желтая кровяная соль берлинская лазурь
FeCI3 + 3 KCNS Fe(CNS )3 +3KCI
роданид калия кроваво-красный
Объясните опыт, который вы увидели в начале урока.
FeSO4 + K3 [Fe(CN)6 ] KFe +2 [Fe +3(CN)6 ] + K2SO4
красная кровяная соль турнбулева синь
FeCI3 + K4 [Fe(CN)6 ] KFe+3 [Fe +2(CN)6 ] +3KCI
желтая кровяная соль берлинская лазурь
FeCI3 + 3 KCNS Fe(CNS )3 +3KCI
роданид калия кроваво-красный
Объясните опыт, который вы увидели в начале урока.
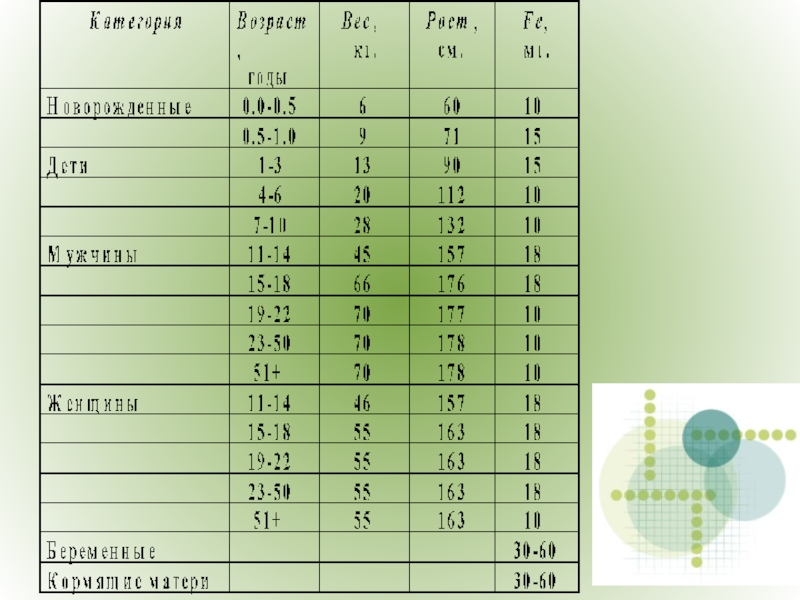
Слайд 10 Для нормального роста и выполнения биологических функций человеку
и животным кроме витаминов необходим целый ряд неорганических элементов :
макроэлементы(Ca, Mg, Na, K, P, Cl) микроэлементы(Zn, Fe и тд)
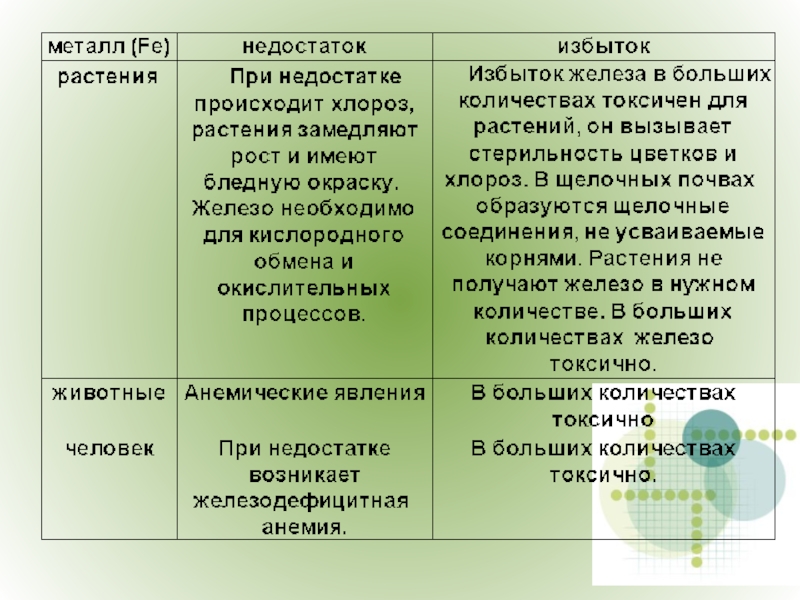
Слайд 11 Значение железа для организма человека и в целом
для живой природы трудно переоценить.
Его биологическая ценность определяется многогранностью его функций, активным участием в клеточном дыхании, обеспечивающим нормальное функционирование клеток и тканей.
Его биологическая ценность определяется многогранностью его функций, активным участием в клеточном дыхании, обеспечивающим нормальное функционирование клеток и тканей.
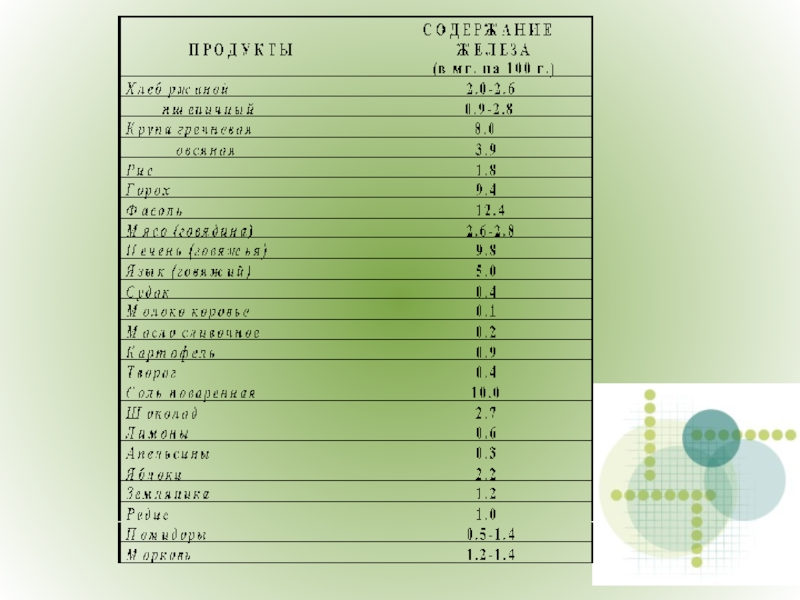
Слайд 14 В организм человека ионы железа попадают с продуктами питания,
поэтому оно должно быть сбалансированным.
Слайд 20Оборудование: Реактивы:
Штатив
Пробирки
Весы
Горелка
Ступка и
пестик
Колба
Воронка
Колба
Воронка
Соляная кислота
Роданид калия
Дистилированная вода
Слайд 22
Ход работы:
1. Взяла по 2.5г каждого образца продукта питания.
2.
Положила их в отдельные тигли и прокалила до золы.
Слайд 23
Ход работы:
3. Измельчила золу до порошка.
4. Перенесла золу в пробирку и
добавила 10мл HCI.
5 . Перемешав, добавила 5мл дистилированной воды.
5 . Перемешав, добавила 5мл дистилированной воды.
Слайд 24Ход работы:
6. собрала прибор для фильтрования.
7. профильтровала содержимое пробирок.
8. 5 мл
каждого фильтрата перелила в пробирку.
Слайд 25Ход работы:
9. К фильтратам
добавила раствор
роданида калия - KSCN.
10. Закрыла
пробкой
и интенсивно
перемешала
встряхиванием.
и интенсивно
перемешала
встряхиванием.
Слайд 27ВЫВОДЫ:
1. Все исследуемые продукты питания содержат железо.
2. Самое большое содержание железа
в ржаном хлебе.
Слайд 28Итог урока.
Изучили соединения железа: оксиды и гидроксиды (II) и (III).
Соединения железа
(II) проявляют основные свойства.
Соединения железа (III) проявляют
слабовыраженные амфотерные свойства , с преобладанием основных.
Реактивом на ион Fe2+ является красная кровяная соль при этом выпадает синий осадок – турнбулева синь.
Реактивами на ион Fe3+ являются желтая кровяная соль при этом выпадает синий осадок – берлинская лазурь и роданид калия – при этом образуется кроваво-красный раствор.
Соединения железа (III) проявляют
слабовыраженные амфотерные свойства , с преобладанием основных.
Реактивом на ион Fe2+ является красная кровяная соль при этом выпадает синий осадок – турнбулева синь.
Реактивами на ион Fe3+ являются желтая кровяная соль при этом выпадает синий осадок – берлинская лазурь и роданид калия – при этом образуется кроваво-красный раствор.
Слайд 29 То, что не ясно, следует выяснить. То,
что трудно творить следует делать с величайшей настойчивостью.
Конфуций.
Конфуций.
Слайд 30Домашнее задание:
1. параграф №14, упр. 5.
2. Решите задачи:
а) В состав некоторых сортов природного мела входит оксид железа (III). Предложите опыт для качественного определения содержания железа в образце мела.
б) В куске белого пшеничного хлеба 0,8 мг Fe. Сколько кусков нужно съесть в день для удовлетворения суточной потребности в этом элементе? Суточная потребность для подростков 11-18 лет составляет 18 мг.
б) В куске белого пшеничного хлеба 0,8 мг Fe. Сколько кусков нужно съесть в день для удовлетворения суточной потребности в этом элементе? Суточная потребность для подростков 11-18 лет составляет 18 мг.
Слайд 31 Не в количестве знаний заключается образование,
а в полном понимании и искусном применении всего того, что знаешь.
Дистервег.
Дистервег.