- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Углеводы (10 класс)
Содержание
- 1. Презентация по химии на тему Углеводы (10 класс)
- 2. Химические элементы Макроэлементы
- 3. Живая
- 4. Углеводы
- 5. Слайд 5
- 6. Дисахариды (С12Н22О11)Сахароза (тростниковый, свекловичный сахар)Лактоза
- 7. 1953г. – фр. химик Р.Лемье
- 8. Полисахариды
- 9. Крахмал и целлюлоза (С6Н10О5)n Сходства - растительное
- 10. Слайд 10
- 11. Слайд 11
- 12. Лабораторный опыт
Химические элементы Макроэлементы МикроэлементыС, Н, О, N – 98%
Слайд 2Химические элементы
Макроэлементы
Микроэлементы
С, Н, О, N – 98% 0,1% - Cu,B,J,Br
О-62,4% Fe,Zn,Mn
С-20,7%
Н-9,9%
N-5,0%
Mg,K,Ca,Na,P,S,Cl-1,9%
С, Н, О, N – 98% 0,1% - Cu,B,J,Br
О-62,4% Fe,Zn,Mn
С-20,7%
Н-9,9%
N-5,0%
Mg,K,Ca,Na,P,S,Cl-1,9%
Слайд 3 Живая и неживая природа
Сходства -
на атомном уровне
Различия - на молекулярном уровне
Живые организмы неорганические вещества
органические вещества
(белки, углеводы, жиры,
витамины, гормоны и т.д.)
Неживая природа неорганические вещества
Различия - на молекулярном уровне
Живые организмы неорганические вещества
органические вещества
(белки, углеводы, жиры,
витамины, гормоны и т.д.)
Неживая природа неорганические вещества
Слайд 4 Углеводы (сахариды)
Конечные
продукты фотосинтеза
Исходный материал для биосинтеза других соединений
В животных клетках – 1-2%
В растительных клетках – 85-90%
Общая формула – Сn(H2O)m
Соотношение Н и О - 1:2, как в H2O
В жизни человека
-продукты питания - бумага и изделия из нее
- волокна и ткани - изделия из древесины
Исходный материал для биосинтеза других соединений
В животных клетках – 1-2%
В растительных клетках – 85-90%
Общая формула – Сn(H2O)m
Соотношение Н и О - 1:2, как в H2O
В жизни человека
-продукты питания - бумага и изделия из нее
- волокна и ткани - изделия из древесины
Слайд 5
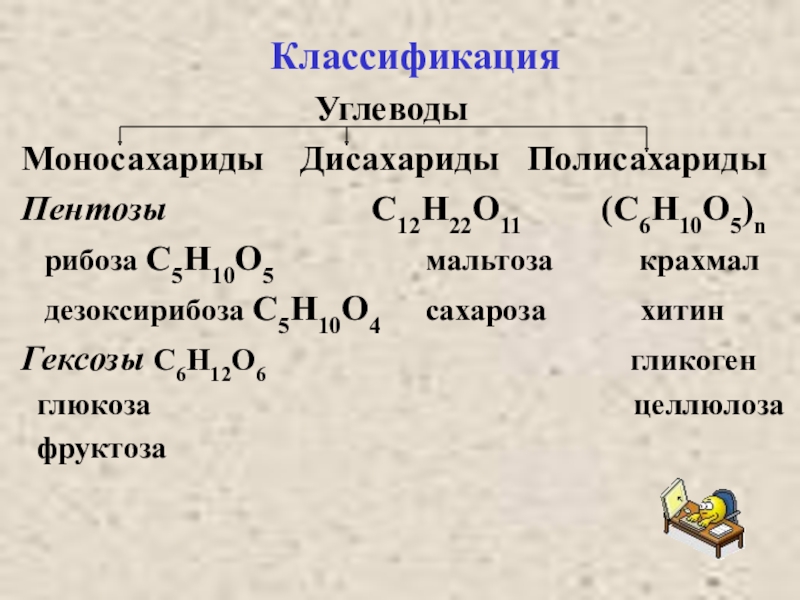
Классификация
Углеводы
Моносахариды Дисахариды Полисахариды
Пентозы С12Н22О11 (С6Н10О5)n
рибоза С5Н10О5 мальтоза крахмал
дезоксирибоза С5Н10О4 сахароза хитин
Гексозы С6Н12О6 гликоген
глюкоза целлюлоза
фруктоза
Углеводы
Моносахариды Дисахариды Полисахариды
Пентозы С12Н22О11 (С6Н10О5)n
рибоза С5Н10О5 мальтоза крахмал
дезоксирибоза С5Н10О4 сахароза хитин
Гексозы С6Н12О6 гликоген
глюкоза целлюлоза
фруктоза
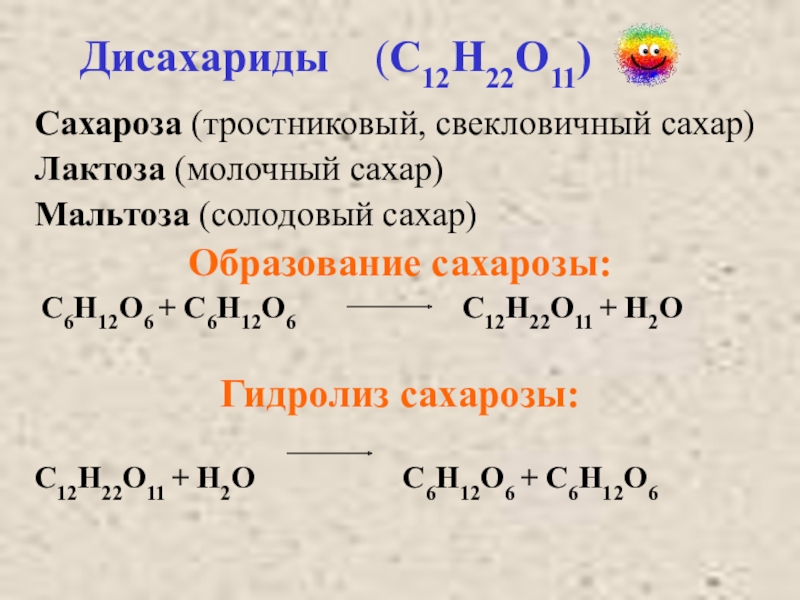
Слайд 6 Дисахариды (С12Н22О11)
Сахароза (тростниковый, свекловичный сахар)
Лактоза (молочный сахар)
Мальтоза (солодовый сахар)
Образование
сахарозы:
C6H12O6 + C6H12O6 С12Н22О11 + H2O
Гидролиз сахарозы:
С12Н22О11 + H2O C6H12O6 + C6H12O6
C6H12O6 + C6H12O6 С12Н22О11 + H2O
Гидролиз сахарозы:
С12Н22О11 + H2O C6H12O6 + C6H12O6
Слайд 7 1953г. – фр. химик Р.Лемье – синтез сахарозы («покорение
Эвереста органической химии»)
В промышленности сахарозу получают из сока сахарной свеклы (16-21%), сахарного тростника (14-16%), канадского клена, земляной груши (топинамбур)
Дисахариды хорошо растворимы в воде, кристаллические вещества, сладкие на вкус
В промышленности сахарозу получают из сока сахарной свеклы (16-21%), сахарного тростника (14-16%), канадского клена, земляной груши (топинамбур)
Дисахариды хорошо растворимы в воде, кристаллические вещества, сладкие на вкус
Слайд 8 Полисахариды
биополимеры
углеводы, которые гидролизуются
(разлагаются водой) с образованием молекул моносахаридов
гидролиз
(С6Н10О5)n + m H2O K t n C6H12O6
полисахарид глюкоза
поликонденсация (образование полимера, с выделением побочного низкомолекулярного вещества (чаще всего H2O)
n C6H12O6 (С6Н10О5)n + m H2O
глюкоза полисахарид
гидролиз
(С6Н10О5)n + m H2O K t n C6H12O6
полисахарид глюкоза
поликонденсация (образование полимера, с выделением побочного низкомолекулярного вещества (чаще всего H2O)
n C6H12O6 (С6Н10О5)n + m H2O
глюкоза полисахарид
Слайд 9Крахмал и целлюлоза (С6Н10О5)n
Сходства - растительное происхождение
- получают поликонденсацией из молекул глюкозы
Различия
Слайд 12 Лабораторный опыт
В пробирку насыпьте немного
порошка крахмала. Прилейте воды и взболтайте смесь. Что можно сказать о растворимости крахмала в воде?
Вылейте взвесь крахмала в воде в химический стакан с горячей водой и прокипятите ее. Что наблюдаете?
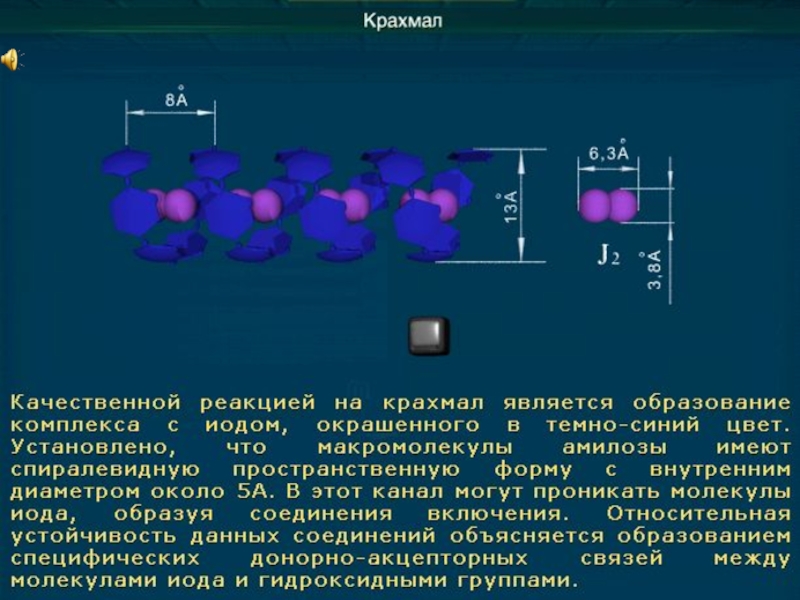
3. В пробирку с 2- 3 мл полученного во втором опыте крахмального клейстера добавьте каплю спиртового раствора иода. Что наблюдаете?
Вылейте взвесь крахмала в воде в химический стакан с горячей водой и прокипятите ее. Что наблюдаете?
3. В пробирку с 2- 3 мл полученного во втором опыте крахмального клейстера добавьте каплю спиртового раствора иода. Что наблюдаете?