- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Повторяем амины и аминокислоты.
Содержание
- 1. Повторяем амины и аминокислоты.
- 2. АминыАми́ны — органические соединения, производные аммиака, в
- 3. По числу замещённых атомов водорода различают соответственно
- 4. НоменклатураК названию органических остатков, связанных с азотом,
- 5. Химические свойстваАмины, являясь производными аммиака, имеют сходное
- 6. Алкиламины являются сильными основаниями, ариламины менее основны.Водные
- 7. Амины присоединяют галогеналканы RCl, с образованием донорно-акцепторной
- 8. Если в качестве исходных соединений взять диамин
- 9. Вторичные амины образуют с азотистой кислотой желтые,
- 10. ПолучениеВосстановление азотсодержащих соединений: нитросоединений(реакция Зинина).Эту реакцию впервые
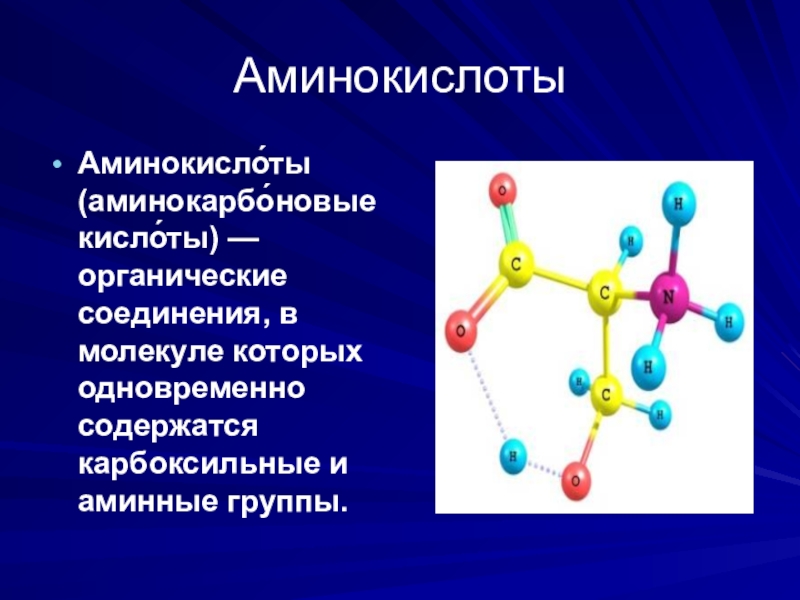
- 11. АминокислотыАминокисло́ты (аминокарбо́новые кисло́ты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.
- 12. Общие химические свойства1. Аминокислоты могут проявлять как
- 13. 2. Важной особенностью аминокислот является их способность
- 14. D-аминокислоты в живых организмахОптические изомеры аминокислот претерпевают
- 15. Сходным образом образуются пептидные антибиотики бактериального происхождения,
- 16. Слайд 16
- 17. Слайд 17
АминыАми́ны — органические соединения, производные аммиака, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы.
Слайд 2Амины
Ами́ны — органические соединения, производные аммиака, в молекуле которого один, два
или три атома водорода замещены на углеводородные радикалы.
Слайд 3По числу замещённых атомов водорода различают соответственно первичные, (R-NH2) вторичные (R-NH-R)
и третичные амины. Четвертичная аммониевая соль вида [R4N]+Cl- является органическим аналогом аммониевой соли.
По характеру органической группы, связанной с азотом, различают алифатические CH3-N< и ароматические С6H5-N< b ;и жирно-алифатические (содержат ароматический и алифатический радикалы) амины.
По числу NH2-групп в молекуле амины делят на моноамины, диамины, триамины и т. д.
По характеру органической группы, связанной с азотом, различают алифатические CH3-N< и ароматические С6H5-N< b ;и жирно-алифатические (содержат ароматический и алифатический радикалы) амины.
По числу NH2-групп в молекуле амины делят на моноамины, диамины, триамины и т. д.
Слайд 4Номенклатура
К названию органических остатков, связанных с азотом, добавляют слово «амин», при
этом группы упоминают в алфавитном порядке: CH3NHC3Н7 — метилпропиламин, CH3N(С6Н5)2 — метилдифениламин. Для высших аминов название составляется, взяв за основу углеводород, прибавлением приставки «амино», «диамино», «триамино», указывая числовой индекс атома углерода:
2-аминопентан
Для некоторых аминов используются тривиальные названия: С6Н5NH2 — анилин (систематическое название — фениламин).
2-аминопентан
Для некоторых аминов используются тривиальные названия: С6Н5NH2 — анилин (систематическое название — фениламин).
Слайд 5Химические свойства
Амины, являясь производными аммиака, имеют сходное с ним строение и
проявляют подобные ему свойства. Для них также характерно образование донорно-акцепторной связи. Азот предоставляет неподеленную электронную пару, исполняя роль донора. В качестве акцептора электоронов может выступать, например, протон Н+, образуя ион R3NH+. Возникшая ковалентная связь N-H полностью эквивалентна остальным связям N-H в амине.
Слайд 6
Алкиламины являются сильными основаниями, ариламины менее основны.
Водные растворы алифатических аминов проявляют
щелочную реакцию, так как при их взаимодействии с водой образуются гидроксиды алкиламмония, аналогичные гидроксиду аммония:
C2H5NH2 + H2O → [C2H5NH3]+ + OH-
Взаимодействуя с кислотами, амины образуют алкиламиновые соли, в большинстве случаев растворимые в воде. Например, амины присоединяют галогеноводороды:
RNH2 + HCl → [RNH3]Cl-
C2H5NH2 + H2O → [C2H5NH3]+ + OH-
Взаимодействуя с кислотами, амины образуют алкиламиновые соли, в большинстве случаев растворимые в воде. Например, амины присоединяют галогеноводороды:
RNH2 + HCl → [RNH3]Cl-
Слайд 7
Амины присоединяют галогеналканы RCl, с образованием донорно-акцепторной связи N-R, которая также
эквивалентна уже имеющимся.
При нагревании с карбоновыми кислотами, их ангидридами, хлорангидридами или сложными эфирами первичные и вторичные амины ацилируются с образованием N-замещенных амидов, соединений с фрагментом -С(О)N<:
Реакция с ангидридами протекает в мягких условиях. Ещё легче реагируют хлорангидриды, реакция проводится в присутствии основания, чтобы свзяать образующийся HCl.
При нагревании с карбоновыми кислотами, их ангидридами, хлорангидридами или сложными эфирами первичные и вторичные амины ацилируются с образованием N-замещенных амидов, соединений с фрагментом -С(О)N<:
Реакция с ангидридами протекает в мягких условиях. Ещё легче реагируют хлорангидриды, реакция проводится в присутствии основания, чтобы свзяать образующийся HCl.
Слайд 8
Если в качестве исходных соединений взять диамин и дикарбоновую кислоту, то
они взаимодействуют по такой же схеме, но поскольку каждое соединение содержит две реагирующие группы, то образуется полиамид.
Первичные и вторичные амины взаимодействуют с азотистой кислотой различным образом. Из первичных аминов образуются первичные спирты:
C2H5NH2 + HNO2 → C2H5OH + N2 +H2O
Первичные и вторичные амины взаимодействуют с азотистой кислотой различным образом. Из первичных аминов образуются первичные спирты:
C2H5NH2 + HNO2 → C2H5OH + N2 +H2O
Слайд 9
Вторичные амины образуют с азотистой кислотой желтые, трудно растворимые нитрозамины —
соединения, содержащие фрагмент >N-N=O:
(C2H5)2NH + HNO2 → (C2H5)2N-N=O + H2O
Третичные амины при обычной температуре с азотистой кислотой не реагируют,
Конденсация первичных аминов с альдегидами и кетонами приводит к образованию иминов или так называемых оснований Шиффа — соединений, содержащих фрагмент -N=C<:
При горении амин выделяет кроме воды и углекислого газа ещё и азот.
(C2H5)2NH + HNO2 → (C2H5)2N-N=O + H2O
Третичные амины при обычной температуре с азотистой кислотой не реагируют,
Конденсация первичных аминов с альдегидами и кетонами приводит к образованию иминов или так называемых оснований Шиффа — соединений, содержащих фрагмент -N=C<:
При горении амин выделяет кроме воды и углекислого газа ещё и азот.
Слайд 10Получение
Восстановление азотсодержащих соединений:
нитросоединений(реакция Зинина).
Эту реакцию впервые осуществил Н. Н. Зинин
в 1842 г.. Действуя на нитробензол сульфидом аммония, он получил анилин:
C6H5NO2 + 3(NH4)2S → C6H5NH2 + 6NH3 + 3S + 2H2O
Алкилирование аммиака (реакция Гофмана)
C6H5NO2 + 3(NH4)2S → C6H5NH2 + 6NH3 + 3S + 2H2O
Алкилирование аммиака (реакция Гофмана)
Слайд 11Аминокислоты
Аминокисло́ты (аминокарбо́новые кисло́ты) — органические соединения, в молекуле которых одновременно содержатся
карбоксильные и аминные группы.
Слайд 12Общие химические свойства
1. Аминокислоты могут проявлять как кислотные свойства, обусловленные наличием
в их молекулах карбоксильной группы -COOH, так и основные свойства, обусловленные аминогруппой -NH2. Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов.
Цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH3+, а карбоксигруппа — в виде -COO-. Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот.
Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп. Для этих аминокислот трудно говорить о каком-то конкретном цвиттер-ионе.
Цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH3+, а карбоксигруппа — в виде -COO-. Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот.
Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп. Для этих аминокислот трудно говорить о каком-то конкретном цвиттер-ионе.
Слайд 132. Важной особенностью аминокислот является их способность к поликонденсации, приводящей к
образованию полиамидов, в том числе пептидов, белков и нейлона-66.
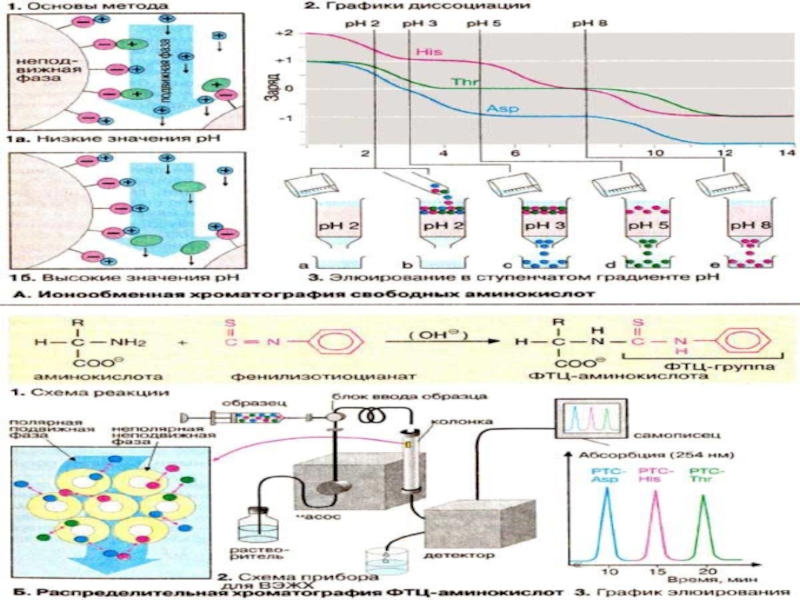
3. Изоэлектрической точкой аминокислоты называют значение pH, при котором максимальная доля молекул аминокислоты обладает нулевым зарядом. При таком pH аминокислота наименее подвижна в электрическом поле, и данное свойство можно использовать для разделения аминокислот, а также белков и пептидов.
4. Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов.
3. Изоэлектрической точкой аминокислоты называют значение pH, при котором максимальная доля молекул аминокислоты обладает нулевым зарядом. При таком pH аминокислота наименее подвижна в электрическом поле, и данное свойство можно использовать для разделения аминокислот, а также белков и пептидов.
4. Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов.
Слайд 14D-аминокислоты в живых организмах
Оптические изомеры аминокислот претерпевают медленную самопроизвольную неферментативную рацемизацию.
Например, в белке дентине (входит в состав зубов) L-аспартат переходит в D-форму со скоростью 0,1 % в год, что может быть использовано для определения возраста биологических объектов.
С развитием следового аминокислотного анализа D-аминокислоты были обнаружены сначала в составе клеточных стенок некоторых бактерий (1966), а затем и в тканях высших организмов. Так, D-аспартат и D-метионин предположительно являются нейромедиаторами у млекопитающих.
В состав некоторых пептидов входят D-аминокислоты, образующиеся при посттрансляционной модификации. Например, D-метионин и D-аланин входят в состав опиоидных гептапептидов кожи южноамериканских амфибий филломедуз (дерморфина, дермэнкефалина и делторфинов). Наличие D-аминокислот определяет высокую биологическую активность этих пептидов как анальгетиков.
С развитием следового аминокислотного анализа D-аминокислоты были обнаружены сначала в составе клеточных стенок некоторых бактерий (1966), а затем и в тканях высших организмов. Так, D-аспартат и D-метионин предположительно являются нейромедиаторами у млекопитающих.
В состав некоторых пептидов входят D-аминокислоты, образующиеся при посттрансляционной модификации. Например, D-метионин и D-аланин входят в состав опиоидных гептапептидов кожи южноамериканских амфибий филломедуз (дерморфина, дермэнкефалина и делторфинов). Наличие D-аминокислот определяет высокую биологическую активность этих пептидов как анальгетиков.
Слайд 15
Сходным образом образуются пептидные антибиотики бактериального происхождения, действующие против грамположительных бактерий
— низин , субтилин и эпидермин.
Гораздо чаще D-аминокислоты входят в состав пептидов и их производных, образующихся путем нерибосомного синтеза в клетках грибов и бактерий. Видимо. в этом случае исходным материалом для синтеза служат также L-аминокислоты. которые изомеризуются одной из субъединиц ферментного комплекса, осуществляющего синтез пептида.
Гораздо чаще D-аминокислоты входят в состав пептидов и их производных, образующихся путем нерибосомного синтеза в клетках грибов и бактерий. Видимо. в этом случае исходным материалом для синтеза служат также L-аминокислоты. которые изомеризуются одной из субъединиц ферментного комплекса, осуществляющего синтез пептида.