и биологии МБОУ «СОШ № 9»
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 9 класс на тему Азотная кислота
Содержание
- 1. Презентация по химии 9 класс на тему Азотная кислота
- 2. Азотная кислота- бесцветная жидкость,
- 3. Карл Вильгельм Шееле (1742-1786 г.г.) Впервые описал химические свойства азотной кислоты.
- 4. НNО3 –проявляет все типичные свойства кислот. Изменяет
- 5. Общие химические свойства НNO3Азотная кислота взаимодействует с
- 6. Задание: Закончить уравнения практически осуществимых реакций.
- 7. Окислительные свойства НNO3 Азотная
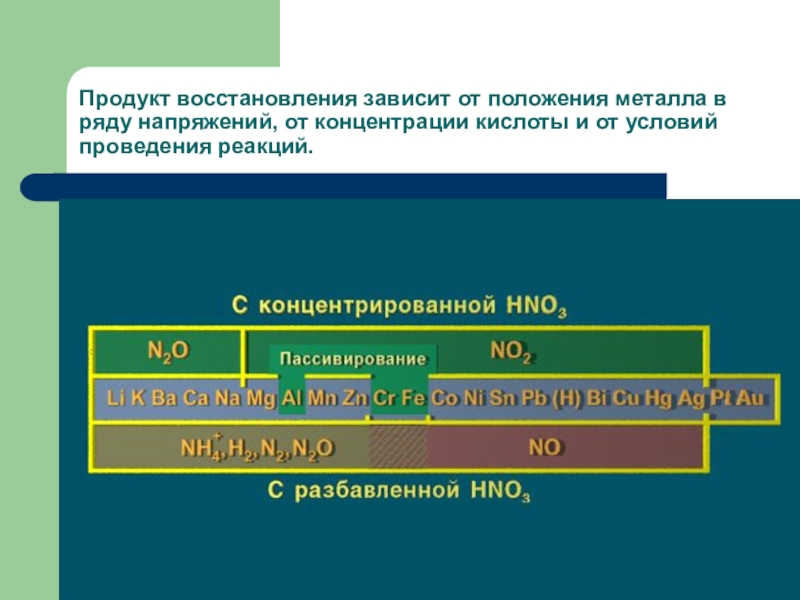
- 8. Продукт восстановления зависит от положения металла в
- 9. Химический эксперимент
- 10. Азотная кислота широко применяется в химической промышленности
- 11. Итоговое задание: установить соответствиеCu+ HNO3 (конц.)=Al(OH)3+ HNO3=Fe+
- 12. Правильные ответы к итоговому заданию.1-б2-а3-г4-в5-д
Азотная кислота- бесцветная жидкость, которая «дымится» на воздухе. При хранении на свету концентрированная азотная кислота желтеет, так как частично разлагается с образованием бурого газа - NO2: 4НNO3=2Н2О+4NO2 ↑+О2 ↑
Слайд 2
Азотная кислота- бесцветная жидкость, которая «дымится» на воздухе.
При хранении на свету концентрированная азотная кислота желтеет, так как частично разлагается с образованием бурого газа - NO2:
4НNO3=2Н2О+4NO2 ↑+О2 ↑
4НNO3=2Н2О+4NO2 ↑+О2 ↑
Физические свойства НNO
3
Слайд 4НNО3 –проявляет все типичные свойства кислот. Изменяет окраску индикаторов, например, лакмуса
на красный цвет.
Химические свойства HNO
3
Слайд 5Общие химические свойства НNO3
Азотная кислота взаимодействует с оксидами металлов:
2 НNO3+CuO= Сu (NO3)2+Н2О
Азотная кислота взаимодействует с гидроксидами металлов:
НNO3+ КОН= КNO3+Н2О
Азотная кислота взаимодействует с солями:
2НNO3+СаСО3= Са (NO3)2+Н2О+СО2
Азотная кислота взаимодействует с гидроксидами металлов:
НNO3+ КОН= КNO3+Н2О
Азотная кислота взаимодействует с солями:
2НNO3+СаСО3= Са (NO3)2+Н2О+СО2
Слайд 6Задание:
Закончить уравнения практически осуществимых реакций. Расставить коэффициенты.
а) НNО3+Мg(OH)2=
б)
НNО3+К2СО3=
в) НNО3+СО2 =
г) НNО3+СаО =
д) НNО3+Н2SО4=
в) НNО3+СО2 =
г) НNО3+СаО =
д) НNО3+Н2SО4=
Слайд 7Окислительные свойства НNO3
Азотная кислота по особому реагирует
с металлами. Ни один из металлов не вытесняет Н2 из кислоты. Это объясняется тем, что НNO3 является очень сильным окислителем, в ней азот имеет максимальную степень окисления +5. именно он и будет восстанавливаться при взаимодействии с металлами.
Слайд 8Продукт восстановления зависит от положения металла в ряду напряжений, от концентрации
кислоты и от условий проведения реакций.
Слайд 10Азотная кислота широко применяется в химической промышленности для производства азотных удобрений,
пластмасс, искусственных волокон, органических красителей и лаков, лекарств и взрывчатых веществ.
Применение
HNO
3
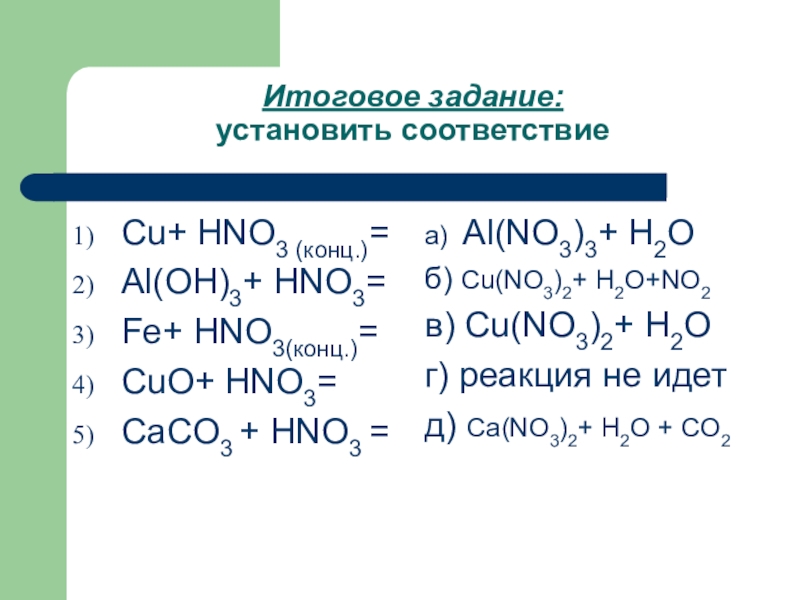
Слайд 11Итоговое задание:
установить соответствие
Cu+ HNO3 (конц.)=
Al(OH)3+ HNO3=
Fe+ HNO3(конц.)=
CuO+ HNO3=
CaCO3 + HNO3 =
а)
Al(NO3)3+ H2O
б) Cu(NO3)2+ H2O+NO2
в) Cu(NO3)2+ H2O
г) реакция не идет
д) Cа(NO3)2+ H2O + СО2
б) Cu(NO3)2+ H2O+NO2
в) Cu(NO3)2+ H2O
г) реакция не идет
д) Cа(NO3)2+ H2O + СО2