- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку химии 8 класс на тему: Соли
Содержание
- 1. Презентация к уроку химии 8 класс на тему: Соли
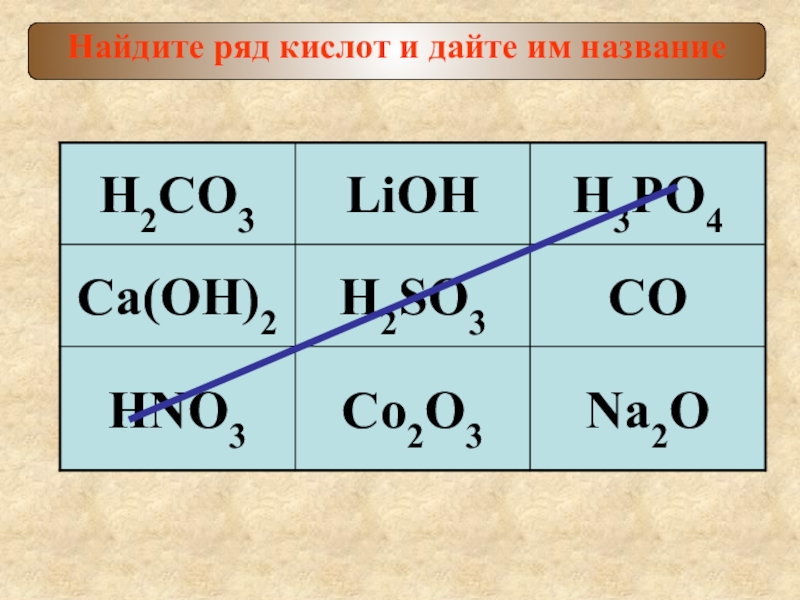
- 2. Найдите ряд кислот и дайте им название
- 3. 1) NаOН + ….. → NаNO3
- 4. Расположите формулы веществ в порядке возрастания основных
- 5. электролиты, при диссоциации которых образуются катионы металлов и анионы кислотных остатковСоли
- 6. Классификация солейМg(НSO4)2КНSO3ZnС12Al2S3CаОНС1(СuОН)2СО3В начале XIX века шведский химик
- 7. Способы получения солей2. Взаимодействие кислот с металлами:1.
- 8. Способы получения солей7. Взаимодействие солей с металлами:6.
- 9. Химические свойства солей2. Соль + кислота →
- 10. Дайте названия веществамNa2СO3СаSiO3BaSO3CuС12АgNO3FeSСульфид железа (II)Нитрат серебраХлорид меди (II)Сульфит барияСиликат кальцияКарбонат натрия
- 11. а) COб) NaOHв) НС1г) Feд) ВаС12е) Н2ОС какими из перечисленных веществ будет реагировать сульфат меди(II)?
- 12. 1.Формула соли это: а) NaOH
- 13. Б В Г А ВОТВЕТЫ
- 14. Домашнее задание
- 15. ЗакреплениеСаСO3 СаО Са(ОН)2 СаСО3
Слайд 31) NаOН + ….. → NаNO3 + Н2О
2) Н2SO4 +
3) …… + HCl → AgCl↓ + HNO3
4) ….. + Н2SО4 → MgSО4 + H2
НNO3
AgNО3
Mg
Вставьте в уравнения химических реакций
пропущенные формулы веществ
и расставьте коэффициенты
MgSО4
Слайд 4Расположите формулы веществ в порядке
возрастания основных свойств:
Ca(OH)2, Mg(OH)2, Ва(OH)2
Al2O3, Na2O,
Расположите формулы веществ в порядке
усиления кислотных свойств:
HNO3, HB, H2CO3
SO3, P2O5, N2O5
Mg(OH)2, Ca(OH)2, Ba(OH)2
Al2O3, MgO, Na2O
HB, H2CO3, HNO3
P2O5, N2O5, SO3
Слайд 5электролиты, при диссоциации которых образуются катионы металлов и анионы кислотных остатков
Соли
Слайд 6Классификация солей
Мg(НSO4)2
КНSO3
ZnС12
Al2S3
CаОНС1
(СuОН)2СО3
В начале XIX века шведский химик Й.Берцелиус предложил рассматривать соли
реакции кислот с основаниями или как соединения, полученные замещением атомов водорода в кислоте на металл. По этому признаку различают:
Слайд 7Способы получения солей
2. Взаимодействие кислот с металлами:
1. Взаимодействие кислот с основаниями:
3.
4. Взаимодействием оснований с солями:
НC1 + NaOH → NaC1 + H2O
2НС1 + Mg → MgC12 + H2
Ca(ОН)2 + CO2 → CaCO3 + H2O
2KОН + MgSO4 → K2SO4 + Mg(OH)2
Слайд 8Способы получения солей
7. Взаимодействие солей с металлами:
6. Взаимодействие солей между собой:
8.
2К3РО4 + 3MgCl2 → Mg3(PO4)2 + 6KCl
СuС12 + Fe → FeC12 + Cu
Fe + S → FeS
5. Взаимодействием основных оксидов с кислотными:
СО2 + MgO → MgСO3
Слайд 9Химические свойства солей
2. Соль + кислота → другая соль + другая
1. Соль + щелочь → другая соль + другое основание
3. Соль1 + соль 2 → соль3 + соль4
4. Соль + металл → другая соль + другой металл
Условие: должен образоваться осадок
1. Ме должен стоять левее, чем тот, который входит в состав соли
2. Ме не должен взаимодействовать с водой.
Условия:
FeC13 + 3NaOH → Fe(OH)3↓ + 3NaC1
ВaС12 + H2SO4 → ВaSO4↓ + 2HС1
BaC12 + 2AgNO3 → 2AgC1↓ + Ba(NO3)2
CuSO4 + Fe → FeSO4 + Cu ↓
Слайд 10Дайте названия веществам
Na2СO3
СаSiO3
BaSO3
CuС12
АgNO3
FeS
Сульфид железа (II)
Нитрат серебра
Хлорид меди (II)
Сульфит бария
Силикат кальция
Карбонат натрия
Слайд 11а) CO
б) NaOH
в) НС1
г) Fe
д) ВаС12
е) Н2О
С какими из перечисленных веществ
будет реагировать сульфат меди(II)?
Слайд 121.Формула соли это:
а) NaOH б) CuC12
2. Лакмус в растворе хлорида натрия:
а) синий б) красный в) фиолетовый г) малиновый
3. С раствором нитрата серебра взаимодействует:
а) оксид лития в) оксид кремния
б) гидроксид меди(II) г) хлорид натрия
4. С раствором сульфата меди не взаимодействует:
а) NaС1 б) ВаС12 в) NaOH г) Fe
5. Пара веществ взаимодействующих друг с другом:
а) Na2SO4 u SiO2 в) FeSO4 u КOH
б) КС1 u СO г) ВаSO4 u НС1
ПРОВЕРЬ СЕБЯ
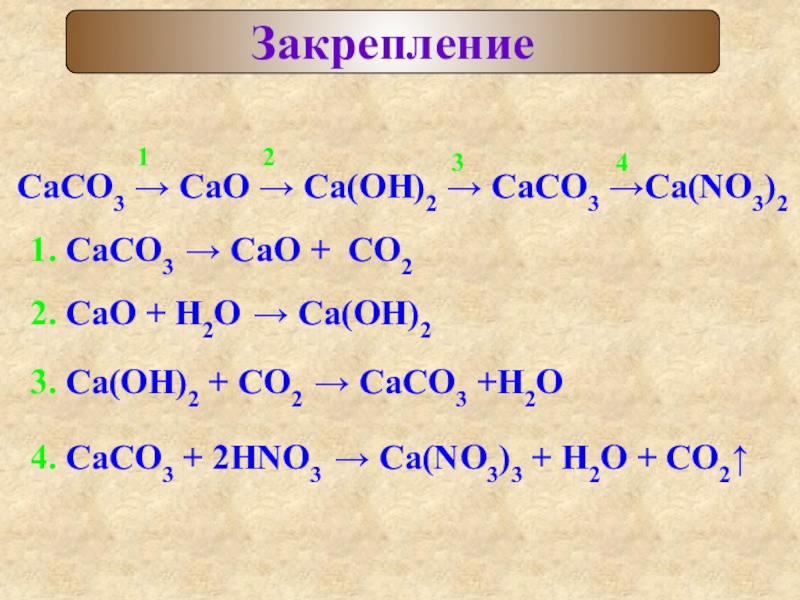
Слайд 15Закрепление
СаСO3 СаО Са(ОН)2 СаСО3 Са(NО3)2
1. СаСO3 СаО
2. СаO + Н2О Са(ОН)2
3. Са(ОН)2 + СО2 СаСО3 +Н2О
4. СаСО3 + 2НNО3 Са(NО3)3 + Н2О + CO2
1
2
3
4