- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Аминокислоты с рисунками с урока.
Содержание
- 1. Аминокислоты с рисунками с урока.
- 2. Общее определениеАминокислоты - органические соединения, в молекуле которых
- 3. Общие химические свойства1. Аминокислоты могут проявлять как
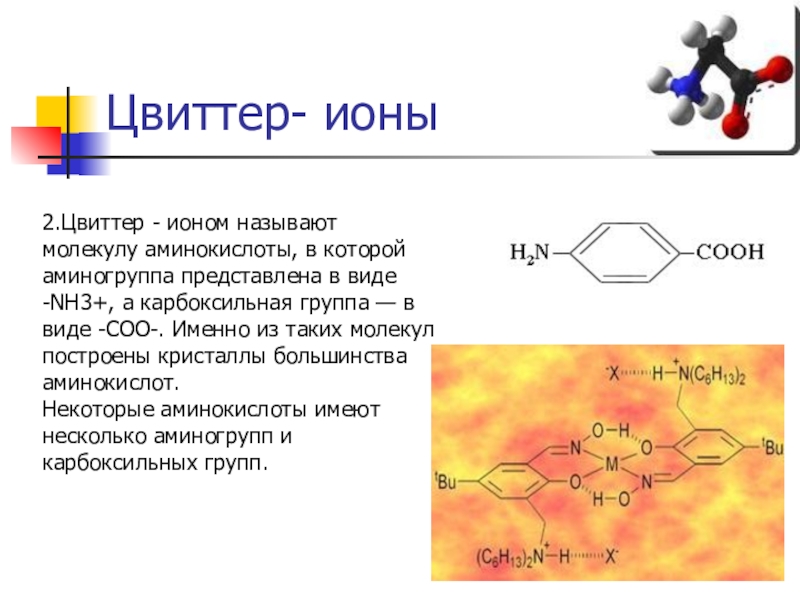
- 4. Цвиттер- ионы2.Цвиттер - ионом называют молекулу аминокислоты,
- 5. Особенности аминокислот3. Важной особенностью аминокислот является их
- 6. Оптическая изомерияВсе входящие в состав живых организмов
- 7. По R-группам:Неполярные: аланин, валин, изолейцин, лейцин, метионин,
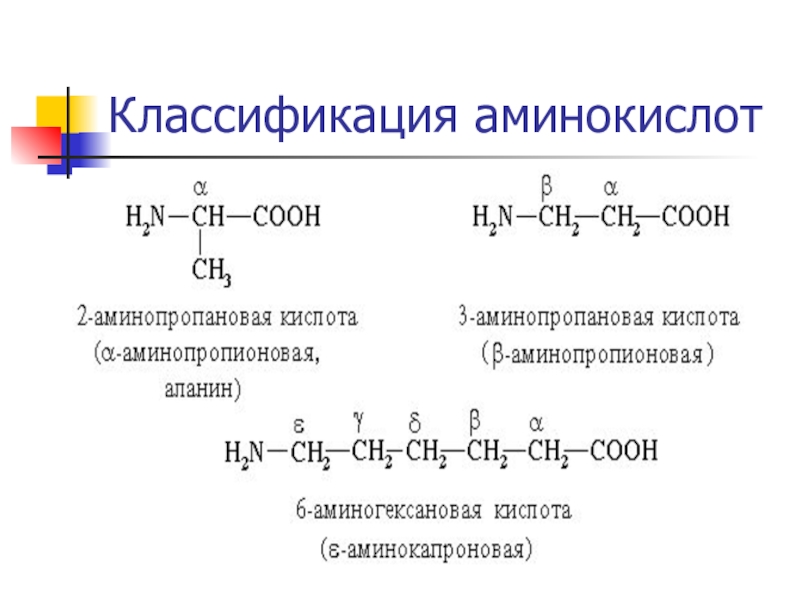
- 8. Классификация аминокислот
- 9. По функциональным группамАлифатические:Моноаминомонокарбоновые: аланин, валин, глицин, изолейцин,
- 10. По аминоацил-тРНК-синтетазам Класс I лейцин, изолейцин, валин,
- 11. Незаменимые: Триптофан, Фенилаланин, Лизин, Треонин, Метионин, Лейцин,
- 12. 10 незаменимых аминокислот
- 13. Незаменимые аминокислотыНезаменимые аминокислоты — необходимые аминокислоты, которые не
- 14. =)
- 15. Несмотря на то, что самостоятельно организм не
- 16. Заменимые аминокислотыЗаменимые аминокислоты могут синтезироваться в организме.
- 17. «Миллеровские» аминокислоты Обобщенное название аминокислот,
- 18. Родственные соединенияВ медицине, ряд веществ, способных выполнять
- 19. СПАСИБО ЗА ВНИМАНИЕ!=)
Общее определениеАминокислоты - органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.
Слайд 2Общее определение
Аминокислоты - органические соединения, в молекуле которых одновременно содержатся карбоксильные и
аминные группы.
Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.
Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.
Слайд 3Общие химические свойства
1. Аминокислоты могут проявлять как кислотные свойства, обусловленные наличием
в их молекулах карбоксильной группы -COOH, так и основные свойства, обусловленные аминогруппой -NH2. Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов.
Слайд 4Цвиттер- ионы
2.Цвиттер - ионом называют молекулу аминокислоты, в которой аминогруппа представлена
в виде -NH3+, а карбоксильная группа — в виде -COO-. Именно из таких молекул построены кристаллы большинства аминокислот.
Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп.
Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп.
Слайд 5Особенности аминокислот
3. Важной особенностью аминокислот является их способность к поликонденсации, приводящей
к образованию полиамидов, в том числе пептидов, белков и нейлона-66.
4. Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов
4. Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов
Слайд 6Оптическая изомерия
Все входящие в состав живых организмов α-аминокислоты, кроме глицина, содержат
асимметричный атом углерода (треонин и изолейцин содержат два асимметричных атома) и обладают оптической активностью. Почти все встречающиеся в природе α-аминокислоты имеют L-форму, и лишь L-аминокислоты включаются в состав белков, синтезируемых на рибосомах.
Слайд 7По R-группам:
Неполярные: аланин, валин, изолейцин, лейцин, метионин, пролин, триптофан, фенилаланин, глицин.
Полярные, незаряженные: аспарагин, глутамин, серин, тирозин, треонин, цистеин.
Полярные ,заряженные отрицательно: аспарагиновая кислота, глутаминовая кислота.
Полярные ,заряженные положительно : аргинин, гистидин, лизин.
Классификация стандартных аминокислот
Слайд 9По функциональным группам
Алифатические:
Моноаминомонокарбоновые: аланин, валин, глицин, изолейцин, лейцин.
Оксимоноаминокарбоновые: серин, треонин
Моноаминодикарбоновые: аспарагиновая кислота, глутаминовая кислота.
Амиды Моноаминодикарбоновых: аспарагин, глутамин.
Диаминомонокарбоновые: аргинин, гистидин, лизин.
Серосодержащие: цистеин (цистин), метионин.
Ароматические: фенилаланин, тирозин.
Гетероциклические: триптофан, гистидин, пролин .
Иминокислоты: пролин.
Слайд 10По аминоацил-тРНК-синтетазам
Класс I
лейцин, изолейцин, валин, цистеин, метионин, аргинин, глютаминовая кислота,
глутамин, тирозин.
Класс II
аланин, глицин, пролин, гистидин, треонин, серин, аспарагин, аспарагиновая кислота, лизин, фенилаланин.
Класс II
аланин, глицин, пролин, гистидин, треонин, серин, аспарагин, аспарагиновая кислота, лизин, фенилаланин.
Слайд 11
Незаменимые: Триптофан, Фенилаланин, Лизин, Треонин, Метионин, Лейцин, Изолейцин, Валин .
Заменимые: Тирозин,
Цистеин ,Гистидин, Аргинин, Глицин, Аланин ,Серин ,Глутамат ,Глутамин, Аспартат, Аспарагин, Пролин.
Некоторые заменимые аминокислоты синтезируются в организме человека в недостаточных количествах и должны поступать с пищей.
Некоторые заменимые аминокислоты синтезируются в организме человека в недостаточных количествах и должны поступать с пищей.
По способности человека синтезировать их из предшественников
Слайд 13Незаменимые аминокислоты
Незаменимые аминокислоты — необходимые аминокислоты, которые не могут быть синтезированы в
том или ином организме, в частности, в организме человека. Поэтому их поступление в организм с пищей необходимо.
Незаменимыми для взрослого здорового человека 8 аминокислот: валин, изолейцин, лейцин, лизин, метионин, треони́н, триптофан и фенилалани́н; для детей незаменимыми являются также аргинин и гистидин.
Незаменимыми для взрослого здорового человека 8 аминокислот: валин, изолейцин, лейцин, лизин, метионин, треони́н, триптофан и фенилалани́н; для детей незаменимыми являются также аргинин и гистидин.
Слайд 15Несмотря на то, что самостоятельно организм не способен синтезировать незаменимые аминокислоты,
их недостаток в некоторых случаях все же может быть частично компенсирован. Так например недостаток поступающего вместе с пищей незаменимого фенилаланина может быть частично замещен заменимым тирозином. Гомоцистеин вместе с необходимым количеством доноров метильных групп, снижает потребности в метионине, а глутаминовая кислота частично замещает аргинин.
Слайд 16Заменимые аминокислоты
Заменимые аминокислоты могут синтезироваться в организме. Однако за счет этого
эндогенного синтеза обеспечиваются только минимальные потребности организма, в связи с чем удовлетворение потребности организма в заменимых аминокислотах должно в основном осуществляться за счет поступления их в составе белков пищи.
Слайд 17«Миллеровские» аминокислоты
Обобщенное название аминокислот, получающихся в условиях, близких
к эксперименту Стенли Миллера 1953 года.
Это:
лейцин, изолейцин, валин, аланин, глицин, пролин, треонин, серин, глутаминовая кислота, аспарагиновая кислота.
Это:
лейцин, изолейцин, валин, аланин, глицин, пролин, треонин, серин, глутаминовая кислота, аспарагиновая кислота.
Слайд 18Родственные соединения
В медицине, ряд веществ, способных выполнять некоторые биологические функции аминокислот,
так же называют аминокислотами:
Таурин.
Таурин.