- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему урока: Молярный объём газов
Содержание
- 1. урока: Молярный объём газов
- 2. Слайд 2
- 3. Молярный объём газа — это объём газа количеством вещества 1 моль.
- 4. Vm
- 5. твёрдое веществожидкое веществогаз
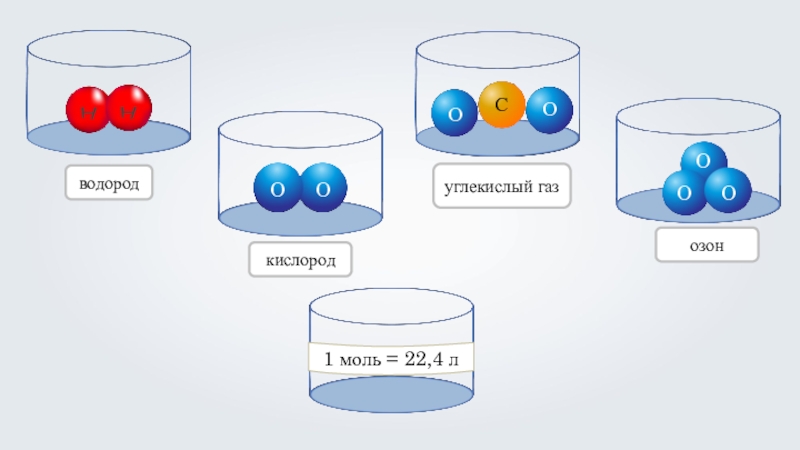
- 6. 1 моль = 22,4 лводородкислородуглекислый газозон
- 7. Нормальными условиями (н.у.) в химии принято называть
- 8. А. АвогадроВ равных объёмах разных газов при
- 9. Молярный объём — это физическая величина, равная отношению объёма вещества к количеству вещества.
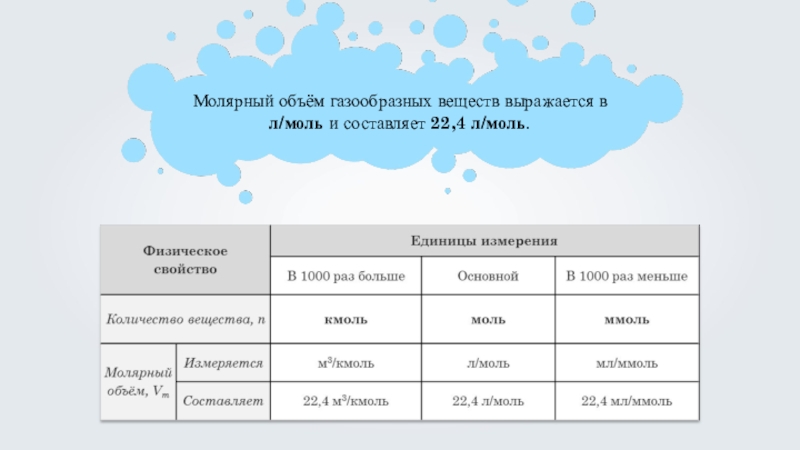
- 10. Молярный объём газообразных веществ выражается в л/моль и составляет 22,4 л/моль.
- 11. Задача 1.Какой объём при нормальных условиях займёт
- 12. Задача 2.Какой объём займёт при нормальных условиях
- 13. Задача 3.Определите массу и объём, занимаемый при
Слайд 7
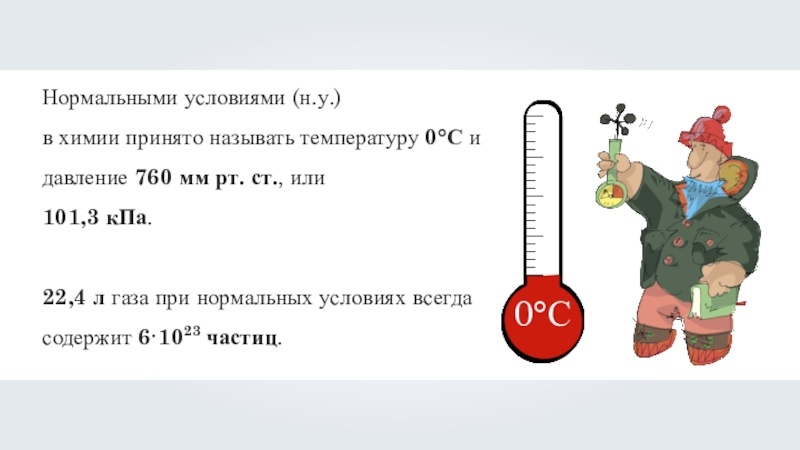
Нормальными условиями (н.у.)
в химии принято называть температуру 0°С и давление
101,3 кПа.
22,4 л газа при нормальных условиях всегда содержит 6·1023 частиц.
0°С
Слайд 8А. Авогадро
В равных объёмах разных газов при одинаковых условиях содержится одинаковое
Закон Авогадро (1811 г.)
Слайд 9
Молярный объём — это физическая величина, равная отношению объёма вещества к
Слайд 11Задача 1.
Какой объём при нормальных условиях займёт углекислый газ, взятый в
Дано:
n(CO2) =
= 0,5 моль (н.у.)
Решение.
V = Vm ∙ n.
V(CO2) — ?
V(CO2) = 22,4 л/моль ∙ 0,5 моль = 11,2 л.
Ответ: V(CO2) = 11,2 л.
Слайд 12Задача 2.
Какой объём займёт при нормальных условиях хлороводород HCl массой 14,6
Дано:
m(HCl) = 14,6 г
Решение.
V(HCl) — ?
Ответ: V(HCl) = 8,96 л.
n(HCl) = 14,6 г : 36,5 г/моль = 0,4 моль.
V(HCl) = Vm(HCl) ∙ n(HCl).
V(HCl) = 22,4 л/моль ∙ 0,4 моль = 8,96 л.
Слайд 13Задача 3.
Определите массу и объём, занимаемый при нормальных условиях 3,01 ∙
Дано:
N(CH4) =
= 3,01 ∙ 1026 (н.у.)
Решение.
m(CH4) — ?
n(CH4) = 3,01 ∙ 1026 : 6 ∙ 1023 = 500 (моль).
Ответ: V(CH4) = 11,2 м3, m(CH4) = 8 кг.
V(CH4) = 22,4 л ∙ 500 моль = 11,2 м3.
m(CH4) = M(CH4) ∙ n(CH4).
V(CH4) — ?
m(CH4) = 16 ∙ 500 = 8000 (г) = 8 (кг).