- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Урок Химические свойства кислот
Содержание
- 1. Урок Химические свойства кислот
- 2. Один опыт я ставлю выше, чем тысячу
- 3. Цели: 1. обучающая-Исследовать физические и
- 4. Цель урока:-Исследовать физические и химические свойства кислот,-Познакомиться
- 5. Задачи:Закрепить умение наблюдать за химическими реакциями, описывать
- 6. Актуализация Дайте определение классу кислот.Исходя из определения,
- 7. Что нас объединяет?
- 8. Выберите и назовите формулы кислот1) HCI,
- 9. Физические свойстважидкости (кроме кремниевой кислоты)без цветабез запахакислые на вкус
- 10. Химические свойства«Кислоты – едкие вещества, вызывающие сильнейшие
- 11. Техника безопасности от строгой химички.Ты в хим.
- 12. Действие индикаторов H2SO4 + лакмус ? красный
- 13. Электрохимический ряд напряжений
- 14. Взаимодействие с металлами ( до Н
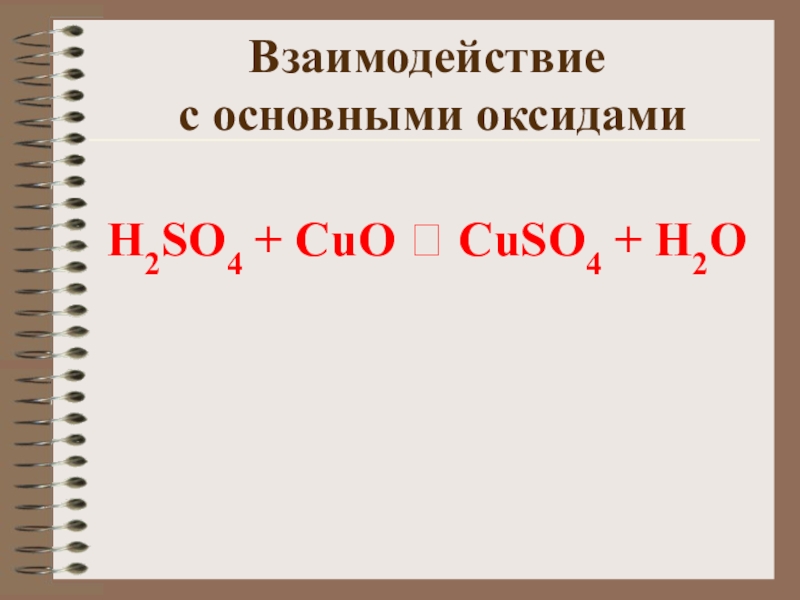
- 15. Взаимодействие с основными оксидамиH2SO4 + CuO ? CuSO4 + H2O
- 16. Взаимодействие с растворимыми основаниями (щелочами) H2SO4 + 2NaOH ? Na2SO4 + 2H2O
- 17. Взаимодействие с нерастворимыми основаниями H2SO4 + Cu(OH)2? ? CuSO4 + 2H2Осиний
- 18. Взаимодействие с солями H2SO4 + ВаCL2 ? BaSO4? + 2 HCLбелый
- 19. КИСЛОТАОснование ? соль + Н2О лакмус – красныйИндикатор метилоранж
- 20. Ответы на тестирование1. В2. В3. В4. В5. --6. А7. В
- 21. 5. Допишите возможные уравнения реакций:6HCl + 2Al
- 22. дополнительное заданиеС какими из перечисленных веществ вступает
- 23. 1. Определяем принадлежность заданных в условий веществ
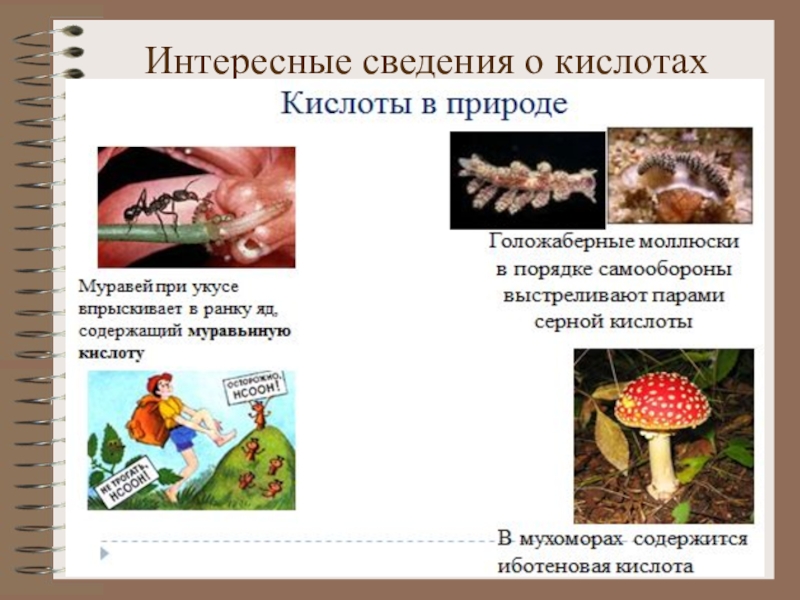
- 24. Интересные сведения о кислотах
- 25. Домашнее заданиеПар. 45, решить стр.155 №3,4,5
- 26. БЛАГОДАРЮ ЗА УРОК !
Один опыт я ставлю выше, чем тысячу мнений, рожденных только воображением. М.В.Ломоносов.
Слайд 3Цели:
1. обучающая
-Исследовать физические и химические свойства
кислот,
-Познакомиться с
электрохимическим рядом
напряжения металлов, показать принцип работы с ним.
--Совершенствовать знания о составе и номенклатуре кислот и солей,
-Совершенствовать умение пользоваться инструкцией и лабораторным оборудованием,
-Наблюдать и фиксировать результаты эксперимента,
-Соблюдать правила техники безопасности.
2. развивающая
-Развивать навыки самостоятельной работы, коммуникативные компетенции.
3. воспитательная.
-Воспитание аккуратности и последовательности в работе, бережного отношения к школьному имуществу.
напряжения металлов, показать принцип работы с ним.
--Совершенствовать знания о составе и номенклатуре кислот и солей,
-Совершенствовать умение пользоваться инструкцией и лабораторным оборудованием,
-Наблюдать и фиксировать результаты эксперимента,
-Соблюдать правила техники безопасности.
2. развивающая
-Развивать навыки самостоятельной работы, коммуникативные компетенции.
3. воспитательная.
-Воспитание аккуратности и последовательности в работе, бережного отношения к школьному имуществу.
Слайд 4Цель урока:
-Исследовать физические и химические свойства
кислот,
-Познакомиться с электрохимическим рядом
напряжения
металлов, показать принцип работы с ним.
-Совершенствовать знания о составе и номенклатуре кислот и солей,
-Совершенствовать умение пользоваться инструкцией и лабораторным оборудованием,
-Наблюдать и фиксировать результаты эксперимента,
-Соблюдать правила техники безопасности.
-Совершенствовать знания о составе и номенклатуре кислот и солей,
-Совершенствовать умение пользоваться инструкцией и лабораторным оборудованием,
-Наблюдать и фиксировать результаты эксперимента,
-Соблюдать правила техники безопасности.
Слайд 5Задачи:
Закрепить умение наблюдать за химическими реакциями, описывать их и делать выводы.
Продолжить
формирование умений и навыков по проведению химического эксперимента.
Формировать умение общаться и работать в группах.
Формировать умение общаться и работать в группах.
Слайд 6Актуализация
Дайте определение классу кислот.
Исходя из определения, выведите общую формулу кислот.
Кислот достаточно много, а можно ли их классифицировать.
На какие группы делятся кислоты по составу
( приведите примеры).
На какие группы делятся кислоты по оснoвности (приведите примеры).
Существует ли общий принцип составления названий кислот или у каждой кислоты свое индивидуальное название.
Слайд 8Выберите и назовите формулы кислот
1) HCI, CO2 ,
NaOH , H2SO4
2) NaCI , H3PO4 , HNO3 , H2S
3) СаО , H2CO3 , Н2О, Н2SiO3
4) Al2O3, H2SO3, HBr , CuSO4
2) NaCI , H3PO4 , HNO3 , H2S
3) СаО , H2CO3 , Н2О, Н2SiO3
4) Al2O3, H2SO3, HBr , CuSO4
Слайд 10Химические свойства
«Кислоты – едкие вещества, вызывающие сильнейшие ожоги, разрушают органические вещества»
- данное высказывание можно часто услышать о кислотах. Так ли это?
Слайд 11Техника безопасности от строгой химички.
Ты в хим. кабинет пришел
Так запомни кроха
Безопасность
хорошо,
Быть безруким плохо.
Ты над брюками держал
С кислотой пробирку?
Круто, парень, ты попал –
На штанишки с дыркой!
Быть безруким плохо.
Ты над брюками держал
С кислотой пробирку?
Круто, парень, ты попал –
На штанишки с дыркой!
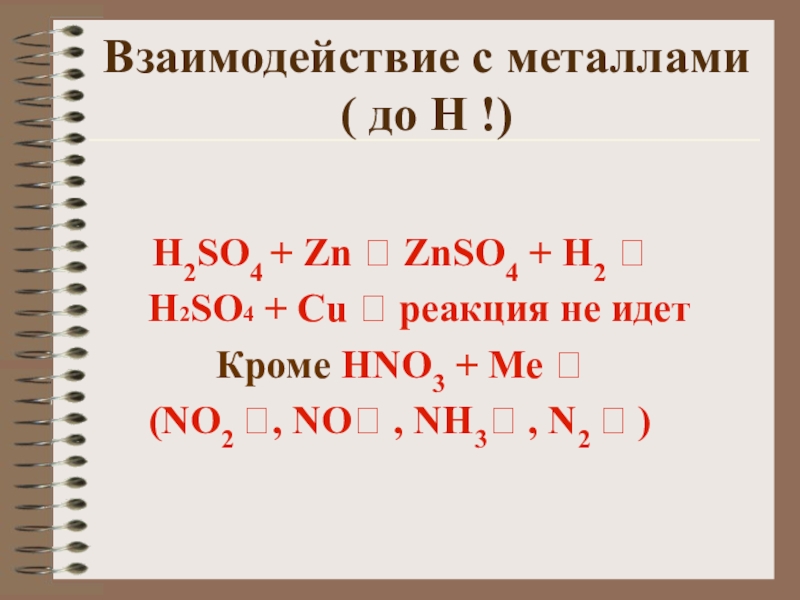
Слайд 14Взаимодействие с металлами
( до Н !)
H2SO4 + Zn ? ZnSO4
+ H2 ?
H2SO4 + Cu ? реакция не идет
Кроме HNO3 + Ме ?
(NO2 ?, NO? , NH3? , N2 ? )
H2SO4 + Cu ? реакция не идет
Кроме HNO3 + Ме ?
(NO2 ?, NO? , NH3? , N2 ? )
Слайд 19К
И
С
Л
О
Т
А
Основание ? соль + Н2О
лакмус – красный
Индикатор метилоранж – красный
фенолфталеин -
бесцветный
МехОу ? соль + Н2О
Ме ? соль + Н2 ?
HNO3+Me?H2 (NO2 ?, NO ?, NH3 ?, N2 ?)
+
+
+
+
/
Слайд 21
5. Допишите возможные уравнения реакций:
6HCl + 2Al = 2AlCl3 + 3H2
H2SO4
+ Hg = реакция не идет
3H2SO4 + Al2O3 = Al2(SO4)3 + 3H2O
3H2SO4 + 2Fe(OH)3 = Fe2(SO4)3 + 3H2O
KOH + HNO3 = KNO3 + H2O
Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
3H2SO4 + Al2O3 = Al2(SO4)3 + 3H2O
3H2SO4 + 2Fe(OH)3 = Fe2(SO4)3 + 3H2O
KOH + HNO3 = KNO3 + H2O
Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
Слайд 22дополнительное задание
С какими из перечисленных веществ вступает в реакцию хлороводородная (соляная)
кислота: Na2О, Сu, SO3, Zn? Составьте уравнения возможных реакций.
Слайд 231. Определяем принадлежность заданных в условий веществ к соответствующим классам и
тут же проверяем, реагируют ли они с кислотами. Получается:
• Na2О — основный оксид — реагирует (получается соль и вода);
• Си — металл, находящийся в ряду активности после водорода, — не реагирует;
• SOз — кислотный оксид — не реагирует;
• Zn — металл, находящийся в ряду активности до водорода, — реагирует (получается соль и водород).
2. Чтобы составить уравнения реакций, определим валентность метал-лов (натрий — I, цинк — II) и составим формулы солей учитывая, что валентность кислотного остатка Сl составляет I. Осталось записать уравнения реакций:
Na2О + 2НСl = 2NaCl + Н2О;
Zn + 2НСl= ZnCl2 + H2.
• Na2О — основный оксид — реагирует (получается соль и вода);
• Си — металл, находящийся в ряду активности после водорода, — не реагирует;
• SOз — кислотный оксид — не реагирует;
• Zn — металл, находящийся в ряду активности до водорода, — реагирует (получается соль и водород).
2. Чтобы составить уравнения реакций, определим валентность метал-лов (натрий — I, цинк — II) и составим формулы солей учитывая, что валентность кислотного остатка Сl составляет I. Осталось записать уравнения реакций:
Na2О + 2НСl = 2NaCl + Н2О;
Zn + 2НСl= ZnCl2 + H2.