химия пәнінің мұғалімі
Жұмақай Гүлмира Серікқызы
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Сабақ Кальций және оның қосылыстары
Содержание
- 1. Сабақ Кальций және оның қосылыстары
- 2. Сабақтың тақырыбы: «Кальций дің периодтық жүйедегі орны, атом құрылысы, қасиеттері» (9 сынып)
- 3. Сабақтың мақсаты:Оқушыларға кальций металының периодтық жүйедегі орны
- 4. Көрнекілігі:Д.И.Менделеевтің периодтық системасы,интерактивті тақта,карточкалар, тест, суреттер ,спирт
- 5. Барысы:Ұйымдастыру кезеңінде әр түрлі түстер бойынша сыныпты
- 6. І топқа таңдау тестісі беріледі.1.Сілтілік жер металдары
- 7. ІІ топқа еске түсіру тестісі-сөзтуымды пайдалануға болады.1.Металдардың
- 8. ІІІ топқа реттік тест беріледі.Металл қосылыстарына байланысты
- 9. «Мағынаны тану» кезеңінде интерактивті тақтаны пайдаланып,слайдтар арқылы
- 10. Слайд 10
- 11. Табиғатта таралуы.Табиғи қосылыстары:ғаныш CaSO4*2H2O,бор ,кальцитCaCO3,доломит CaCO3*MgCO3,фосфорит Ca3(PO4)2,апатит
- 12. СаСаСО3кальцитСаF2флюоритСаSО4 · 2Н2ОғанышСа3(РО4)2фосфорит,апатитТабиғатта таралуыдоломит CaCO3 · MgCO3, фторапатит Ca5(PO4)3F,
- 13. Алынуы:кальцийдің СаСІ2 балқымасын электролиздеп алады.CaCI2↔Ca2+ +2CI-K(-)Ca2+ +2e→Ca0 тотықсыздануA(+)2CI- -2e-→CI2↑тотығуCaCI2эл.тоғы→Ca+CI2↑
- 14. Физикалық қасиеттері.Кальций –күміс түстес ,ақ,жеңіл металл.Оның тығыздығы
- 15. Химиялық қасиеттері.Химиялық белсенділігі бойынша кальций сілтілік металдардан
- 16. Слайд 16
- 17. Есептер шығару
- 18. Толғаныс.1.Кальцийдің физикалық қасиеттеріА) түссіз, жеңіл металл; Ә)
Сабақтың тақырыбы: «Кальций дің периодтық жүйедегі орны, атом құрылысы, қасиеттері» (9 сынып)
Слайд 2Сабақтың тақырыбы:
«Кальций дің периодтық жүйедегі орны, атом құрылысы, қасиеттері»
(9 сынып)
Слайд 3Сабақтың мақсаты:Оқушыларға кальций металының периодтық жүйедегі орны ,физикалық және химиялық қасиеттері,
табиғатта таралуы,алынуы және қолданылуы жөніндегі түсінік беру;
сабаққа белсенділіктерін арттыру;
өз бетімен жұмыс істеу дағдыларын қалыптастыру;
қосымша материалдарды пайдалануға дағдыландыру.
Әдісі: топқа бөлу, дәріс, зертханалық жұмыс,сұрақ-жауап,интерактивті тақтамен жұмыс.
сабаққа белсенділіктерін арттыру;
өз бетімен жұмыс істеу дағдыларын қалыптастыру;
қосымша материалдарды пайдалануға дағдыландыру.
Әдісі: топқа бөлу, дәріс, зертханалық жұмыс,сұрақ-жауап,интерактивті тақтамен жұмыс.
Слайд 4Көрнекілігі:Д.И.Менделеевтің периодтық системасы,интерактивті тақта,карточкалар, тест, суреттер ,спирт шам, кәрлен табақша,стакан, индикаторлар,ұстағыш,
Пәнаралық
байланыс:география-металдың кездесетін жерін,биология-металдың адам ағзасындағы маңызын оқытады.
Слайд 5Барысы:
Ұйымдастыру кезеңінде әр түрлі түстер бойынша сыныпты үш топқа бөлінеді.
«Ой
толғаныс» кезеңі. Бұл бөлімде үй тапсырмасын тексеріп,жаңа сабақпен байланыстырады.
Слайд 6
І топқа таңдау тестісі беріледі.
1.Сілтілік жер металдары сумен әрекеттескенде түзілетін қандай
зат?
А)қышқыл; Ә)Сілті; Б) оксид; В) тұз;
2. Екідайлы оксид .
А) СаО; Ә) АІ2О3; Б) СиО; В) ҒеО;
3.Бордың құрамында қандай элемент бар?
А) Са; Ә) АІ; СІ; К;
А)қышқыл; Ә)Сілті; Б) оксид; В) тұз;
2. Екідайлы оксид .
А) СаО; Ә) АІ2О3; Б) СиО; В) ҒеО;
3.Бордың құрамында қандай элемент бар?
А) Са; Ә) АІ; СІ; К;
Слайд 7ІІ топқа еске түсіру тестісі-сөзтуымды пайдалануға болады.
1.Металдардың жемірілуі;
2.Тіршілікті қолдамайтын элемент;
3.1 грамынан
3км сым созуға болатын металл;
4.Жоғары температурада балқитын элемент;
5.Францияның құрметіне аталған элемент;
6.металдық қасиеті жоғары сілтілік металл;
7.ІІ А тобындағы екідайлы элемент
4.Жоғары температурада балқитын элемент;
5.Францияның құрметіне аталған элемент;
6.металдық қасиеті жоғары сілтілік металл;
7.ІІ А тобындағы екідайлы элемент
Слайд 8
ІІІ топқа реттік тест беріледі.
Металл қосылыстарына байланысты ІІІ период элементтерінің орналасуын
жаз.
А)Са →СаО →СаСО3
Ә)Na →Mg→AI
Б) Na→ Na2O→ NaOH →Na2CO3
А)Са →СаО →СаСО3
Ә)Na →Mg→AI
Б) Na→ Na2O→ NaOH →Na2CO3
Слайд 9«Мағынаны тану» кезеңінде интерактивті тақтаны пайдаланып,слайдтар арқылы жаңа сабақ түсіндіріледі.
Кальций IV
период,ІІ топтың негізгі топшасының элементі,реттік саны 20,ядросында 20протон мен 20 нейтроны бар(Аr=40),электрондарының жалпы саны да 20.Кальцийдің электрондық формуласы 1S2 2S2 2P6 3S2 3P6 4S2,валенттілік электрондары 4S2 болғандықтан кальций қосылыстарында ІІ валентті.
Са тотығу дәрежесі 0,+2,(Са,0 Са+2О-2).
Са тотығу дәрежесі 0,+2,(Са,0 Са+2О-2).
Слайд 11Табиғатта таралуы.Табиғи қосылыстары:ғаныш CaSO4*2H2O,бор ,кальцитCaCO3,доломит CaCO3*MgCO3,фосфорит Ca3(PO4)2,апатит Ca5(PO4)3OH,фторапатит Ca5(PO4)3F,флюорит CaF2.
Қазақстан жерінің
бәрінде дерлік кальций қосылыстары кең таралған. Фосфориттің ең ірі кен орындары Жамбыл облысындағы Қаратау тауларында,Ақтөбе облысында Шилісайда бар. Бағалы қызғылт түсті ұлутас Маңғыстауда,гипс Жамбыл облысында ,цементке қажетті балшық Шымкент ,Семей маңында өндірілсе , әктастың қоры және отқа төзімді балшық еліміздің көптеген облыстарында өндіріледі.Қазақстанның физикалық картасынан кездесетін жерлерін табамыз.
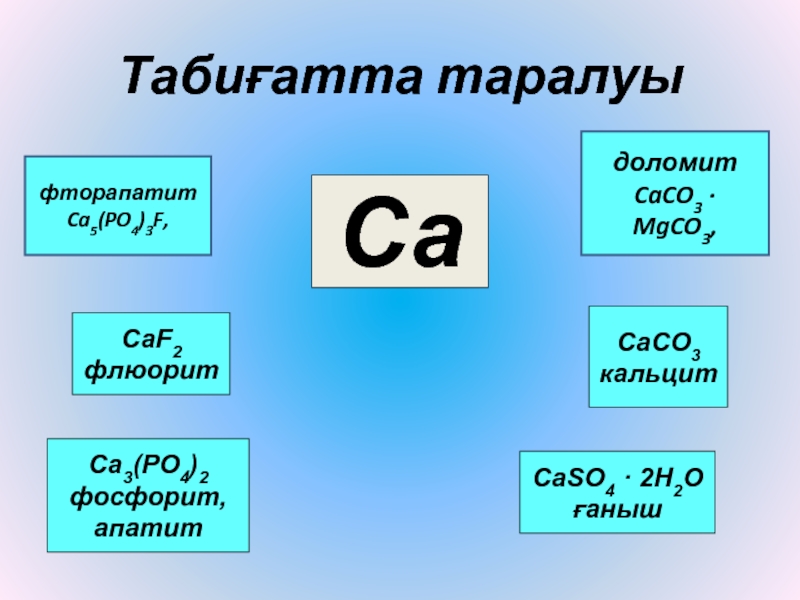
Слайд 12Са
СаСО3
кальцит
СаF2
флюорит
СаSО4 · 2Н2О
ғаныш
Са3(РО4)2
фосфорит,
апатит
Табиғатта таралуы
доломит CaCO3 · MgCO3,
фторапатит Ca5(PO4)3F,
Слайд 13Алынуы:кальцийдің СаСІ2 балқымасын электролиздеп алады.
CaCI2↔Ca2+ +2CI-
K(-)Ca2+ +2e→Ca0 тотықсыздану
A(+)2CI- -2e-→CI2↑тотығу
CaCI2эл.тоғы→Ca+CI2↑
Слайд 14Физикалық қасиеттері.Кальций –күміс түстес ,ақ,жеңіл металл.Оның тығыздығы 1,55 г/см3.Кальций ауамен тез
әрекеттесіп ,тотығу өнімдерінен тұратын кеуектеу жұқа ақ қабықшамен қапталады,сондықтан оны сілтілік металдар сияқты керосин қабатының астында сақтайды.Кальций –қатты металл,оның балқу температурасы 8510С.
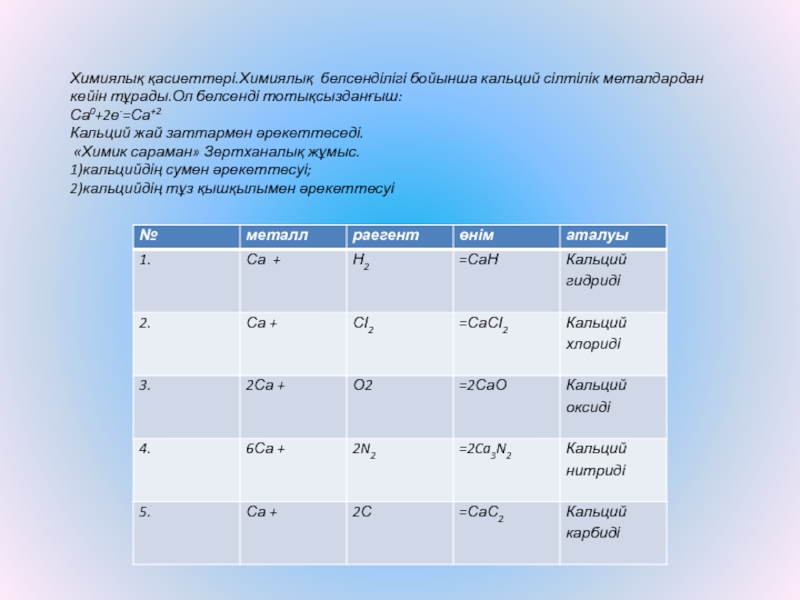
Слайд 15Химиялық қасиеттері.Химиялық белсенділігі бойынша кальций сілтілік металдардан кейін тұрады.Ол белсенді тотықсызданғыш:
Са0+2е-=Са+2
Кальций
жай заттармен әрекеттеседі.
«Химик сараман» Зертханалық жұмыс.
1)кальцийдің сумен әрекеттесуі;
2)кальцийдің тұз қышқылымен әрекеттесуі
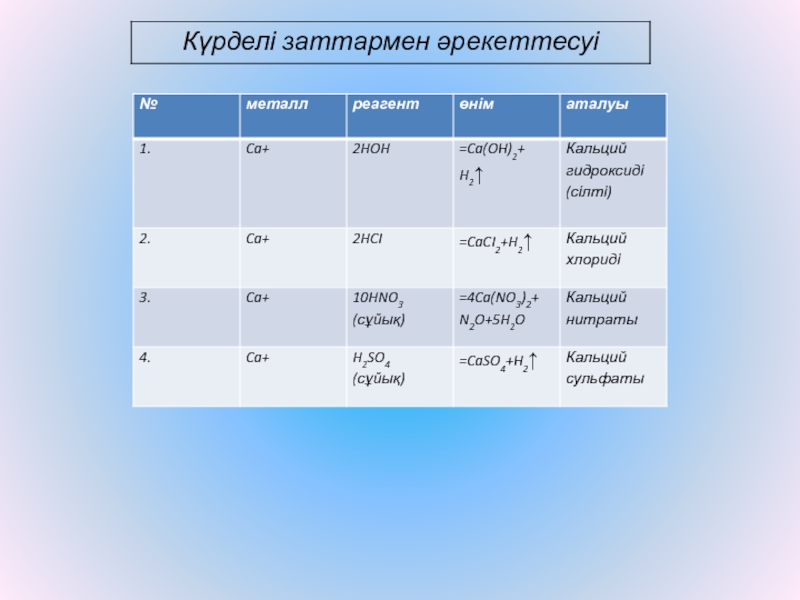
«Химик сараман» Зертханалық жұмыс.
1)кальцийдің сумен әрекеттесуі;
2)кальцийдің тұз қышқылымен әрекеттесуі
Слайд 18Толғаныс.
1.Кальцийдің физикалық қасиеттері
А) түссіз, жеңіл металл; Ә) ақ түсті, қатты металл;
Б)
түсі қызыл, жеңіл металл;
В) түсі ақ, жеңіл металл;
2.Кальцийдің сумен әрекеттесуі кезіндегі барлық коффициенттердің қосындысы нешеге тең?
А)5; Ә) 6; Б) 4; В) 7;
3.Өндірісте қальцийді қандай әдіспен аламыз?
А)кальций қосылыстарын сутекпен тотықсыздандырып;
Ә)кальций қосылыстарын иіс газымен тотықсыздандырып;
Б)кальций қосылыстарын алюминиймен тотықсыздандырып;
В)тұздардың балқымасын электролиздеп;
4. Сөндірілген ізбестің формуласын кқрсетіңдер.
А)СaCO3 ;Ә)Ca(OH)2 ;Б)CaO;)Ca(HCO3)2 ;
5.кальций карбонатының ерітіндісін артық мөлшерде көмір қышқыл газын өткізгенде түзілетін зат.
А)Сa;Ә)Ca(OH)2 ;Б)CaO;)Ca(HCO3)2 ;
В) түсі ақ, жеңіл металл;
2.Кальцийдің сумен әрекеттесуі кезіндегі барлық коффициенттердің қосындысы нешеге тең?
А)5; Ә) 6; Б) 4; В) 7;
3.Өндірісте қальцийді қандай әдіспен аламыз?
А)кальций қосылыстарын сутекпен тотықсыздандырып;
Ә)кальций қосылыстарын иіс газымен тотықсыздандырып;
Б)кальций қосылыстарын алюминиймен тотықсыздандырып;
В)тұздардың балқымасын электролиздеп;
4. Сөндірілген ізбестің формуласын кқрсетіңдер.
А)СaCO3 ;Ә)Ca(OH)2 ;Б)CaO;)Ca(HCO3)2 ;
5.кальций карбонатының ерітіндісін артық мөлшерде көмір қышқыл газын өткізгенде түзілетін зат.
А)Сa;Ә)Ca(OH)2 ;Б)CaO;)Ca(HCO3)2 ;