Автор: Кузькина О.В. МОУ «Коменская СОШ»
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Решение задач по химическим уравнениям
Содержание
- 1. Решение задач по химическим уравнениям
- 2. Номинация 1 – «Учебная презентация по теме (8 класс)».
- 3. Урок химии 8 класс УМК О.С.Габриелян Тема: Химические уравненияАвтор: Кузькина О.В. МОУ «Коменская СОШ»
- 4. Содержание урока:Правила расстановки коэффициентовХимические уравненияЗадания для проверки знаний
- 5. Закон сохранения массы веществ:.Масса веществ, вступающих в
- 6. В левой части уравнения пишут формулы веществ,
- 7. Составление химических уравнений:Н2 + O2 → Н2OСначала
- 8. Правила расстановки коэффициентов в уравнении химических реакций:Подбор
- 9. Правила расстановки коэффициентов в уравнении химических реакций:Подбор
- 10. Правила расстановки коэффициентов в уравнении химических реакций:Подбор
- 11. Правила расстановки коэффициентов в уравнении химических реакций:Подбор
- 12. История химических уравнений:
- 13. Кто впервые сформулировал закон сохранения массы веществ? А.ЛавуазьеПроверка знаний:Д.И.МенделеевМ.В.Ломоносов
- 14. Коэффициенты перед продуктом реакции в уравнении Р + О2 = Р2О5 254
- 15. Сумма коэффициентов в уравнении: фосфорная кислота
- 16. www.themegallery.comСпасибо за внимание!Домашнее задание: §28 вопрос 4
- 17. Список источников:1. О.С.Габриелян Учебник Химия 8 класс – М.:Дрофа, 2017 – 287 стр.2.https://ru.wikipedia.org
Слайд 1Автор: Кузькина Олеся Викторовна, учитель химии МОУ «Коменская СОШ» Прибайкальского района Республики
Слайд 3Урок химии 8 класс УМК О.С.Габриелян
Тема: Химические уравнения
Автор: Кузькина О.В. МОУ
Слайд 4Содержание урока:
Правила расстановки коэффициентов
Химические уравнения
Задания для проверки знаний
Слайд 5Закон сохранения массы веществ:
.
Масса веществ, вступающих в химическую
реакцию, равна массе веществ,
образующихся в результате реакции.
Открыт в 1748 году М.В.Ломоносовым
Экспериментально подствержден А.Лавуазье
На основании
этого закона
пишут химичес-
кие предложе-
ния – химичес-
кие уравнения.
Экспериментальная проверка закона сохранения массы веществ:
а — взвешивание колбы с фосфором до реакции; б — горение фосфора в закрытой колбе; в — взвешивание колбы с продуктом реакции
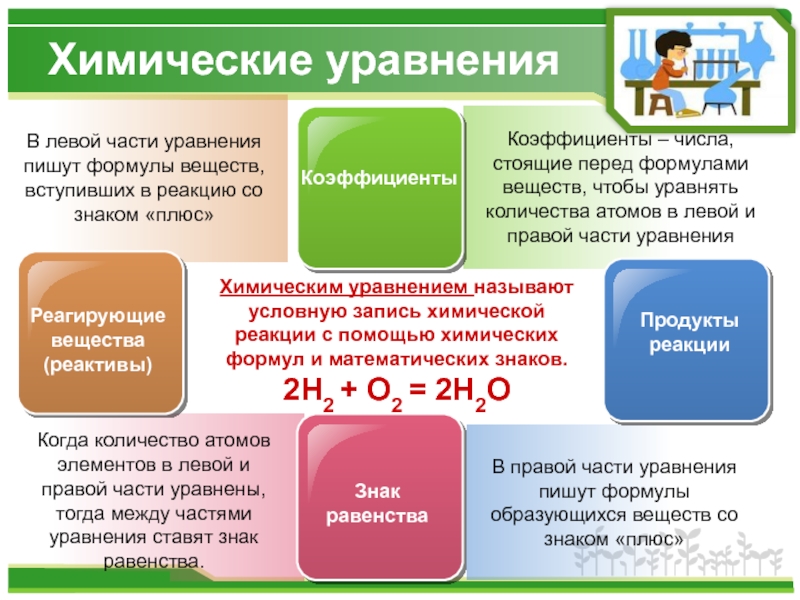
Слайд 6В левой части уравнения пишут формулы веществ, вступивших в реакцию со
Когда количество атомов элементов в левой и правой части уравнены, тогда между частями уравнения ставят знак равенства.
Коэффициенты – числа, стоящие перед формулами веществ, чтобы уравнять количества атомов в левой и правой части уравнения
В правой части уравнения пишут формулы образующихся веществ со знаком «плюс»
Коэффициенты
Знак равенства
Продукты реакции
Реагирующие вещества
(реактивы)
Химическим уравнением называют условную запись химической реакции с помощью химических формул и математических знаков.
2H2 + O2 = 2H2O
Химические уравнения
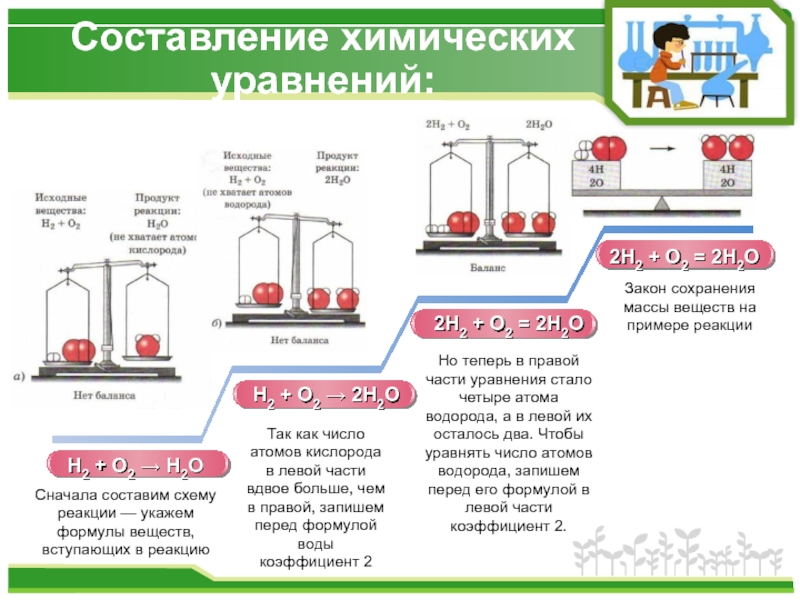
Слайд 7Составление химических уравнений:
Н2 + O2 → Н2O
Сначала составим схему реакции —
Так как число атомов кислорода в левой части вдвое больше, чем в правой, запишем перед формулой воды коэффициент 2
Но теперь в правой части уравнения стало четыре атома водорода, а в левой их осталось два. Чтобы уравнять число атомов водорода, запишем перед его формулой в левой части коэффициент 2.
Закон сохранения массы веществ на примере реакции
Н2 + O2 → 2Н2O
2Н2 + O2 = 2Н2O
2Н2 + O2 = 2Н2O
Слайд 8Правила расстановки коэффициентов в уравнении химических реакций:
Подбор
коэффициентов
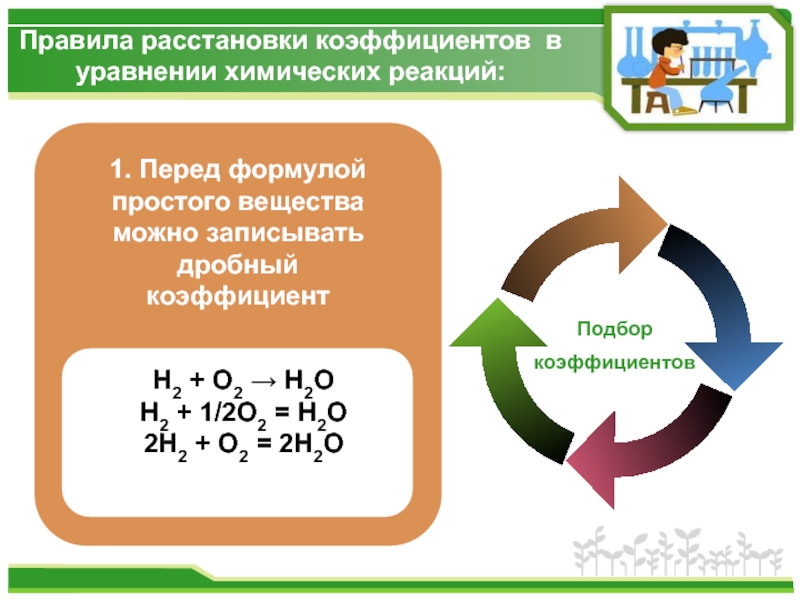
Н2 + O2 →
H2 + 1/2O2 = H2O
2Н2 + O2 = 2Н2O
1. Перед формулой простого вещества можно записывать дробный коэффициент
Слайд 9Правила расстановки коэффициентов в уравнении химических реакций:
Подбор
коэффициентов
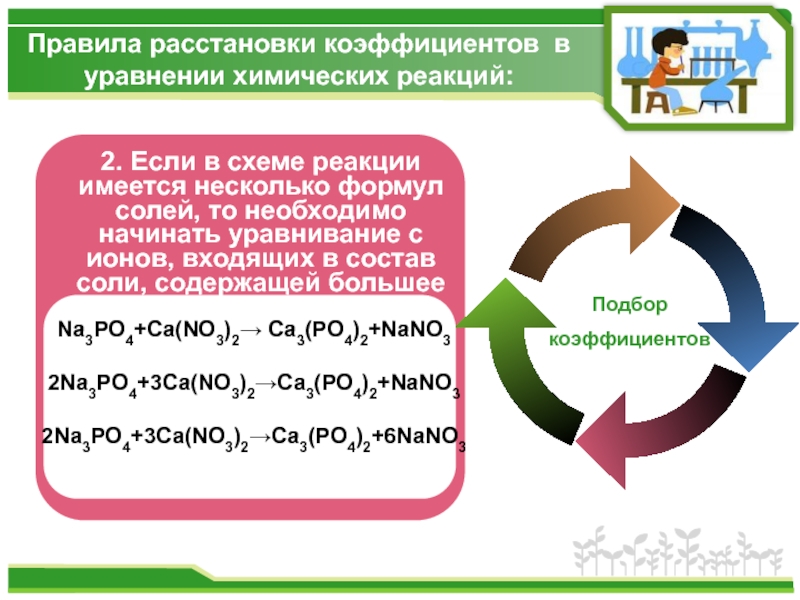
2. Если в схеме
Na3PO4+Ca(NO3)2→ Ca3(PO4)2+NaNO3
2Na3PO4+3Ca(NO3)2→Ca3(PO4)2+NaNO3
2Na3PO4+3Ca(NO3)2→Ca3(PO4)2+6NaNO3
Слайд 10Правила расстановки коэффициентов в уравнении химических реакций:
Подбор
коэффициентов
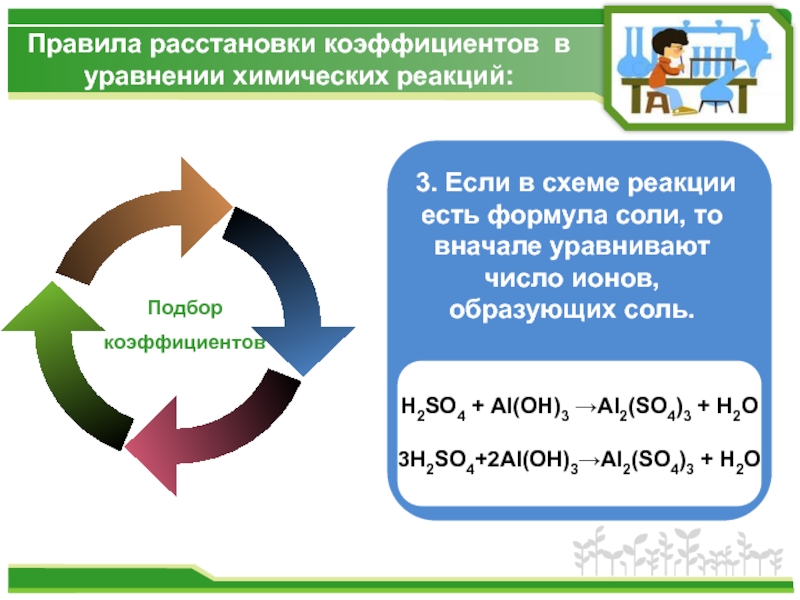
H2SO4 + Аl(OН)3 →Al2(SO4)3
3H2SO4+2Аl(OН)3→Al2(SO4)3 + Н2O
3. Если в схеме реакции есть формула соли, то вначале уравнивают число ионов, образующих соль.
Слайд 11Правила расстановки коэффициентов в уравнении химических реакций:
Подбор
коэффициентов
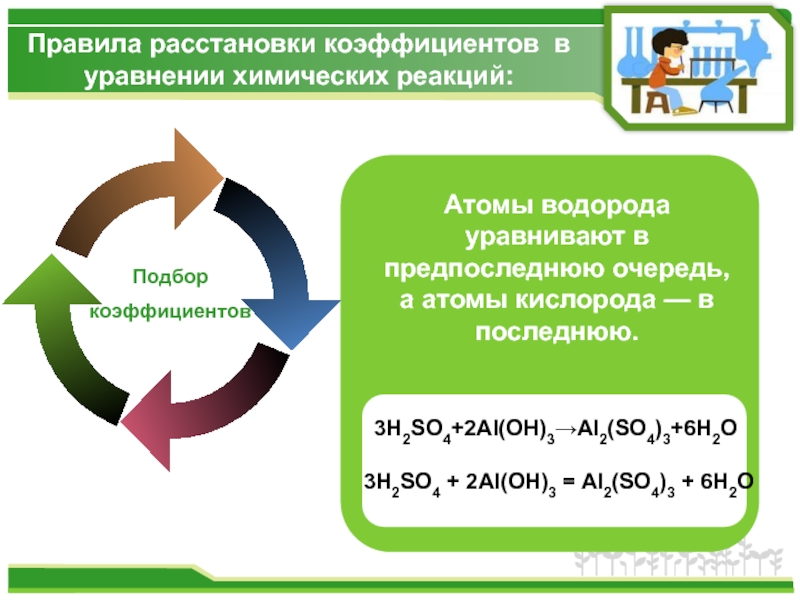
Атомы водорода уравнивают в
3H2SO4+2Аl(OН)3→Al2(SO4)3+6Н2O
3H2SO4 + 2Аl(OН)3 = Al2(SO4)3 + 6Н2O
Слайд 12История химических уравнений:
Первым предложил использовать химические
Иеремия Беньямин Рихтер
Конец XVIII—начало XIX вв. — становление законов стехиометрии. У истоков этих исследований стоял немецкий ученый И. В. Рихтер. Он посвятил свою диссертацию использованию математики в химии. Не будучи в сущности химиком, Рихтер ввел первые количественные уравнения химических реакций, стал использовать термин стехиометрия.
Слайд 13
Кто впервые сформулировал закон сохранения массы веществ?
А.Лавуазье
Проверка знаний:
Д.И.Менделеев
М.В.Ломоносов
Слайд 15 Сумма коэффициентов в уравнении: фосфорная кислота + гидроксид натрия = фосфат
2
Проверка знаний:
8
6
Слайд 17Список источников:
1. О.С.Габриелян Учебник Химия 8 класс – М.:Дрофа, 2017 –
2.https://ru.wikipedia.org