- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Научно-исследовательская работа: ИЗУЧЕНИЕ ЯВЛЕНИЯ ГИДРОЛИЗА
Содержание
- 1. Научно-исследовательская работа: ИЗУЧЕНИЕ ЯВЛЕНИЯ ГИДРОЛИЗА
- 2. АктуальностьОдно из основных химических понятийТема ЕГЭНедостаточное освещение
- 3. Задачи работы:1) Изучить теоретические основы гидролиза органических
- 4. ГидролизОрганических веществ происходит в присутствии катализаторов (ферментов),
- 5. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬОбъектом исследования является процесс гидролиза органических
- 6. Методика проведения экспериментовОпыт 1 Исследование различных случаев
- 7. Методика проведения экспериментовОпыт 4 Влияние температуры на
- 8. Методика проведения экспериментовОпыт 5 Гидролиз крахмала под
- 9. Результаты экспериментов В реакцию гидролиза вступают соли,
- 10. Чем больше заряд иона и меньше радиус
- 11. Гидролиз раствора хлорида олова идёт по первой
- 12. Гидролиз крахмала под влиянием амилазы слюны Крахмал
- 13. ВыводыВ широком смысле слова гидролиз – это
Слайд 1Тема: ИЗУЧЕНИЕ ЯВЛЕНИЯ ГИДРОЛИЗА
.
Работу выполнила:
Ибраимова Эльвина,ученица 9-Б класса ,
МБОУ «Гимназия №5
Научный руководитель:
Квитко Оксана Фёдоровна
учитель биологии и химии
высшей категории
МБОУ «Гимназия №5 г.Феодосии, республики Крым»
Слайд 2Актуальность
Одно из основных химических понятий
Тема ЕГЭ
Недостаточное освещение в школьных учебниках
Тесная связь
Процессы в природе
Деятельность человека
Особенность
комплексный подход при рассмотрении химического процесса, что позволяет сформировать целостное представление о явлении гидролиза.
Слайд 3Задачи работы:
1) Изучить теоретические основы гидролиза органических и неорганических веществ;
2) Провести
3) Выявить факторы, влияющие на осуществление гидролиза;
4) Выяснить практическое применение гидролиза в жизни человека.
Цель работы – изучение явления гидролиза неорганических и органических веществ, а также практических следствий этого явления.
Слайд 4Гидролиз
Органических веществ
происходит в присутствии катализаторов (ферментов), которые разрывают химические связи
Неорганических
происходит в водном растворе при полной диссоциации на ионы
Гидролиз (от греч. hydro – вода, lysis – разложение) в широком смысле слова – это реакция обменного разложения между различными веществами и водой. Такое определение охватывает гидролиз, как неорганических веществ, так и органических – жиров, углеводов, белков.
Гидролиз белков – разрушение, приводящее к образованию a- аминокислот.
Жиры - глицерин и жирные кислоты
Сложные углеводы – простые углеводы (крахмал гидролизируется под действием амилазы слюны и образуется глюкоза).
Процесс пищеварения - это, прежде всего гидролиз органических веществ пищи.
Слайд 5ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объектом исследования является процесс гидролиза органических и неорганических веществ.
Предметом исследования
Методы исследования: анкетирование, качественный анализа и биохимический
Правила техники безопасности: при выполнении экспериментальной части работы соблюдались в соответствии с Санитарно-эпидемиологическими правилами и нормативами СанПиН.
Проведённые исследования:
Анкетирование
Различные случаи гидролиза
Влияние силы кислот, образующих соль, на степень ее гидролиза.
Влияние силы основания, образующего соль, на степень гидролиза.
Влияние температуры на гидролиз
Влияние разбавления раствора на степень гидролиза.
Гидролиз крахмала под влиянием амилазы слюны
Слайд 6Методика проведения экспериментов
Опыт 1 Исследование различных случаев гидролиза
сильное основание и сильная
сильное основание и сильная кислота NaCl
Слабое основание и слабая кислота - CH3COONH4
слабое основание и сильная кислота Al2(SO4)3
слабое основание и сильная кислота FeCl3
Индикаторы: универсальные индикаторные бумажки и фенолфталеин
По изменению цвета индикатора определяла показатели рН для каждой соли
Опыт 2 Влияние силы кислот, образующих соль, на степень ее гидролиза
Na2SO3
Na2CO3
образованных анионами разных кислот и одинаковыми катионами
Опыт 3 Влияние силы оснований, образующих соль, на степень ее гидролиза
AlCl3
MgCl2
образованных анионами одинаковых кислот и разными катионами.
По цвету универсального индикатора сделала вывод о степени гидролиза растворов
Слайд 7Методика проведения экспериментов
Опыт 4 Влияние температуры на гидролиз
Раствор ацетата натрия CH3COONa,
Опыт 5 Влияние разбавления раствора на степень гидролиза.
Определила среду раствора хлорида олова SnCl2 универсальным индикатором,
Добавила к раствору 5 мл. дистиллированной воды, зафиксировала наблюдения.
Слайд 8Методика проведения экспериментов
Опыт 5 Гидролиз крахмала под влиянием амилазы слюны
К
Далее при помощи раствора йода определяю наличие крахмала
Слайд 9Результаты экспериментов
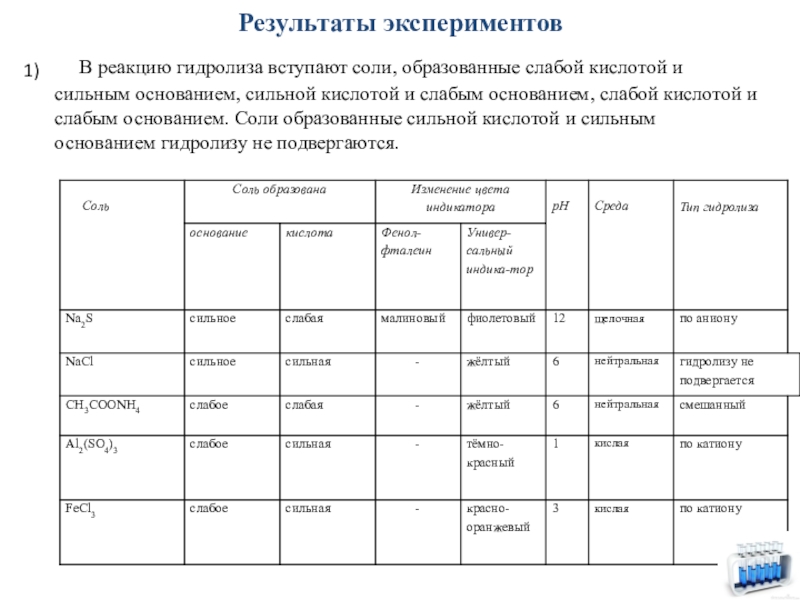
В реакцию гидролиза вступают соли, образованные слабой кислотой и
1)
Слайд 10Чем больше заряд иона и меньше радиус катиона и слабее основание,
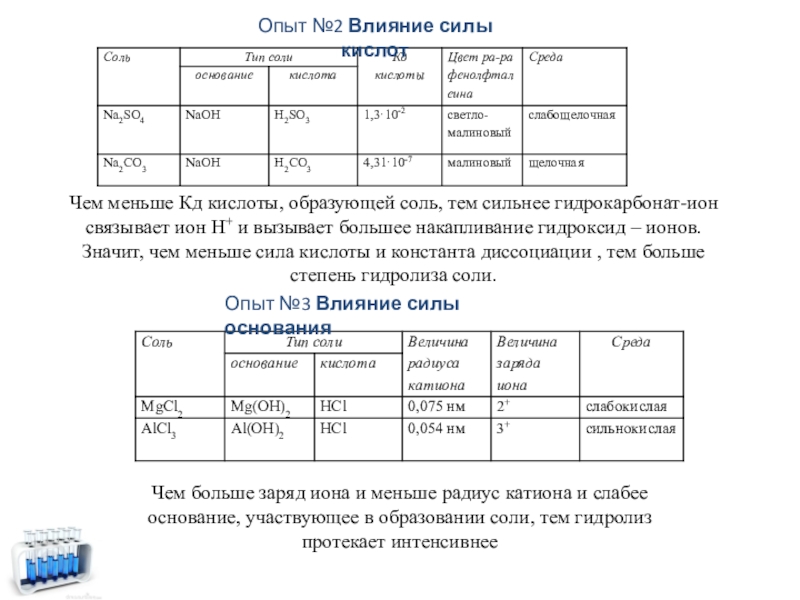
Опыт №2 Влияние силы кислот
Чем меньше Кд кислоты, образующей соль, тем сильнее гидрокарбонат-ион связывает ион H+ и вызывает большее накапливание гидроксид – ионов. Значит, чем меньше сила кислоты и константа диссоциации , тем больше степень гидролиза соли.
Опыт №3 Влияние силы основания
Слайд 11Гидролиз раствора хлорида олова идёт по первой ступени.
При добавлении равного объема
Первая стадия гидролиза
SnCl2 + HOH ⇄ SnOHCl + HCl
Sn2+ + 2Cl- + HOH ⇄ SnOH+ + Cl- + H+ + Cl-
Sn2+ + HOH ⇄ SnOH+ + H+
Вторая стадия гидролиза
SnOHCl + H2O ⇄ Sn(OH)2 + HCl
SnOH+ + Cl- + H2O ⇄ Sn(OH)2 + H+ + Cl-
SnOH+ + H2O ⇄ Sn(OH)2 + H+
При добавлении в раствор ацетата натрия фенолфталеина, раствор продолжал оставаться бесцветным. При нагревании раствора соли наблюдается появление характерной для фенолфталеина в щелочной среде малиновой окраски, которая после охлаждения исчезает.
При повышении температуры степень гидролиза увеличивается, т.к. увеличивается диссоциация воды, что приводит к накоплению в растворе гидроксид - ионов.
Опыт №4 Зависимость степени гидролиза от температуры
Опыт №5 Зависимость степени гидролиза от степени разбавления
Слайд 12Гидролиз крахмала под влиянием амилазы слюны
Крахмал является химически инертным веществом. Для
Схема процесс расщепления крахмала:
крахмал → растворимый крахмал (амилоза) → олигосахариды
(декстрины) → дисахарид (мальтоза = солод) → глюкоза.
Уравнение:
(C6H10O5)n + nH2O +(кат.- фермент) = nC6H12O6
проведена качественная реакция раствора щелочи и сульфат меди (II). Доказывая, что получившийся продукт – глюкоза, проводим качественную реакцию, добавив к полученному раствору щелочь и сульфат меди (II)(CuSO4). Раствор приобретает
ярко-синюю окраску.
Слайд 13Выводы
В широком смысле слова гидролиз – это реакция обменного разложения между
Гидролиз является одним из самых важных процессов в природе.
Реакции, происходящие во время гидролизного процесса, широко используются в современных производственных процессах.
Гидролизу подвержены соединения различных классов. Наиболее изучен гидролиз неорганических солей. В реакцию гидролиза вступают соли, образованные слабой кислотой и сильным основанием, сильной кислотой и слабым основанием, слабой кислотой и слабым основанием. Соли образованные сильной кислотой и сильным основанием гидролизу не подвергаются.
На степень гидролиза влияет природа соли : чем меньше сила кислоты т.е. Константа диссоциации, тем больше степень гидролиза соли, чем слабее основание, участвующее в образовании соли, тем гидролиз протекает интенсивнее
На степень гидролиза влияет увеличение температуры: при повышении температуры степень гидролиза увеличивается, т.к. увеличивается диссоциация воды, что приводит к накоплению в растворе гидроксид - ионов.
При разбавлении раствора соли растет степень диссоциации и увеличивается степень гидролиза.
Гидролиз органических веществ происходит в присутствии катализаторов (ферментов), которые разрывают химические связи. Освободившиеся валентности используются для присоединения групп Н+ и ОН– из молекул воды. При этом реакция среды не изменяется