ВСЕ МЫ СВЯЗЫВАЕМ С ХИМИЧЕСКОЙ НАУКОЙ ПРОГРЕСС В ПОЗНАНИИ ОКРУЖАЮЩЕГО МИРА. И НЕ МОЖЕТ БЫТЬ В НАШИ ДНИ СПЕЦИАЛИСТА, КОТОРЫЙ МОГ БЫ ОБОЙТИСЬ БЕЗ ЗНАНИЯ ХИМИИ.
Н. Семенов
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Призентация к уроку Серная кислота
Содержание
- 1. Призентация к уроку Серная кислота
- 2. При Петре 1 это вещество привозили в
- 3. Слайд 3
- 4. Серная кислота (история открытия )H2SO4SO3
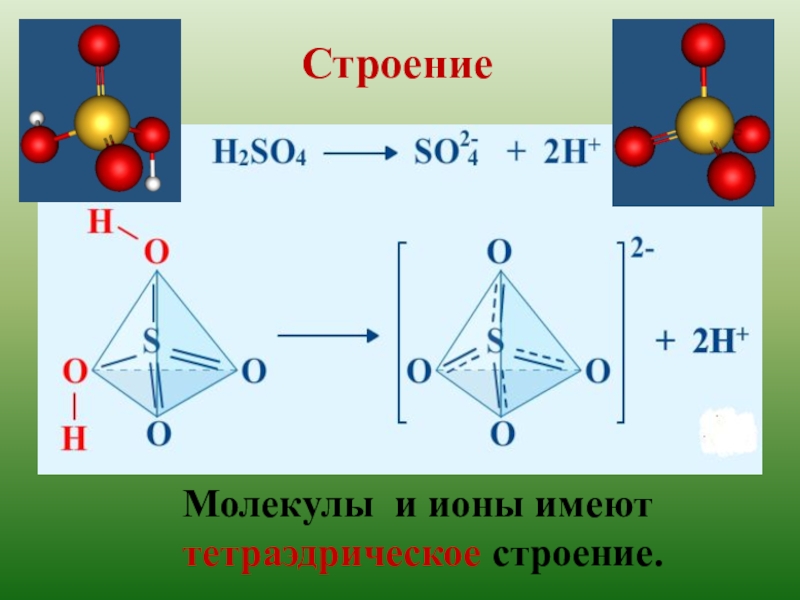
- 5. Строение Молекулы и ионы имеют тетраэдрическое строение.
- 6. Серную кислоту называют хлебом химической промышленности
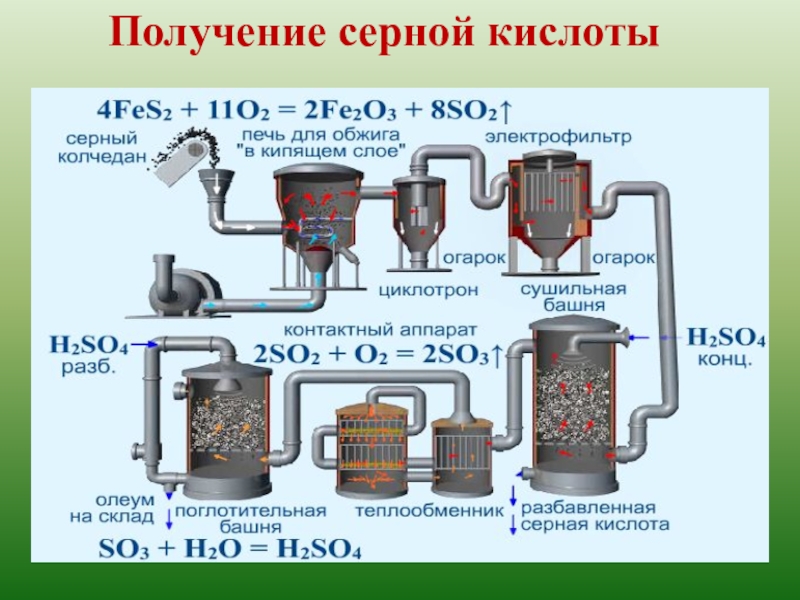
- 7. Получение серной кислотыV2O5H2SSFeS2SO2 → SO3 → H2SO4 ПиритСерный колчедан
- 8. Получение серной кислоты
- 9. Знаете ли вы что:
- 10. Бесцветная маслянистая жидкость =1,83кг/дм3 Большая
- 11. Правило разбавления кислотН2ОСначала вода, потом кислота –
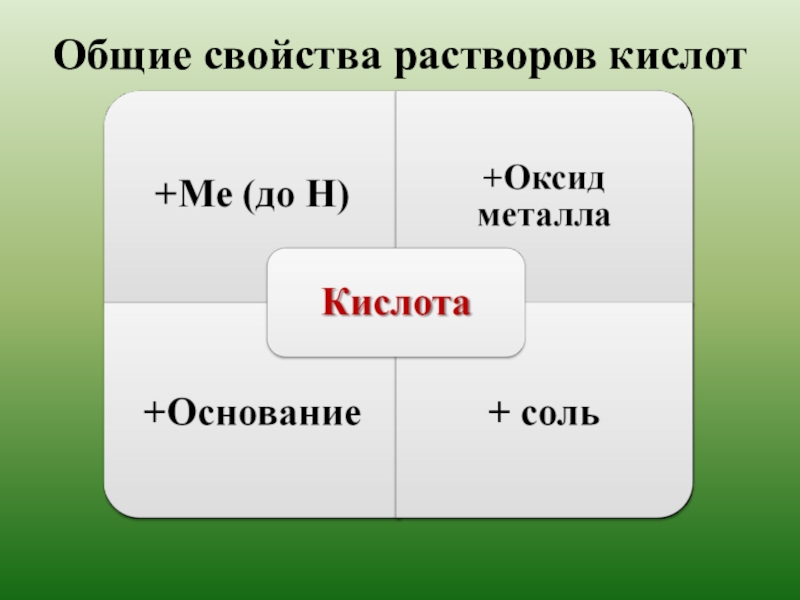
- 12. Общие свойства растворов кислот
- 13. I. Химические свойства разбавленной серной кислоты 1.Диссоциация:
- 14. 2. Взаимодействие с оcновными оксидами
- 15. 3. Взаимодействие с основаниями 2NaOH +
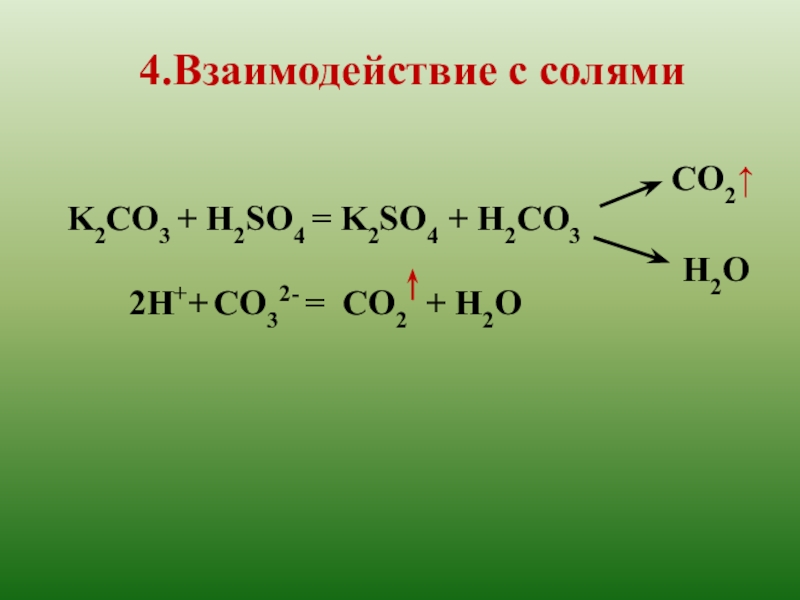
- 16. K2CO3 + H2SO4 = K2SO4
- 17. Качественная реакцияH2SO4+BaCI2 = BaSO4 + 2HCI2H+
- 18. Взаимодействие H2SO4 с металлами
- 19. 2. Взаимодействие с металлами ( до Н
- 20. Окислительные свойства конц. H2SO4 Cu0 +
- 21. Применение серной кислоты
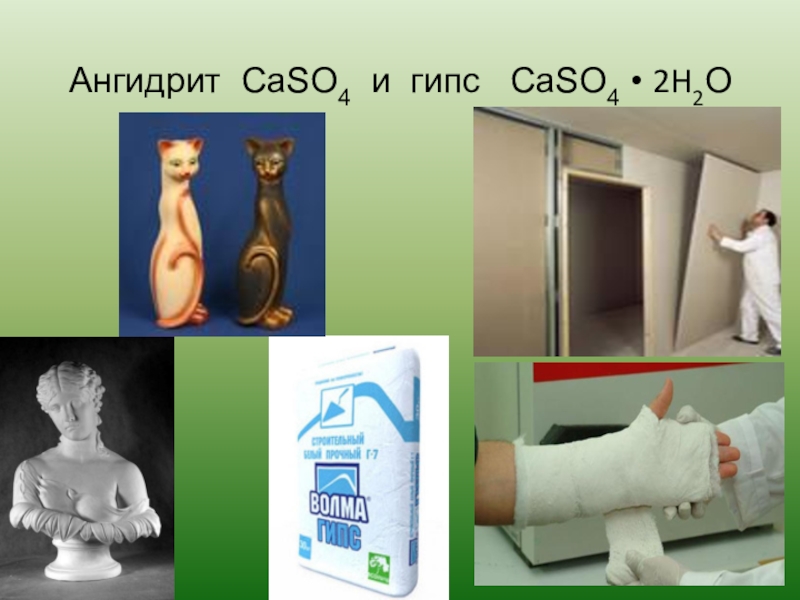
- 22. Ангидрит CaSO4 и гипс CaSO4 • 2H2О
- 23. Архангельская область
- 24. Знаете ли вы что:Месторождение Звозское в Архангельской
- 25. Сульфат меди (II) — CuSO4 · 5H2O — медный купорос
- 26. Глауберова соль — Na2SO4 · 10H2O мирабилит
- 27. ВСЕМ СПАСИБО ЗА ВНИМАНИЕ
- 28. А Ц Б К
- 29. Кислотные дожди
Слайд 1ШИРОКО ПРОСТИРАЕТ ХИМИЯ РУКИ СВОИ В ДЕЛА ЛЮДСКИЕ
Слайд 2При Петре 1 это вещество привозили в Россию из-за границы. Но
«Купоросная кислота», «купоросное масло», «серное масло», «купоросный спирт» -
так называли в 18-19 веке это вещество.
Как вы думаете, какое современное название этого вещества?
Слайд 9Знаете ли вы что:
В одном из
Слайд 10 Бесцветная маслянистая жидкость
=1,83кг/дм3
Большая вязкость
Обладает сильным гигроскопическим
Физические свойства серной кислоты
t кип. = 340ºС
Слайд 11Правило разбавления кислот
Н2О
Сначала вода, потом кислота –
иначе случится большая беда!
«Я
Слайд 13I. Химические свойства разбавленной серной кислоты
1.Диссоциация:
HSO4- ↔ H+ + SO42-
Слайд 153. Взаимодействие с основаниями
2NaOH + H2SO4 → Na2SO4 +2 H2O
H+ + ОН- → H2O
NaOH + H2SO4 → NaHSO4 +H2O
Кислая соль гидросульфат натрия
Демонстрационный опыт
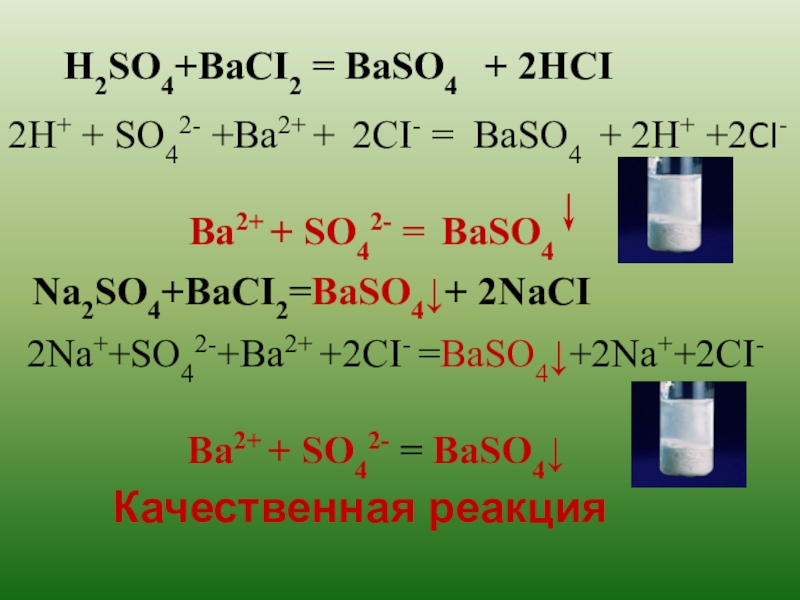
Слайд 17Качественная реакция
H2SO4+BaCI2 = BaSO4 + 2HCI
2H+ + SO42- +Ba2+ +
Ba2+ + SO42- = BaSO4
Na2SO4+BaCI2=BaSO4↓+ 2NaCI
2Na++SO42-+Ba2+ +2CI- =BaSO4↓+2Na++2CI-
Ba2+ + SO42- = BaSO4↓
Слайд 192. Взаимодействие с металлами ( до Н )
Zn + H2SO4
Mg + H2SO4 → MgSO4 + H2↑
Cu + H2SO4 →
Так взаимодействует с металлами разбавленная серная кислота
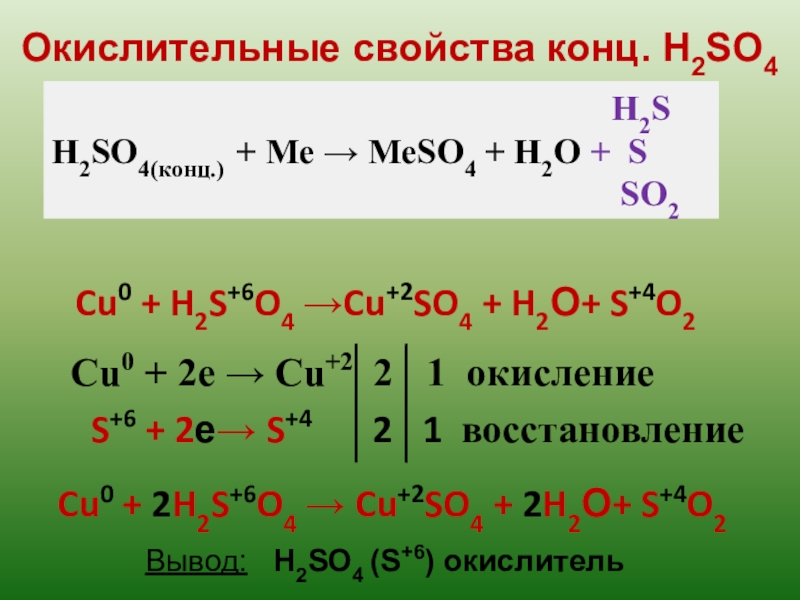
Слайд 20Окислительные свойства конц. H2SO4
Cu0 + H2S+6O4 →Cu+2SO4 + H2О+
H2S
H2SO4(конц.) + Mе → МеSO4 + H2O + S
SO2
Вывод: H2SO4 (S+6) окислитель
Cu0 + 2е → Cu+2 2 1 окисление
S+6 + 2е→ S+4 2 1 восстановление
Cu0 + 2H2S+6O4 → Cu+2SO4 + 2H2О+ S+4O2
Слайд 24Знаете ли вы что:
Месторождение Звозское в Архангельской области – одно из
Высокое качество гипсов предопределило интерес к данному виду сырья со стороны зарубежных компаний.
Первые упоминания о залежах этих пород имеются в «Дневных записках путешествия доктора Академии наук Ивана Лепихина по разным провинциям Российского Государства» в 1771 году