- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Растворение как физико-химический процесс
Содержание
- 1. Презентация Растворение как физико-химический процесс
- 2. Слайд 2
- 3. Слайд 3
- 4. Познакомиться с растворением как физико-химическим процессом 2.
- 5. Где используются растворы? Велика роль растворов в
- 6. Применение растворов в быту и медицине
- 7. Применение растворов в промышленности
- 8. Применение растворов в сельском хозяйстве
- 9. Применение растворов в полиграфии
- 10. Распространение воды в природеВода занимает 3/4
- 11. Какие ассоциации у вас возникают со словом раствор?Раствор
- 12. Ситуативная задача Вы торопитесь в колледж, но
- 13. Является ли чай раствором? Вспомните, что
- 14. Химик-органик Н.Н. Семенов писал: «Химия – это
- 15. Задание 1 Наблюдение влияния природы растворенного вещества
- 16. Растворимость -Способность вещества образовывать с другими веществами
- 17. По растворимости выделяютХорошо растворимые вещества (в 100г
- 18. Задание 2 Наблюдение влияния температуры на растворимость
- 19. Задание 3 Наблюдение влияния природы растворителя на
- 20. Задание 4.Классификация растворов. Использование мобильных телефонов для поиска информации.Сделайте вывод о типах растворов.
- 21. Вода
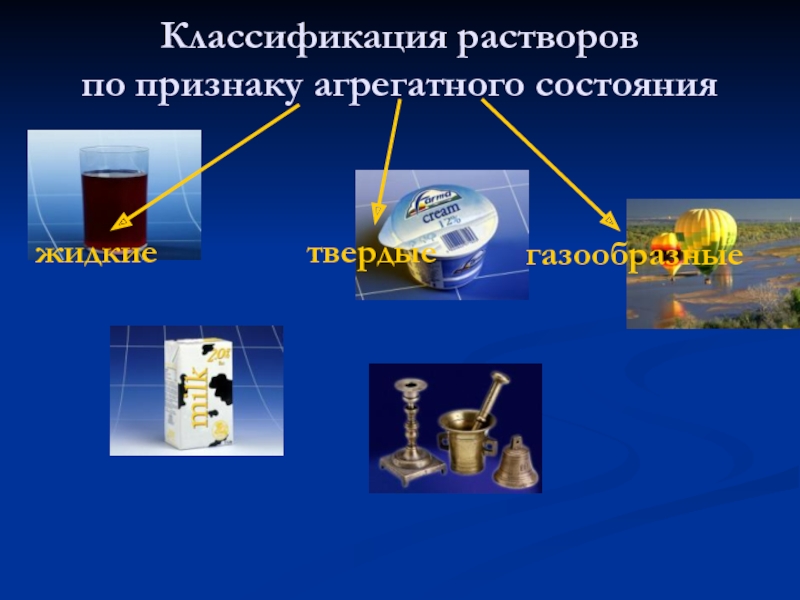
- 22. Классификация растворов по признаку агрегатного состояния
- 23. Растворы и растворениеРАСТВОРЫоднородная устойчивая система, состоящая из
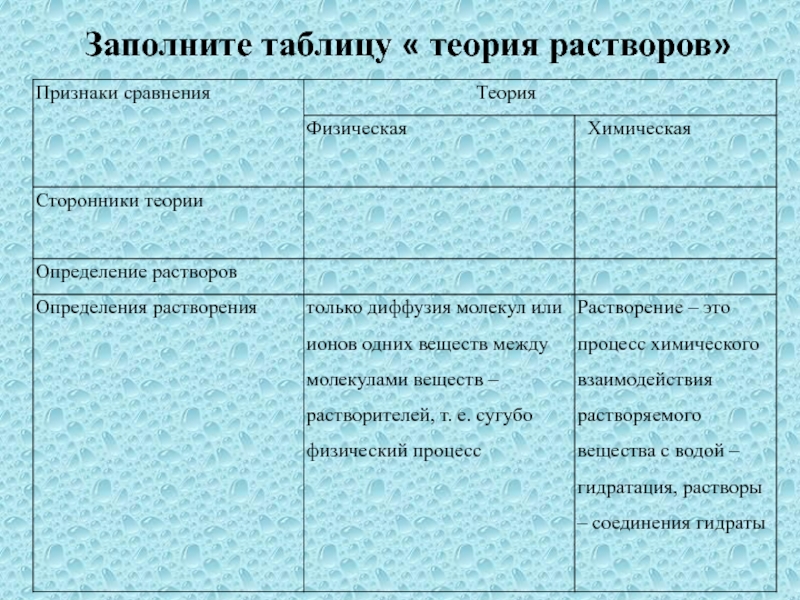
- 24. Физическая теория.Вант-Гофф, Оствальд, Аррениус.Растворение –это процесс диффузии. Растворы – это однородные смеси.Признаки физического процесса: диффузия.
- 25. Признаки химического взаимодействия при растворенииТепловые явления при
- 26. Заполните таблицу « теория растворов»
- 27. 1 теория. Доказать, что растворение – это
- 28. РастворениеФизический процесс –заключающийся в перемешивании молекул растворенного
- 29. Растворение? Современная теория
- 30. Классификация растворов по содержанию растворенного веществаНенасыщенный раствор:
- 31. «Химическая волна»
- 32. 1. Однородность – характерный признак растворов.2.Раствор –
- 33. Слайд 33
- 34. Ответы1. А,Б,Г2. В3. Б4. А5. А6. В
- 35. Домашнее задание § 30, задание 2.
- 36. Рефлексия
- 37. Химический состав крови
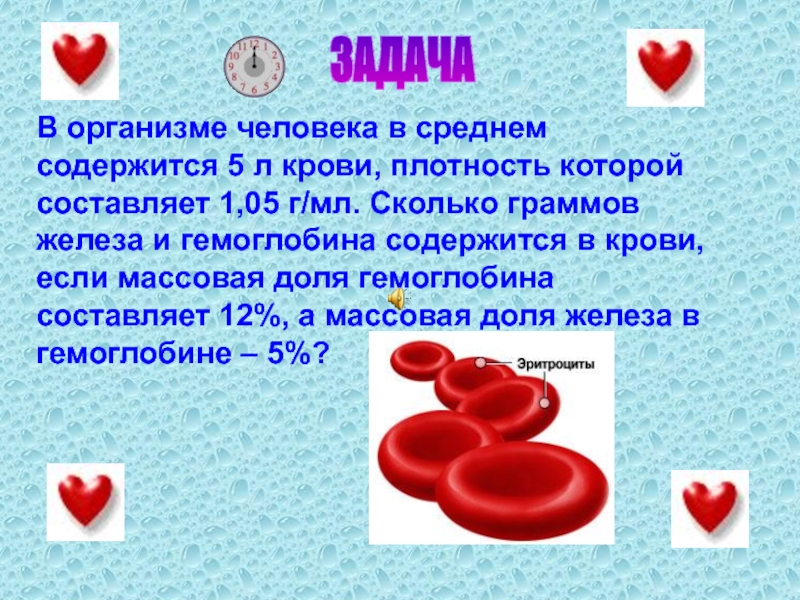
- 38. ЗАДАЧАВ организме человека в среднем содержится 5
- 39. ОТВЕТ: m(гем.) = 630 г
Слайд 4Познакомиться с растворением как физико-химическим процессом
2. Показать зависимость растворимости от
Дать классификацию растворов по содержанию растворенного вещества.
Слайд 5Где используются растворы?
Велика роль растворов в возникновении и развитии жизни
В организме человека находятся физиологически важные растворы. Какие? (кровь, желудочный сок и др.)
Различные процессы, происходящие в организме, протекают в растворах. Например, усвоение пищи связано с переводом питательных веществ в раствор.
В природе водные растворы участвуют в процессах почвообразования и снабжают растения питательными веществами.
В технике такие процессы, как получение соды, удобрений, бумаги, также протекают в растворах.
Слайд 10Распространение воды в природе
Вода занимает 3/4 поверхности Земного шара
В организме
В арбузе воды около 90%
Слайд 12Ситуативная задача Вы торопитесь в колледж, но еще не пили чай. Перед
Слайд 13Является ли чай раствором? Вспомните, что такое раствор? Давайте определим состав
Слайд 14Химик-органик Н.Н. Семенов писал: «Химия – это наука экспериментальная, а не
Слайд 15Задание 1
Наблюдение влияния природы растворенного вещества на процесс растворения.
Порядок выполнения:
В пробирки с веществами прилейте 10мл воды и хорошо встряхните для лучшего растворения вещества.
№1 Хлорид кальция, №2 гидроксид кальция, №3 карбонат кальция
Какое из предложенных веществ хорошо растворяется в воде? Какое не растворяется?
Сделайте вывод о классификации веществ в зависимости от способности веществ растворяться в воде.
Слайд 16Растворимость -
Способность вещества образовывать с другими веществами (растворителями) однородные системы –
- величина, которая показывает максимальную массу растворённого вещества в 100г воды
Слайд 17По растворимости выделяют
Хорошо растворимые вещества (в 100г воды растворяется > 1г
Малорастворимые (в 100г воды растворяется < 1г вещества)
Нерастворимые (в 100г воды растворяется < 0,01г вещества).
Найдите в таблице растворимости хорошо растворимые вещества, малорастворимые и нерастворимые, запишите примеры
Растворимость зависит от…
Слайд 18Задание 2
Наблюдение влияния температуры на растворимость веществ.
Видео опыт: “Влияние температуры
Сделайте вывод о влиянии температуры на растворимость веществ.
Слайд 19Задание 3
Наблюдение влияния природы растворителя на процесс растворения веществ.
Порядок выполнения:
В пробирки с медным купоросом прилейте в 10мл спирта (№1) и 10мл воды (№2), закройте пробкой и хорошо встряхните для лучшего растворения вещества.
Какой из предложенных растворителей хорошо растворяет медный купорос?
Сделайте вывод о влиянии природы растворителя на процесс растворения и способности веществ растворяться в разных растворителях.
Слайд 20Задание 4.
Классификация растворов.
Использование мобильных телефонов для поиска информации.
Сделайте вывод о
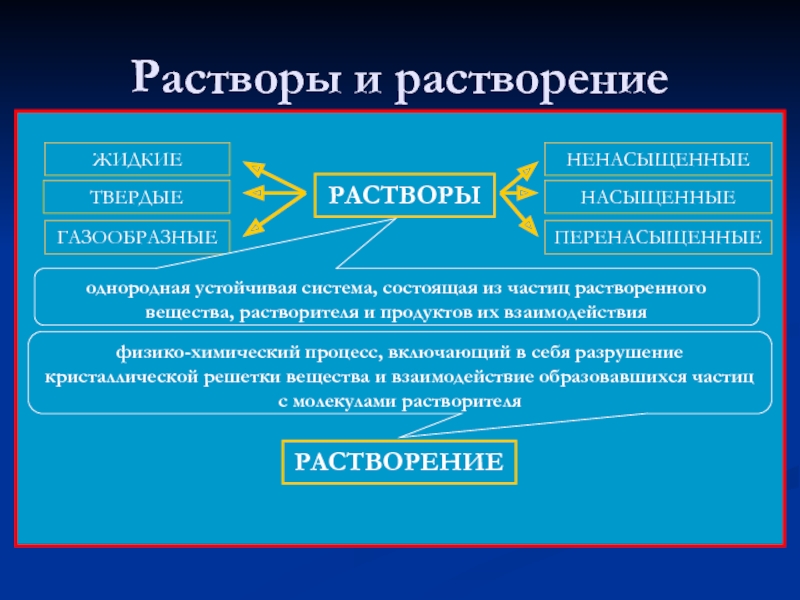
Слайд 23Растворы и растворение
РАСТВОРЫ
однородная устойчивая система, состоящая из частиц растворенного вещества, растворителя
РАСТВОРЕНИЕ
физико-химический процесс, включающий в себя разрушение кристаллической решетки вещества и взаимодействие образовавшихся частиц с молекулами растворителя
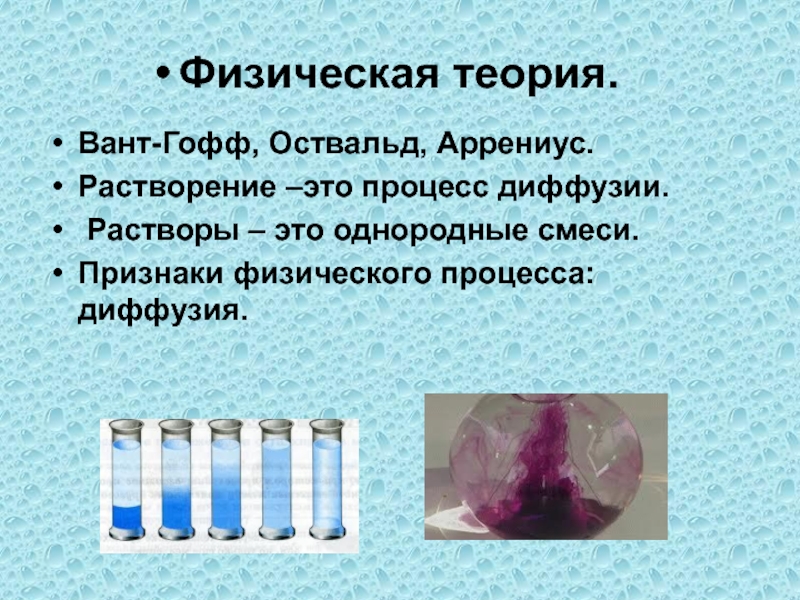
Слайд 24Физическая теория.
Вант-Гофф, Оствальд, Аррениус.
Растворение –это процесс диффузии.
Растворы – это однородные
Признаки физического процесса: диффузия.
Слайд 25Признаки химического взаимодействия при растворении
Тепловые явления при растворении
Изменение окраски:
Химическая теория.
Менделеев, Каблуков,
Растворение – это процесс химического взаимодействия растворяемого вещества с водой – гидратация.
Растворы – продукты взаимодействия вещества с водой –гидраты.
Слайд 271 теория. Доказать, что растворение – это физическое явление, выявить признаки
ОПЫТ: растворение перманганата калия. Возьмем стакан с водой и осторожно опустим на дно кристалл марганцовки.
2 теория. Доказать, что растворение – это химическое явление, выявить признаки химического явления при растворении.
ОПЫТ: в один стакан прибавьте немного серной кислоты, а в другой – кристаллы аммиачной селитры NH4NO3. Поглощается или выделяется тепло?
Слайд 28Растворение
Физический процесс –заключающийся в перемешивании молекул растворенного вещества и растворителя, результат
Химический процесс –заключающийся во взаимодействии молекул растворенного вещества и растворителя и образование гидратов.
Слайд 29Растворение?
Современная теория
Раствор – это однородная устойчивая
– это физико-химический процесс, включающий в себя разрушение кристаллической решетки вещества (диссоциацию) и взаимодействие образовавшихся частиц с молекулами растворителя (сольватацию)
продуктов их взаимодействия
…
Слайд 30Классификация растворов по содержанию растворенного вещества
Ненасыщенный раствор: при данной температуре находится
Насыщенный раствор: при данной температуре вещество больше не растворяется
Пересыщенный раствор: в растворенном состоянии больше вещества, чем его в насыщенном растворе
Слайд 321. Однородность – характерный признак растворов.
2.Раствор – это однородная, гетерогенная система,
3.Между компонентами раствора происходят только физические взаимодействия.
4.При смешивании глины с водой, образуется мутная смесь, которая называется взвесь.
5.Растворимость веществ различна, поэтому их делят на три группы: хорошо растворимые, малорастворимые и практически нерастворимые.
6.В 1 литре воды растворили 1000 грамм сахара, такой раствор называется насыщенным.
7. Растворы, суспензии, эмульсии с течением времени отстаиваются.