- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Электролиз (10 класс)
Содержание
- 1. Презентация по химии на тему Электролиз (10 класс)
- 2. В результате изучения темы, вы будете способны:1.Определять
- 3. Электролиз- это окислительно - восстановительные реакции, протекающие
- 4. Т. е. химическая реакция, протекающая под действием
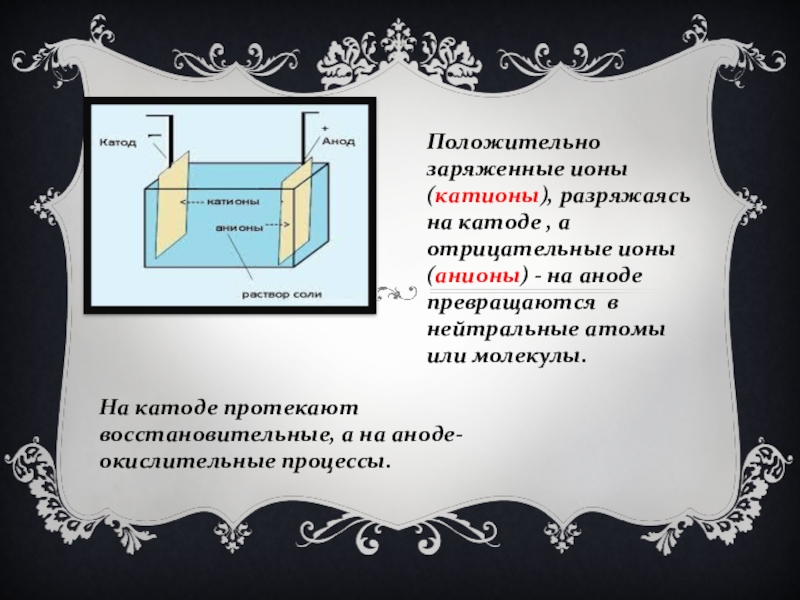
- 5. Положительно заряженные ионы(катионы), разряжаясь на катоде ,
- 6. Сущностью процесса электролиза является получение химических реакций за счёт электролитической энергии.
- 7. Электролиз расплавов солейКатодный процесс: восстановление катиона металлаМеn+ + nе- = Me0 Анодный процесс: окисление кислотного остатка
- 8. ЭЛЕКТРОЛИЗ РАСПЛАВОВПри проведении электролиза электролита в виде
- 9. ЭЛЕКТРОЛИЗ РАСПЛАВОВНа катоде происходит процесс восстановления В
- 10. ЭЛЕКТРОЛИЗ РАСПЛАВОВНа аноде происходит процесс окисления В
- 11. Электролиз расплава NaCl К(-)
- 12. ЭЛЕКТРОЛИЗ РАСПЛАВОВПри проведении электролиза электролита в виде
- 13. ЭЛЕКТРОЛИЗ РАСПЛАВОВЗадание: Составить уравнение электролиза расплава CuCl2CuCl2 K(-):
- 14. ЭЛЕКТРОЛИЗ РАСПЛАВОВЗадание: Составить уравнение электролиза расплава NaOH
- 15. Слайд 15
- 16. ЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ ЭЛЕКТРОЛИТОВ.Надо отличить друг от
- 17. РЯД КАТИОНОВLi,K,Ca,Na,Mg,Al,Mn,Zn,Cr,Fe,Co,Ni,Sn,Pb,H,Cu,Hg,Ag,Pt,Au.Начиная от лития по алюминию включительно
- 18. РЯД АНИОНОВS-2, I-, Br-, C l-, OH-,
- 19. ЭЛЕКТРОЛИЗ РАСТВОРОВВ отличии от расплава в растворе
- 20. Электролиз раствора NaCl
- 21. ЭЛЕКТРОЛИЗ РАСТВОРАЗадание: Составить уравнение электролиза раствора NaCl
- 22. Характер электрохимических процессов, протекающих на электродах при
- 23. I. Химическая промышленность: Получение галогенов, водорода: 2
- 24. ГальванопластикаIII. ГальванотехникаГальваностегияЭлектрополирование,оксидирование металлов
- 25. Гальваностегия –нанесение металлического покрытия на предмет
- 26. КОПИРОВАНИЕ РЕЛЬЕФНЫХ ИЗДЕЛИЙ ИЗ МЕТАЛЛОВ И ДРУГИХ
- 27. Установка для электрохимического покрытия предметов слоем металла
- 28. ЦЕЛЬ ГАЛЬВАНОСТЕГИИ- ПРИДАТЬ ПРЕДМЕТАМ ОПРЕДЕЛЕННЫЕ СВОЙСТВА:повышенную
- 29. Гальванопластика –получения металлических копий с рельефных предметов
- 30. Словолитноегальвано-пластическое стереотипное заведение И. Гольдберга в Санкт-Петербурге. С гравюры на дереве
- 31. Металлическая копия старинного кружева.
- 32. РЕФЛЕКСИЯ 1.На уроке я работал… 2.Своей работой
- 33. Разобрать конспект.Повторить параграф: § Домашнее задание
Слайд 2В результате изучения темы,
вы будете способны:
1.Определять понятие "электролиз", записывать схемы
2.Выводить практическое применение гальванических элементов.
3.Объяснять восстановление катионов металлов на катоде, окисление анионов на аноде при электролизе расплавов солей NaCl, KCl;
4.Объяснять роль воды в катодных процессах при электролизе растворов NaCl, KCl;
5.Осуществлять рефлексию учебной
деятельности
Слайд 3Электролиз- это окислительно - восстановительные реакции, протекающие на электродах, при пропускании
Слайд 4Т. е. химическая реакция, протекающая под действием электрического тока, называется электролизом.
Слайд 5Положительно заряженные ионы(катионы), разряжаясь на катоде , а отрицательные ионы(анионы) -
На катоде протекают восстановительные, а на аноде- окислительные процессы.
Слайд 6Сущностью процесса электролиза является получение химических реакций за счёт электролитической энергии.
Слайд 7Электролиз расплавов солей
Катодный процесс: восстановление катиона металла
Меn+ + nе- = Me0
Анодный процесс:
окисление кислотного остатка
Слайд 8ЭЛЕКТРОЛИЗ РАСПЛАВОВ
При проведении электролиза электролита в виде расплава ,на катоде разряжаются
Слайд 9ЭЛЕКТРОЛИЗ РАСПЛАВОВ
На катоде происходит процесс восстановления
В расплавах катионы металла восстанавливаются до
Мn+ + nē = М0
Слайд 10ЭЛЕКТРОЛИЗ РАСПЛАВОВ
На аноде происходит процесс окисления
В расплавах анионы бескислородных кислот (кроме
2Cl– – 2ē = Cl20
• Кислородсодержащие анионы выделяют кислород и превращаются в один из оксидов:
SO42– – 2ē = SO20 + O20.
4OH- - 4 ē = 2H2O+O2
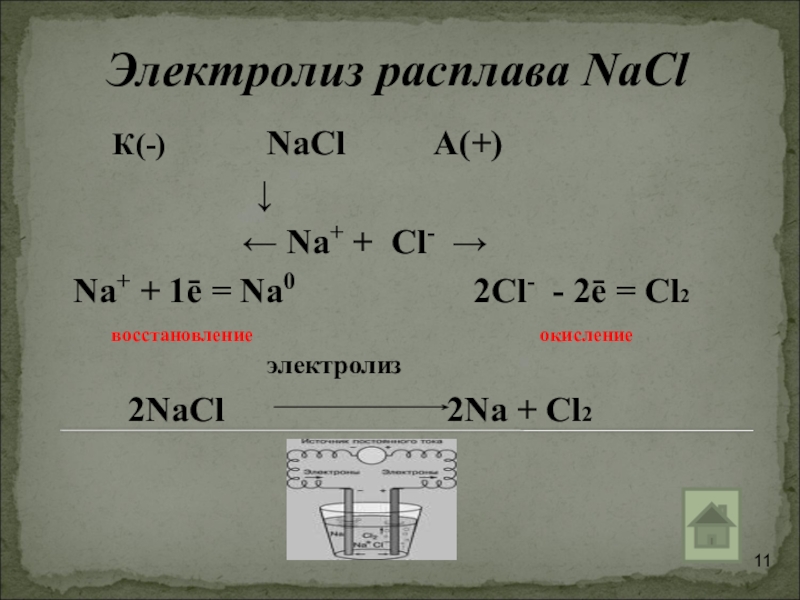
Слайд 11Электролиз расплава NaCl
К(-) NaCl А(+)
← Na+ + Cl- →
Na+ + 1ē = Na0 2Cl- - 2ē = Cl2
электролиз
2NaCl 2Na + Cl2
восстановление
окисление
Слайд 12ЭЛЕКТРОЛИЗ РАСПЛАВОВ
При проведении электролиза электролита в виде расплава ,на катоде разряжаются
Например:
Электролиз расплава хлорида натрия.
NaCl K(-): Na ++ 1 ē → Na0
A(+): 2Cl- - 2 ē → Cl2
2NaCl → 2Na + Cl2
Слайд 13ЭЛЕКТРОЛИЗ РАСПЛАВОВ
Задание: Составить уравнение электролиза расплава CuCl2
CuCl2 K(-): Cu 2++ 2
A(+): 2Cl- - 2 ē → Cl2
CuCl2 → Cu + Cl2
электролиз
Слайд 14ЭЛЕКТРОЛИЗ РАСПЛАВОВ
Задание: Составить уравнение электролиза расплава NaOH
NaOH K(-): Na ++
A(+): 4OH- - 4 ē → 2H2O+O2
4NaOH→ 4Na+ O2↑+2H2O
электролиз
Слайд 16ЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ ЭЛЕКТРОЛИТОВ.
Надо отличить друг от друга электролиз расплава и
Слайд 17РЯД КАТИОНОВ
Li,K,Ca,Na,Mg,Al,Mn,Zn,Cr,Fe,Co,Ni,Sn,Pb,H,Cu,Hg,Ag,Pt,Au.
Начиная от лития по алюминию включительно при электролизе их солей
У металлов расположенных между Al и H при электролизе в водных растворах их солей, на катоде выделяется как металл, так и водород.
В водных растворах солей металлов, стоящие после водорода, на катоде выделяется сам металл
Слайд 18РЯД АНИОНОВ
S-2, I-, Br-, C l-, OH-, SO4-2 и анионы
других
Анионы стоящие до OH- в указанной последовательности окисляясь , превращаются в простые вещества. Анионы стоящие после OH- при электролизе на аноде не окисляются. В этом случае окисляются молекулы воды и выделяется кислород.
Слайд 19ЭЛЕКТРОЛИЗ РАСТВОРОВ
В отличии от расплава в растворе электролита кроме ионов, получившихся
воды, а также ионы H+ и OH-
Например:
Электролиз раствора хлорида натрия.
NaCl K(-): 2H2O + 2e → H2 + 2OH-
A(+): 2Cl- - 2e → Cl20
Итог: 2NaCl + 2H2O → Cl2 + H2 + 2NaOH
Слайд 20Электролиз раствора NaCl
К(-) NaCl А(+)
↓
← Na+ + Cl- →
2Н2О + 2ē = H2 + 2OH- 2Cl- - 2ē = Cl2↑
электролиз
2NaCl + 2H2O H2 + Cl2 +2NaOH
Слайд 21ЭЛЕКТРОЛИЗ РАСТВОРА
Задание: Составить уравнение электролиза раствора NaCl
NaCl K(-): 2Н2О + 2ē
A(+): 2Cl- - 2ē = Cl2↑
2NaCl + 2H2O→ H2↑ + Cl2↑ +2NaOH
электролиз
Слайд 22Характер электрохимических процессов, протекающих на электродах при электролизе в растворах, зависит
Природа иона.
Природа растворителя.
Концентрация электролита.
Материал, из которого изготовлен электрод.
Температура.
Плотность тока.
Слайд 23I. Химическая промышленность:
Получение галогенов, водорода:
2 NaF→ 2 Na
Получение щелочей:
2 NaCL+ 2 H2O →H2 ↑ + CL2 ↑ + 2NaOH
II. Металлургия:
Получение щелочных и щелочноземельных металлов
Получение малоактивных металлов
2CuSO4 + 2H2O → 2 Cu + O2 ↑ + H2SO4
Рафинирование металлов(очистка Ме от примесей)
Применение электролиза
Слайд 26КОПИРОВАНИЕ РЕЛЬЕФНЫХ ИЗДЕЛИЙ ИЗ МЕТАЛЛОВ И ДРУГИХ МАТЕРИАЛОВ. ГАЛЬВАНОПЛАСТИКА ПОЗВОЛЯЕТ СОЗДАВАТЬ
Слайд 28ЦЕЛЬ ГАЛЬВАНОСТЕГИИ-
ПРИДАТЬ ПРЕДМЕТАМ ОПРЕДЕЛЕННЫЕ СВОЙСТВА:
повышенную коррозийную стойкость (цинкование, кадмирование, свинцевание)
износостойкость
защитно-декоративные (покрытие драгоценными металлами)