- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Предельные углеводороды (алканы)
Содержание
- 1. Презентация Предельные углеводороды (алканы)
- 2. АЛКАНЫАлканы = предельные углеводороды = =насыщенные углеводороды = парафины
- 3. Вспомните, какие вещества мы называем углеводородами?УГЛЕВОДОРОДЫ –это
- 4. CnH2n+2Алканы – углеводороды, атомы углерода в которых
- 5. Строение алканов
- 6. Метан Для алканов характерна sp³-гибридизация; Длина С-С
- 7. Строение молекулы метанаCH4 Пространственное строение молекулыметана
- 8. Какое же пространственное строение будут иметь гомологи
- 9. Физические свойстваС увеличением относительных молекулярных масс
- 10. ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ. НАХОЖДЕНИЕ В ПРИРОДЕ.МЕТАН –
- 11. ЭТАН, ПРОПАН И БУТАН входят в состав
- 12. СН4 + Сl2 CH3Cl
- 13. 2. Реакции изомеризации:СН3
- 14. Применение алканов1-3 – производство сажи(1 – картриджи;2
- 15. Составьте все возможные изомеры для гептана и
- 16. Практическая работа “Изготовление моделей молекул органических веществ.
- 17. ДОМАШНЕЕ ЗАДАНИЕ:1. § 9.1, № 1, №
Слайд 1«Не так давно случилась на Кольском полуострове небывалая история. Горный инженер,
Слайд 3Вспомните, какие вещества мы называем углеводородами?
УГЛЕВОДОРОДЫ –
это органические соединения,
состоящие из двух
элементов – УГЛЕРОДА И ВОДОРОДА.
Слайд 4
CnH2n+2
Алканы – углеводороды, атомы углерода в которых соединены простыми связями.
Запишите
СН4 метан
С2H6 этан
C3H8 пропан
C4H10 бутан
C5H12 пентан
C6H14 гексан
C7H16 гептан
C8H18 октан
C9H20 нонан
C10H22 декан
Гомологи – это вещества, сходные по строению и свойствам
и отличающиеся на одну или более групп - СH2
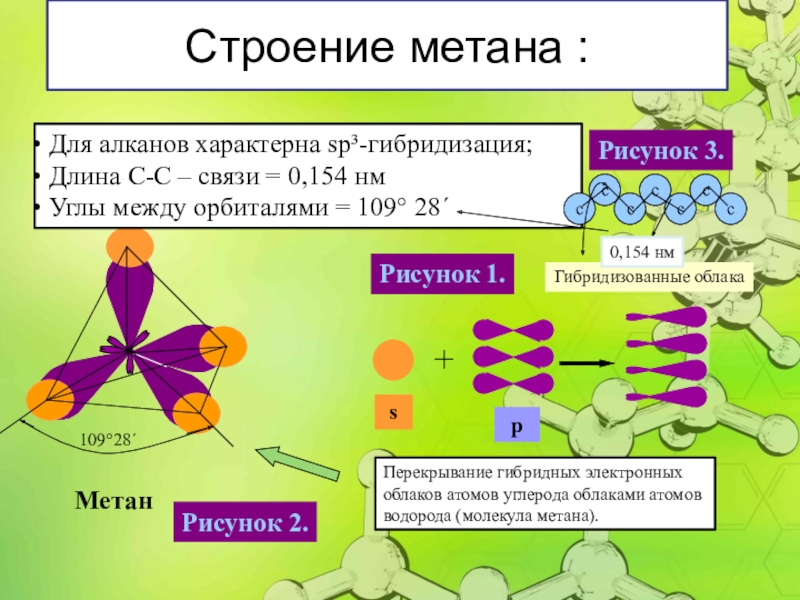
Слайд 6Метан
Для алканов характерна sp³-гибридизация;
Длина С-С – связи = 0,154
Углы между орбиталями = 109° 28´
Перекрывание гибридных электронных
облаков атомов углерода облаками атомов
водорода (молекула метана).
+
109°28´
Строение метана :
s
р
Гибридизованные облака
Рисунок 1.
Рисунок 2.
Рисунок 3.
c
c
c
c
c
c
c
0,154 нм
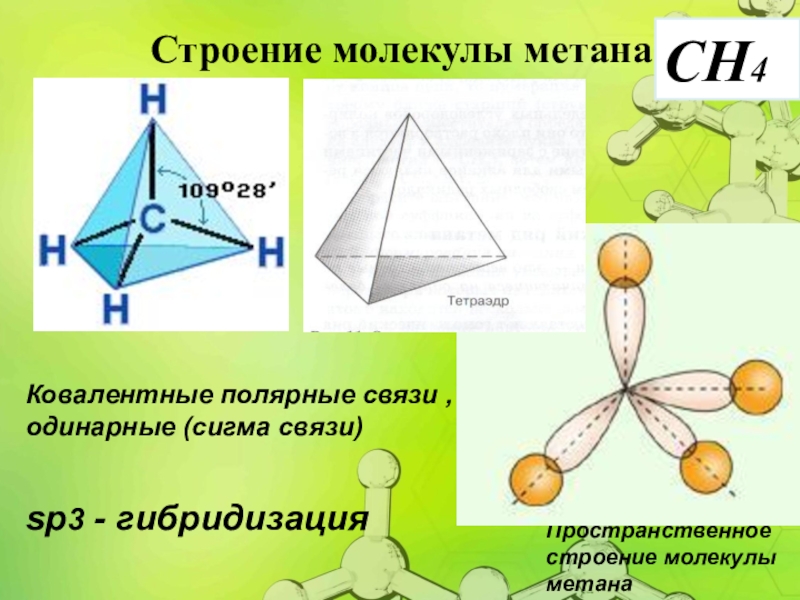
Слайд 7Строение молекулы метана
CH4
Пространственное
строение молекулы
метана
Ковалентные
sp3 - гибридизация
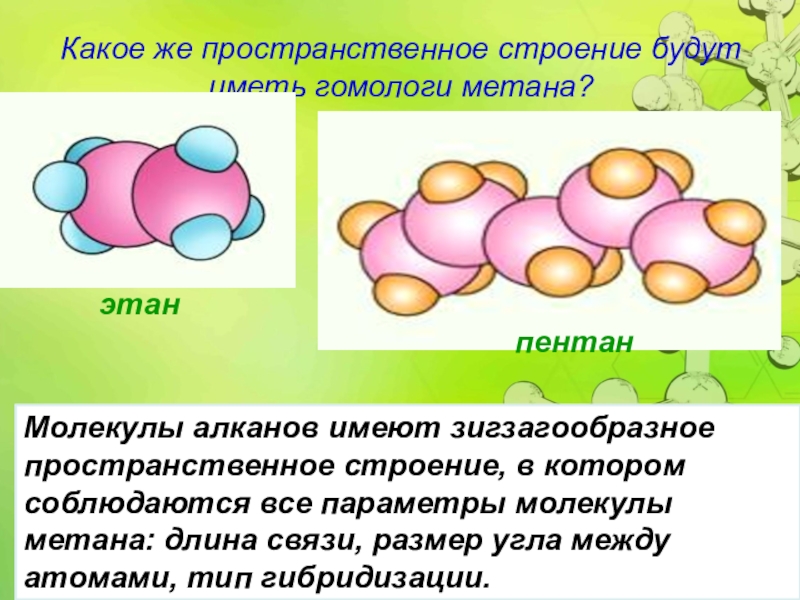
Слайд 8Какое же пространственное строение будут иметь гомологи метана?
этан
пентан
Молекулы алканов имеют зигзагообразное
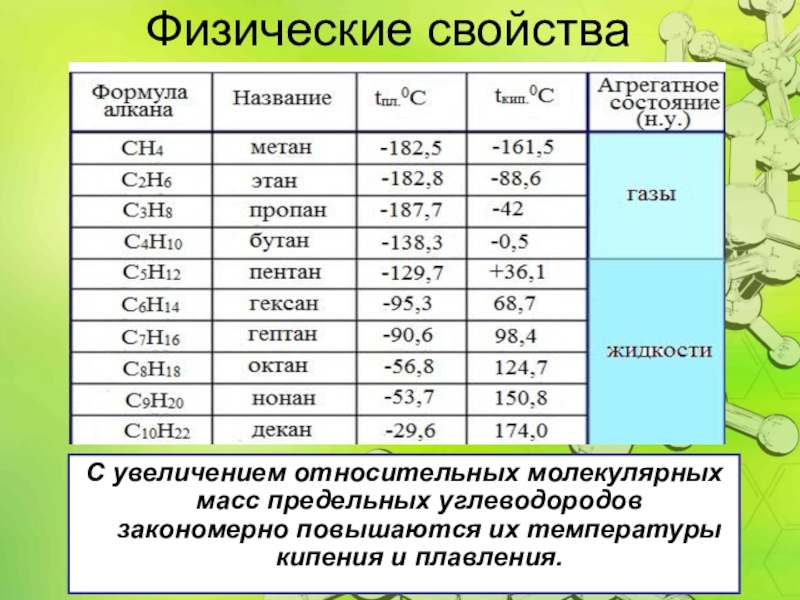
Слайд 9
Физические свойства
С увеличением относительных молекулярных масс предельных углеводородов закономерно повышаются
Слайд 10ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ. НАХОЖДЕНИЕ В ПРИРОДЕ.
МЕТАН – газ, без цвета и
Слайд 11ЭТАН, ПРОПАН И БУТАН входят в состав природного и попутного нефтяного
Остальные АЛКАНЫ в основном содержатся в нефти.
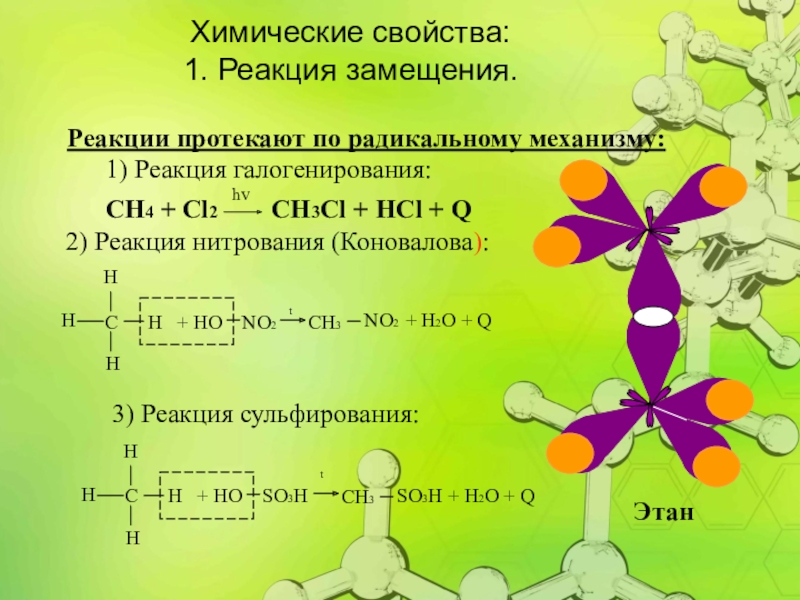
Слайд 12СН4 + Сl2 CH3Cl + HCl + Q
Реакции протекают по радикальному механизму:
Этан
С Н
Н
Н
Н
+ НО NO2
СН3
NO2
+ H2O + Q
С Н
Н
Н
Н
+ НО SO3H
СН3
SO3H
+ H2O + Q
t
t
Химические свойства:
1. Реакция замещения.
2) Реакция нитрования (Коновалова):
3) Реакция сульфирования:
1) Реакция галогенирования:
Слайд 132. Реакции изомеризации:
СН3 СН2
t, катализатор
СН3 СН СН2 СН3
СН3
3.Реакции с водяным паром:
СН4 + Н2О СО + 3Н2
800°С
синтез-газ
4. Реакции дегидрирования:
2СН4 Н С ≡ С Н + 3Н2 + Q
1500°С
СН3 СН3 Н2С=СН2 + Н2 + Q
5.Реакции окисления или реакция горения:
Предельные углеводороды горят (пламя не коптящее):
С3Н8 + 5О2
3СО2 + 4Н2О + Q
В присутствии катализаторов окисляются:
СН4 + О2
500°С, катализатор
Н С
О
Н
+ Н2О + Q
Слайд 14Применение алканов
1-3 – производство сажи
(1 – картриджи;
2 – резина;
3 – типографическая
4-7 – получение
органических веществ
(4 – растворителей;
5 – хладогентов,
используемых
в холодильных установках;
6 – метанол;
7 - ацетилен)
Слайд 15Составьте все возможные изомеры для гептана и назовите их
Составьте два ближайших
Определите предельный углеводород, плотность паров которого по воздуху равна двум
Закрепление
Слайд 16Практическая работа
“Изготовление моделей молекул органических веществ.
Составление структурных формул углеводородов”.
Цель работы:
Научиться составлять
Научиться записывать структурные формулы углеводородов и назвать их по международной номенклатуре.
Ход работы:
1.Изучение теоретического материала
2. Выполнение заданий по вариантам
Вывод: