- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме Оксиды и гидроксиды, их свойства дисциплины ОУД.10 Химия, специальности 33.02.01 Фармация, СПО
Содержание
- 1. Презентация по теме Оксиды и гидроксиды, их свойства дисциплины ОУД.10 Химия, специальности 33.02.01 Фармация, СПО
- 2. Дать понятие об амфотерности, амфотерных оксидах и
- 3. Основные классы сложных веществ (повторение)Генетическая связь (повторение)Лабораторная
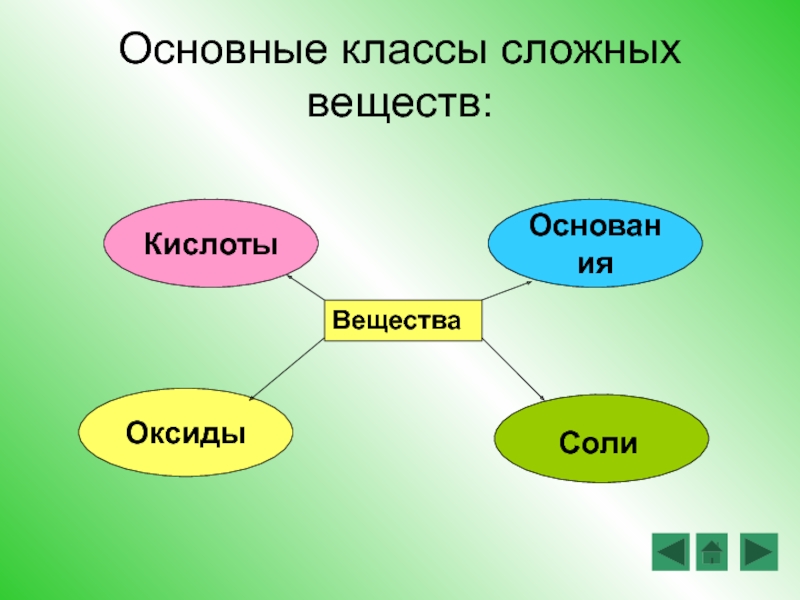
- 4. Основные классы сложных веществ:Вещества Кислоты Основания Оксиды Соли
- 5. Оксиды – это сложные вещества, состоящие из
- 6. Задание 1 Выберите из списка веществ оксиды: H2O,CO2,P2O5,WO3Fe2O3SO3,CaCl2,SCl6,CuO,H2SO4,NaOH,
- 7. Слайд 7
- 8. Основания – это сложные вещества, состоящие из
- 9. Щелочи образованы металлами I группы гл. подгруппы,
- 10. Кислоты – это сложные вещества, молекулы которых
- 11. Соли – это сложные вещества, состоящие из ионов металлов и кислотных остатковСоли KNO3NaClCuSO4FeSCaCO3Ca3(PO4)2
- 12. Распределите вещества по классам
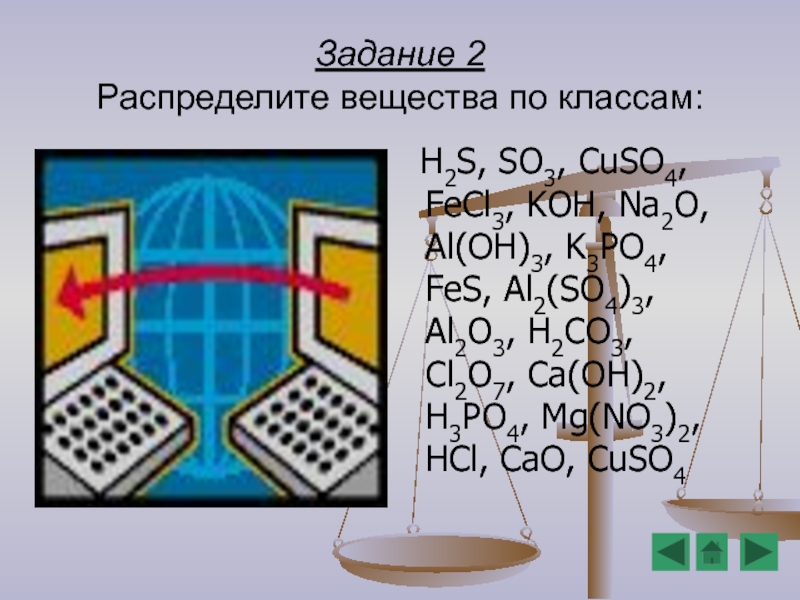
- 13. Задание 2 Распределите вещества по классам:
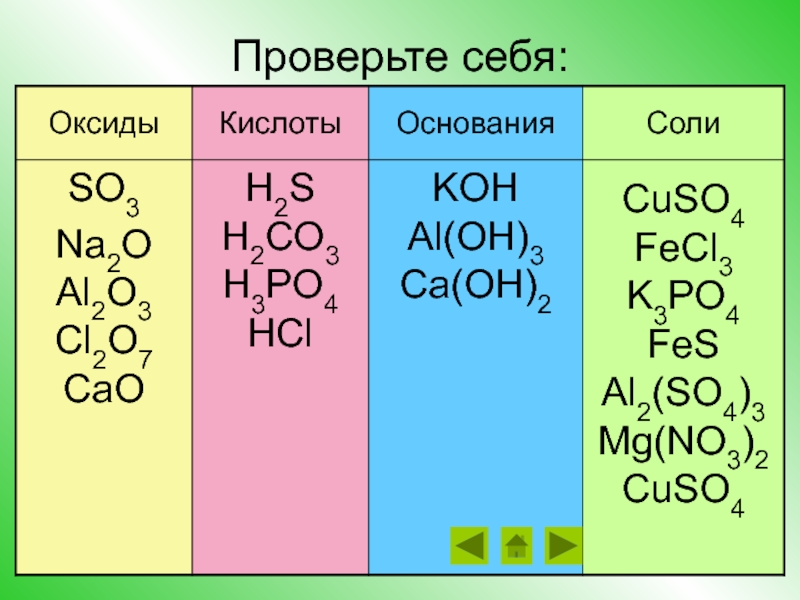
- 14. Проверьте себя:
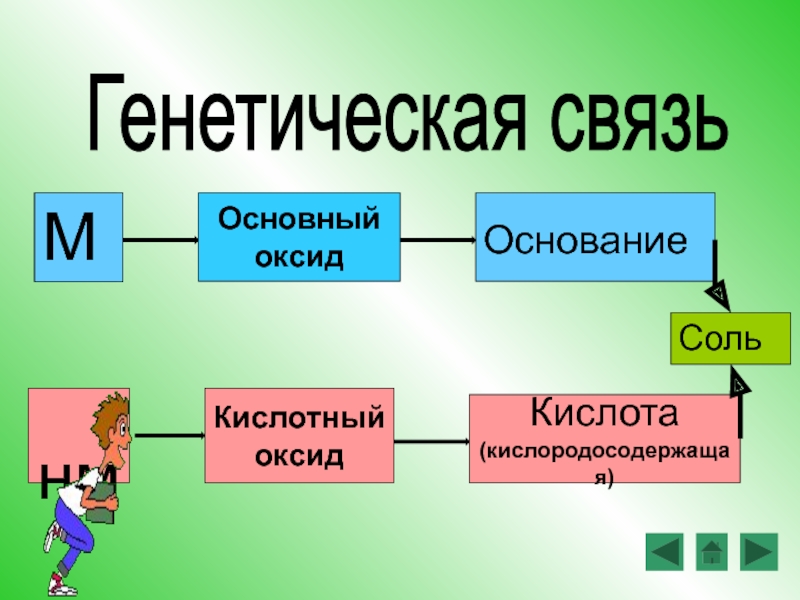
- 15. МОснование нм Кислота (кислородосодержащая)Генетическая связь Основный оксидКислотный оксидСоль
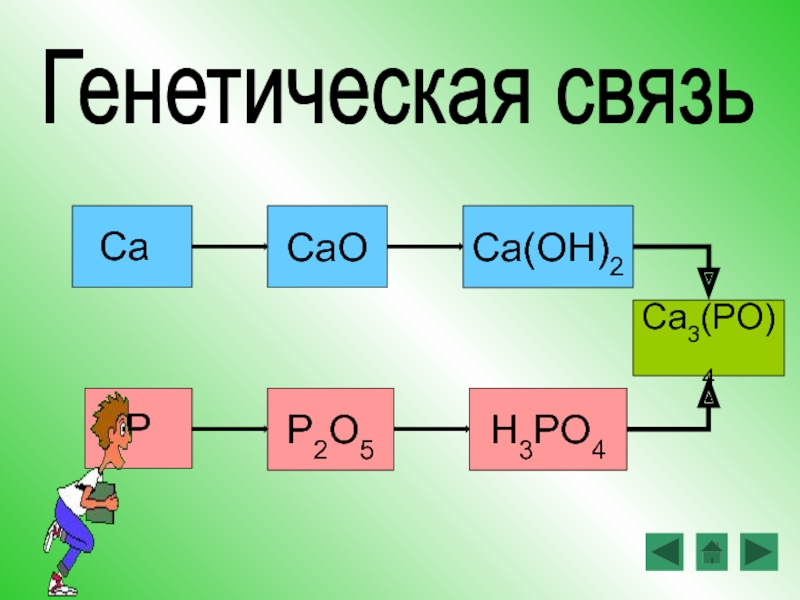
- 16. CaOCa(OH)2P2O5H3PO4PCaГенетическая связь Ca3(PO)4
- 17. Получение гидроксида алюминияВ 2 пробирки налейте по
- 18. Доказательство амфотерности:1.Взаимодействие с кислотами В одну
- 19. Что наблюдали? Осадки гидроксида алюминия в обеих
- 20. Гидроксид – вещество, где есть гидроксогруппа -ОН
- 21. Гидроксид алюминия можно записать как основание и как кислотуAl(OH)3=H3AlO3AlO3H3==Кислота Основание
- 22. Al(OH)3 + 3HCl = AlCl3 +3H2OH3AlO3 + 3NaOH = Na3AlO3+3H2OХлорид алюминияАлюминат натрияЗапишите уравнения реакций:
- 23. Al2O3 + 6HCl = 2AlCl3 +
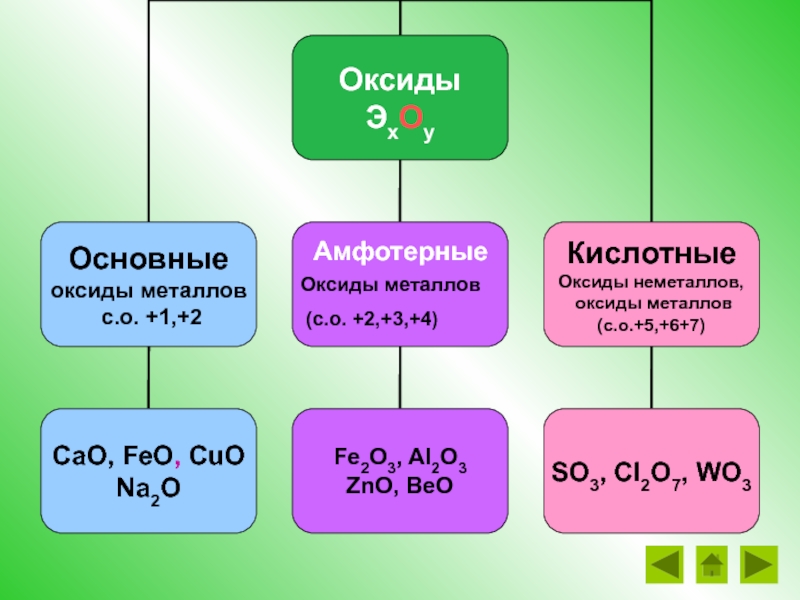
- 24. Амфотерные Оксиды металлов (с.о. +2,+3,+4)
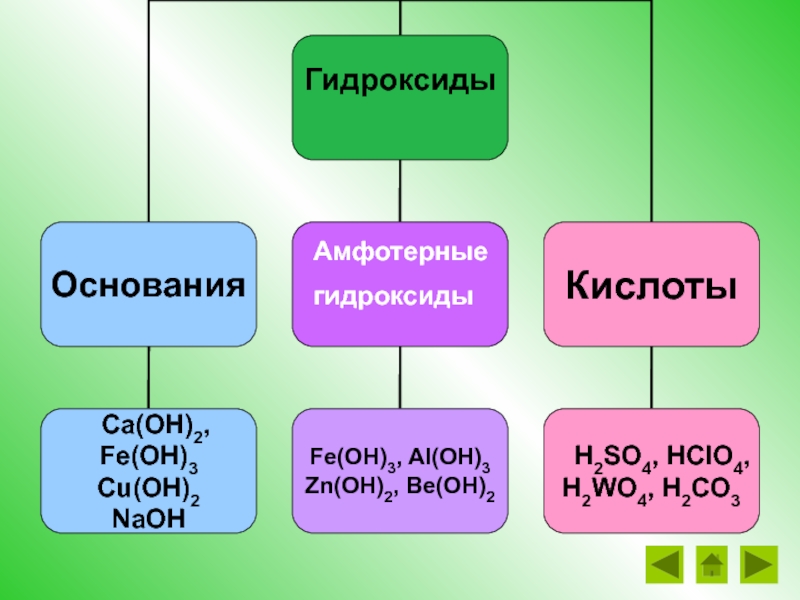
- 25. Амфотерныегидроксиды
- 26. Какие из групп веществ проявляют амфотерные свойства?CaCa(ОН)2,
- 27. Допишите уравнение реакции: Zn(OH)2 + 2NaOH
- 28. Совершенно верно!!!
- 29. Подумай ещё немного!
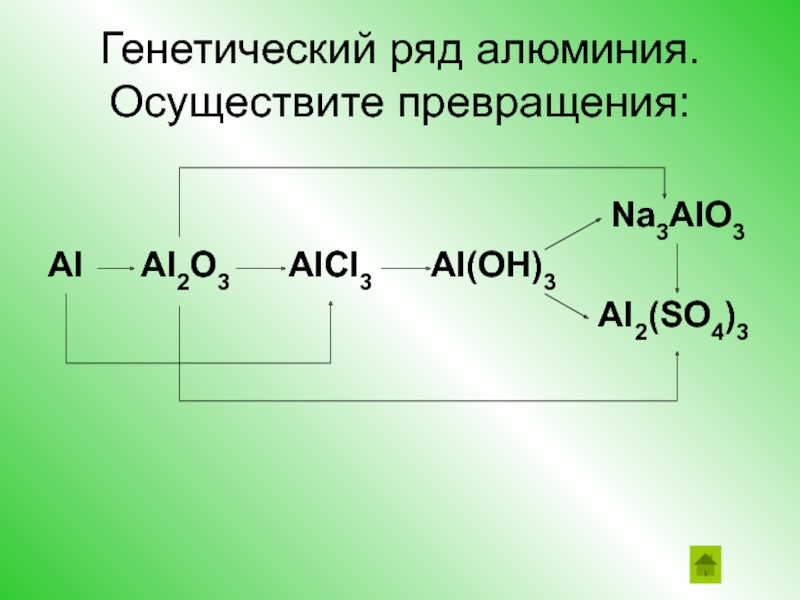
- 30. Генетический ряд алюминия. Осуществите превращения:
Слайд 2Дать понятие об амфотерности, амфотерных оксидах и гидроксидах, переходных металлах;
Повторить, закрепить
Цели урока:
Слайд 3Основные классы сложных веществ (повторение)
Генетическая связь (повторение)
Лабораторная работа
Понятие амфотерности. Понятие амфотерности.
План урока
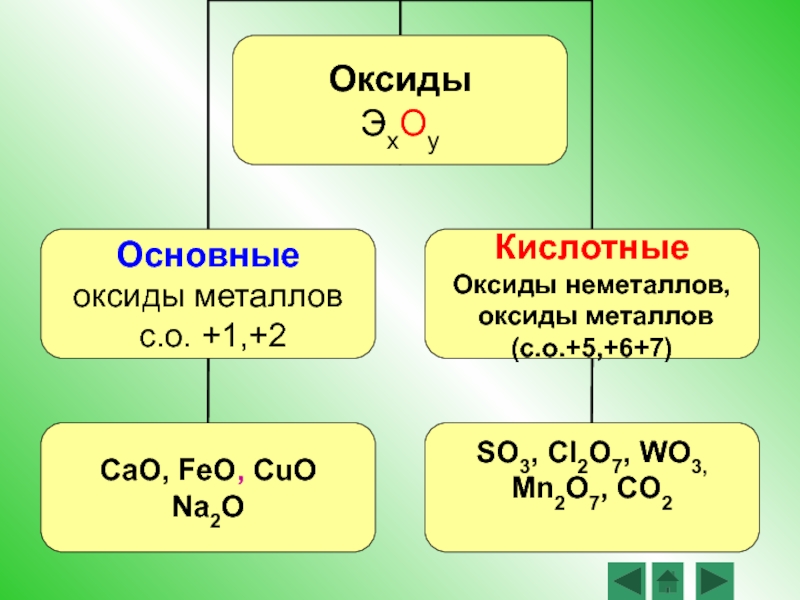
Слайд 5Оксиды – это сложные вещества, состоящие из двух химических элементов, один
SiO2
Cl2O7
CO2
H2O
FeO
оксиды
Слайд 6Задание 1
Выберите из списка веществ оксиды:
H2O,
CO2,
P2O5,
WO3
Fe2O3
SO3,
CaCl2,
SCl6,
CuO,
H2SO4,
NaOH,
Слайд 8
Основания – это сложные вещества, состоящие из ионов металлов и связанных
Основания
-
М(ОН)n
__
где М – металл, n – число групп ОН и в то же время заряд иона металла
NaOH Ca(OH)2 Fe(OH)3
+
+2
+3
Называем: гидроксид металла
Слайд 9
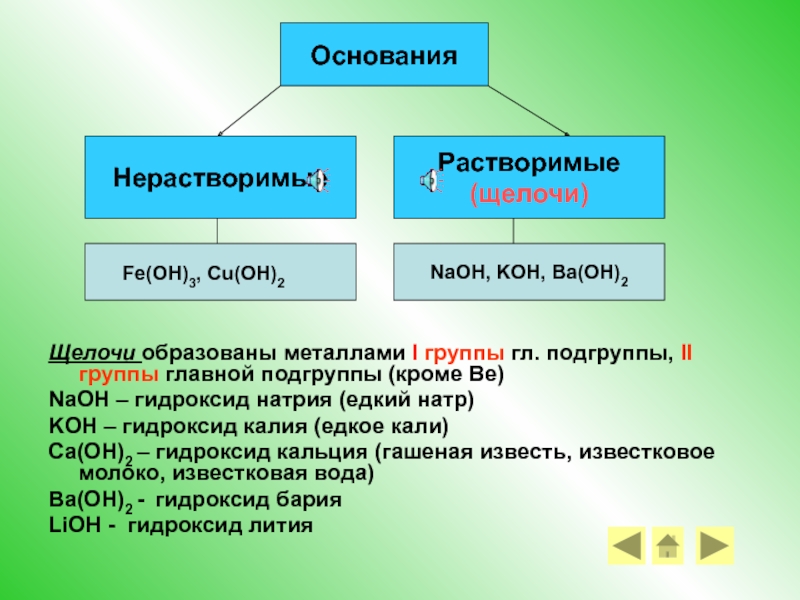
Щелочи образованы металлами I группы гл. подгруппы, II группы главной подгруппы
NaOH – гидроксид натрия (едкий натр)
KOH – гидроксид калия (едкое кали)
Ca(OH)2 – гидроксид кальция (гашеная известь, известковое молоко, известковая вода)
Ba(OH)2 - гидроксид бария
LiOH - гидроксид лития
Основания
Нерастворимые
Растворимые
(щелочи)
NaOH, KOH, Ba(OH)2
Fe(OH)3, Cu(OH)2
Слайд 10
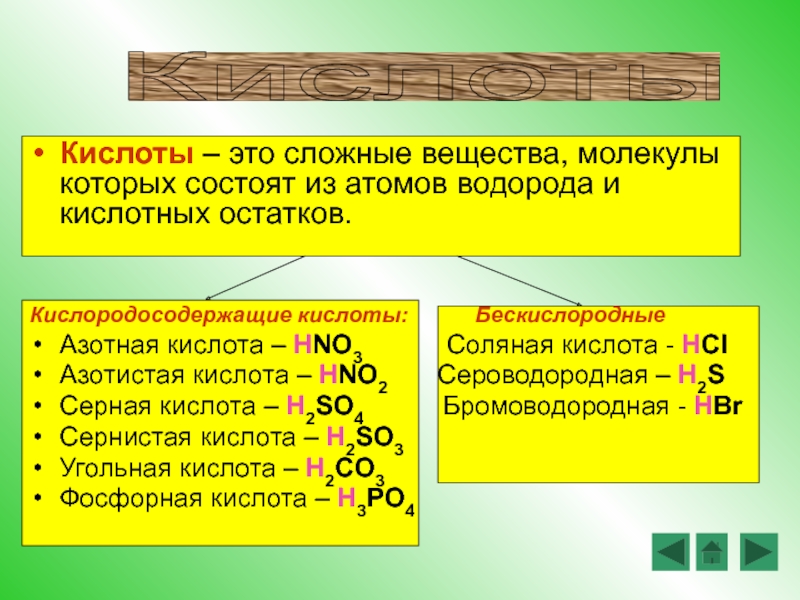
Кислоты – это сложные вещества, молекулы которых состоят из атомов водорода
Кислородосодержащие кислоты: Бескислородные
Азотная кислота – HNO3 Соляная кислота - HCl
Азотистая кислота – HNO2 Сероводородная – H2S
Серная кислота – H2SO4 Бромоводородная - HBr
Сернистая кислота – H2SO3
Угольная кислота – H2CO3
Фосфорная кислота – H3PO4
Кислоты
Слайд 11
Соли – это сложные вещества,
состоящие из ионов металлов
и кислотных
Соли
KNO3
NaCl
CuSO4
FeS
CaCO3
Ca3(PO4)2
Слайд 13Задание 2
Распределите вещества по классам:
H2S, SO3, CuSO4, FeCl3, KOH,
Слайд 15
М
Основание
нм
Кислота
(кислородосодержащая)
Генетическая связь
Основный
оксид
Кислотный
оксид
Соль
Слайд 17Получение гидроксида алюминия
В 2 пробирки налейте по 1 мл раствора соли
В обе пробирки прилейте по каплям раствор щелочи до появления белого осадка гидроксида алюминия:
AlCl3 + 3NaOH Al(OH)3 + 3NaCl
Лабораторная работа
Слайд 18Доказательство амфотерности:
1.Взаимодействие с кислотами
В одну пробирку с осадком прилейте
2.Взаимодействие со щелочами
В другую пробирку с осадком прилейте избыток раствора щелочи
Лабораторная работа
Слайд 19Что наблюдали?
Осадки гидроксида алюминия в обеих пробирках растворяются.
Вывод: гидроксид алюминия
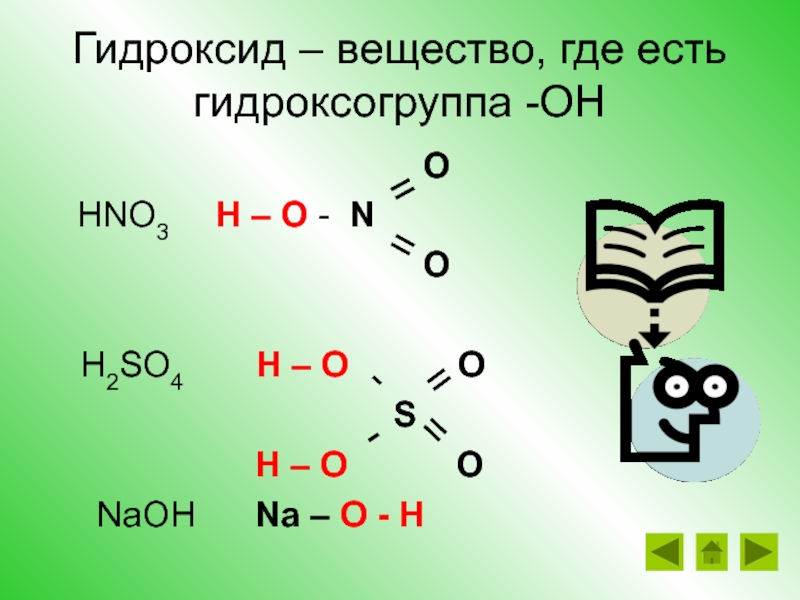
Слайд 20Гидроксид – вещество, где есть гидроксогруппа -ОН
HNO3 H – O - N
O
H2SO4 H – O O
S
H – O O
NaOH Na – O - H
=
=
-
-
=
=
Слайд 21Гидроксид алюминия можно записать как основание и как кислоту
Al(OH)3
=
H3AlO3
AlO3H3
=
=
Кислота
Основание
Слайд 22
Al(OH)3 + 3HCl = AlCl3 +3H2O
H3AlO3 + 3NaOH = Na3AlO3+3H2O
Хлорид алюминия
Алюминат
Запишите уравнения реакций:
Слайд 23
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Al2O3 + 3NaOH
Как основный
Как кислотный
Амфотерность оксида алюминия
Слайд 26Какие из групп веществ проявляют амфотерные свойства?
CaCa(ОН)2, CuCu(ОН)2, NaNaОН, NaОН, FeNaОН,
Fe2O3, Al2O3, , Fe, Fe(, Fe(O, Fe(OН)3 , ZnO, BeZnO, Be(ZnO, Be(OZnO, Be(OН)2
SO3, , Cl2O7, , WO33, Н2SO4, Н2CrO4
Слайд 27Допишите уравнение реакции:
Zn(OH)2 + 2NaOH
в результате образуются
Na2ZnO2 +
Zn(OH)2 + Na2O
ZnSO4 + + 2 + 2NaCl
Реакция не идет