Что можно вдохнуть и сдохнуть, как последний мудак?
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме: Аммиак.
Содержание
- 1. Презентация по теме: Аммиак.
- 2. Скажем вместе- "Аммиак!"
- 3. ЦЕЛЬ УРОКА: изучение строения молекулы аммиака, его
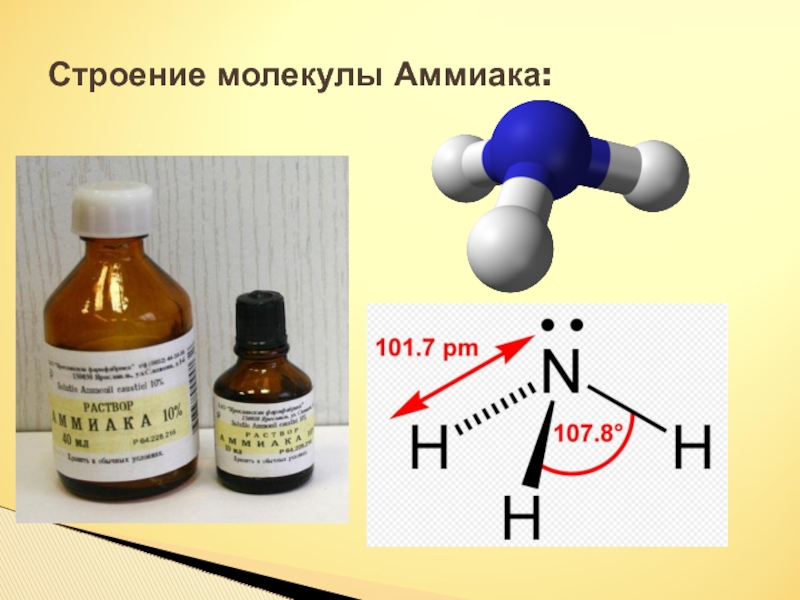
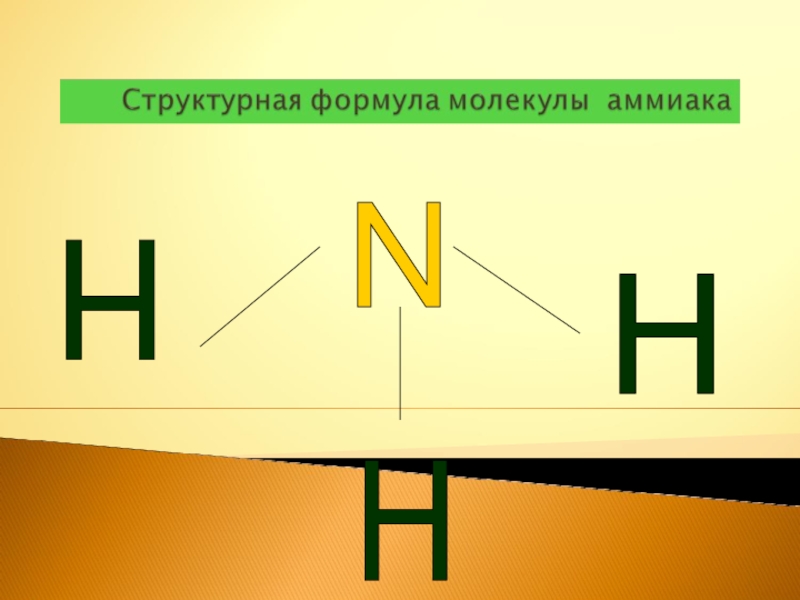
- 4. Строение молекулы Аммиака:
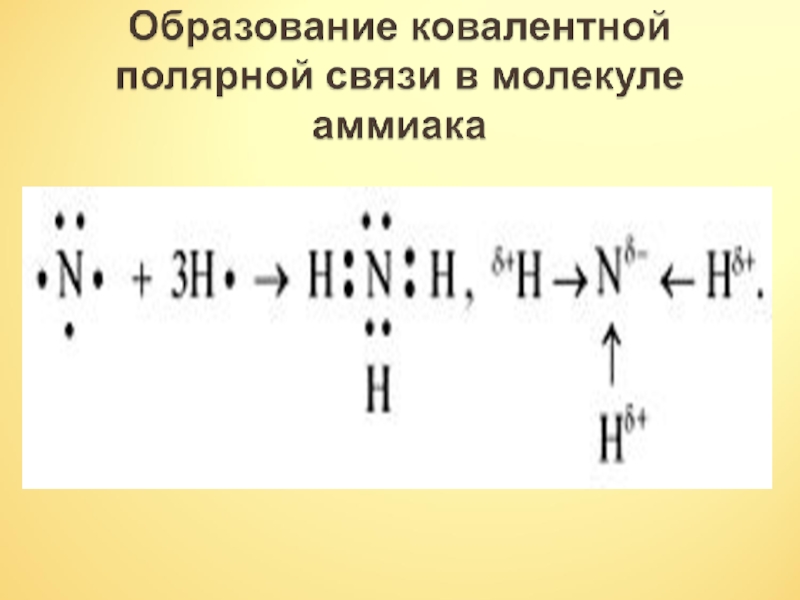
- 5. N H 3
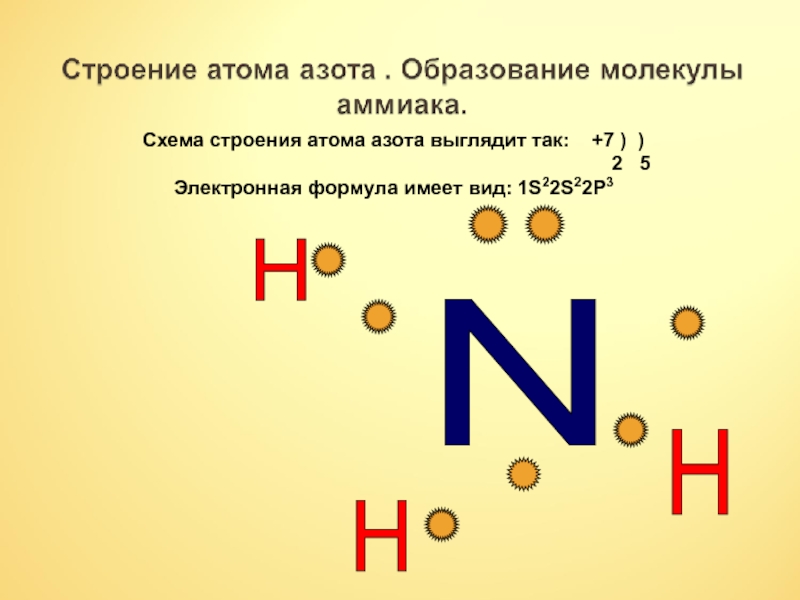
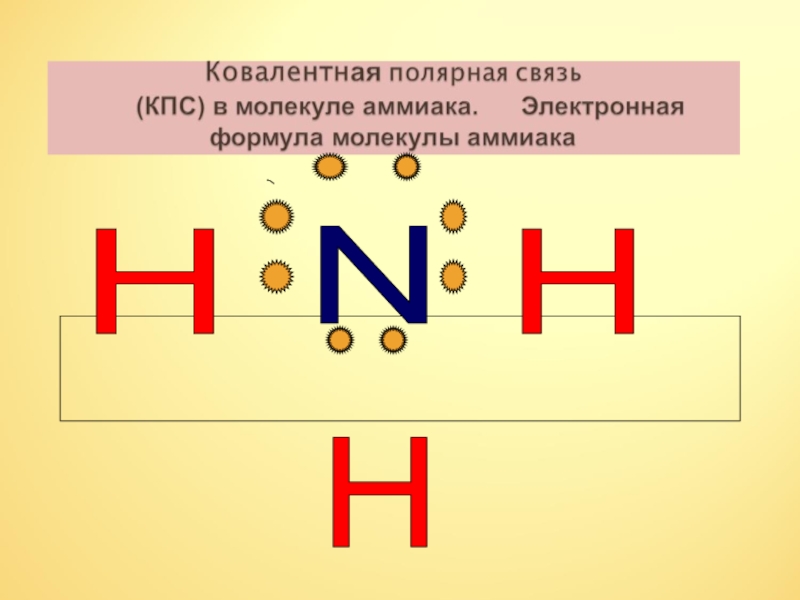
- 6. N H H H Схема строения атома
- 7. Слайд 7
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. Аммиак –это газ, бесцветный, с резким запахом,
- 12. Свойства физическиеСтроениеЛегче воздухаХорошо растворим в водеH2O
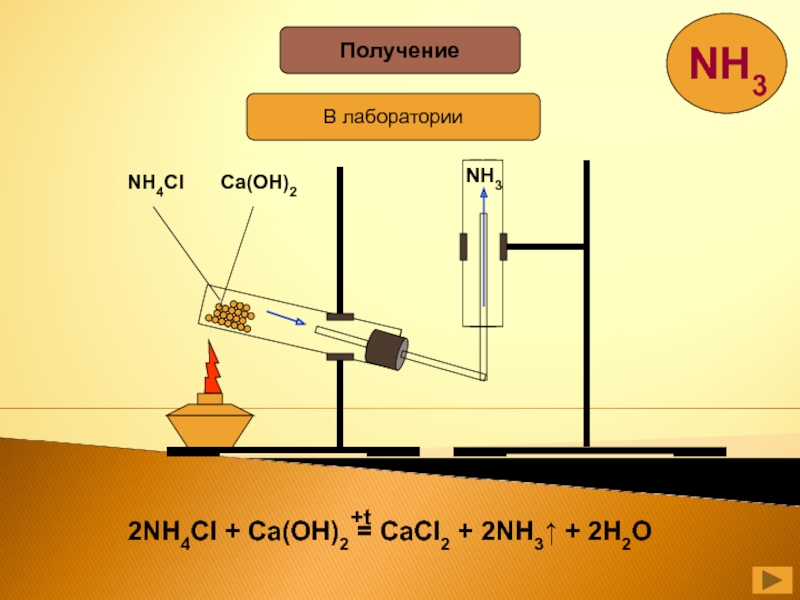
- 13. ПолучениеВ лабораторииNH4ClCa(OH)2NH3
- 14. Получение аммиака
- 15. Слайд 15
- 16. Слайд 16
- 17. Слайд 17
- 18. Растворение аммиака в воде и в кислотах
- 19. Аммиак не горит на воздухе, но в
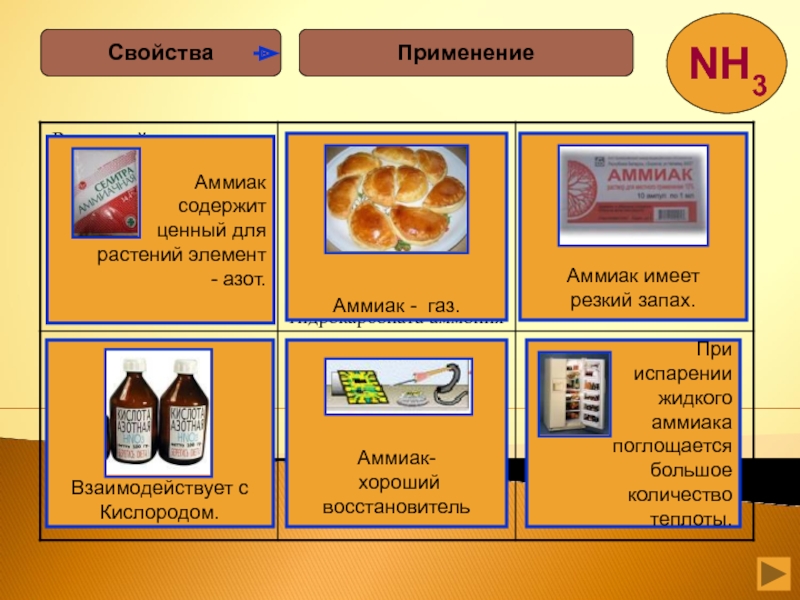
- 20. ПрименениеСвойства
- 21. Чтоб продукты не пропалиВам поможет аммиак, И
- 22. ПРИМЕНЕНИЕ АММИАКА И ЕГО СОЕДИНЕНИЙ
- 23. Нельзя прикасаться к
- 24. N2?NH3?(NH4)2SO4?NH4Cl?NH3 Cоставьте кроссворд, ключевым словом которого будет нашатырь.
Скажем вместе- "Аммиак!"
Слайд 3ЦЕЛЬ УРОКА:
изучение строения молекулы аммиака, его физических и химических свойств;
определение
роли аммиака и его производных в жизни человека, их применение;
Тема урока: Аммиак. Физические и химические свойства аммиака, получение, применение.
Слайд 6N
H
H
H
Схема строения атома азота выглядит так:
+7 ) )
2 5
Электронная формула имеет вид: 1S22S22P3
2 5
Электронная формула имеет вид: 1S22S22P3
Слайд 11Аммиак –это газ, бесцветный,
с резким запахом,
ядовит,
сжижается при –33,35
°С,
затвердевает при –77,7 °С.
при давлении 9•105 Па сжижается уже при комнатной температуре,
хорошо растворим в воде, при 20 °С в 1 объеме воды растворяется 700 объемов аммиака,
а также хорошо растворяется в спиртах, ацетоне.
Кроме того, сжиженный аммиак при испарении поглощает тепло,
при соприкосновении с кожей возникает обморожение различной степени.
затвердевает при –77,7 °С.
при давлении 9•105 Па сжижается уже при комнатной температуре,
хорошо растворим в воде, при 20 °С в 1 объеме воды растворяется 700 объемов аммиака,
а также хорошо растворяется в спиртах, ацетоне.
Кроме того, сжиженный аммиак при испарении поглощает тепло,
при соприкосновении с кожей возникает обморожение различной степени.
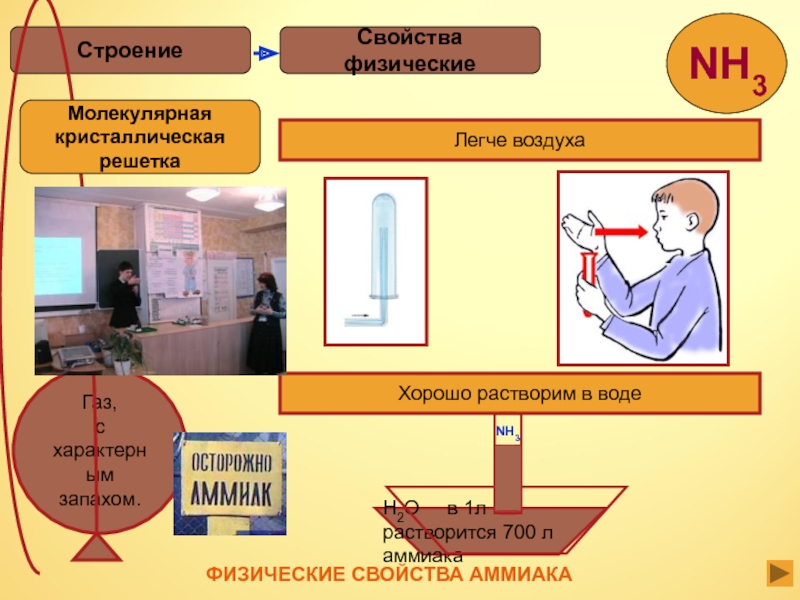
Слайд 12Свойства физические
Строение
Легче воздуха
Хорошо растворим в воде
H2O в 1л растворится
700 л аммиака
NH3
Молекулярная
кристаллическая
решетка
ФИЗИЧЕСКИЕ СВОЙСТВА АММИАКА
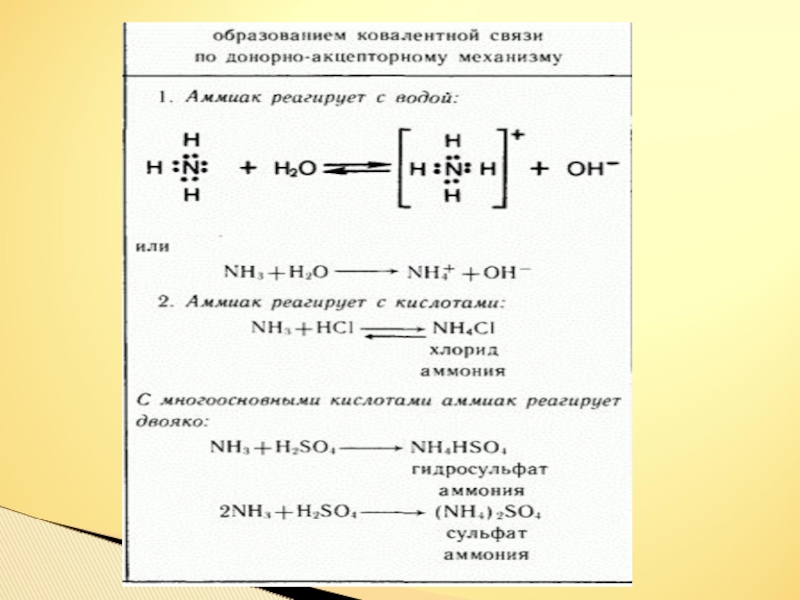
Слайд 18Растворение аммиака в воде и в кислотах – процесс химический, в
основе которого лежит способность молекул аммиака связывать ионы водорода. Причина этого – наличие у атома азота свободной электронной пары, которая «перетягивает» протон водорода из молекул воды и кислоты.
Слайд 19Аммиак не горит на воздухе, но в чистом кислороде или в
присутствии катализатора аммиак хорошо окисляется, проявляя свойства восстановителя.
Слайд 21Чтоб продукты не пропали
Вам поможет аммиак,
И растениям, конечно,
Аммиак совсем не
враг.
Если обморок случился –
Может в чувство привести,
Вывести из опьяненья,
Глянец окнам навести.
Если обморок случился –
Может в чувство привести,
Вывести из опьяненья,
Глянец окнам навести.
Слайд 23
Нельзя прикасаться к разлитому веществу, это может
вызвать болезненный ожог кожных покровов.
При утечке аммиака важно в первую очередь защитить кожу и органы дыхания, а также избегать падания аммиака в глаза.
Категорически запрещается делать искусственное дыхание, если человек надышался аммиачными парами, так как это только ускорит процесс окисления и вызовет удушье.
При отравлении аммиаком нельзя пить, а нужно закапать в глаза альбуцид или промыть глаза раствором борной кислоты.
В нос закапать теплое подсолнечное, оливковое или персиковое масло, а лицо, руки и вообще пораженные участки тела промыть 2-процентным раствором борной кислоты.
При утечке аммиака важно в первую очередь защитить кожу и органы дыхания, а также избегать падания аммиака в глаза.
Категорически запрещается делать искусственное дыхание, если человек надышался аммиачными парами, так как это только ускорит процесс окисления и вызовет удушье.
При отравлении аммиаком нельзя пить, а нужно закапать в глаза альбуцид или промыть глаза раствором борной кислоты.
В нос закапать теплое подсолнечное, оливковое или персиковое масло, а лицо, руки и вообще пораженные участки тела промыть 2-процентным раствором борной кислоты.