- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии решение задач
Содержание
- 1. Презентация по химии решение задач
- 2. Задание 21 № 579К 104 г раствора с массовой
- 3. Слайд 3
- 4. Задание 21 № 603К раствору сульфита натрия массой 252
- 5. Задание 21 № 668Через 10%-ный раствор серной кислоты пропускали
- 6. Задание 21 № 880К 125 г раствора серной кислоты
- 7. Из данного перечня веществ выберите те, с
- 8. Расставить коэффициенты, написать полные и сокращенные уравнения
- 9. Часть В. Установите соответствие 10.Название органического соединенияКласс органического соединенияа)толуолб)гексанв)ацетиленг)бутадиен -1,31)алканы2)алкадиены3)арены4)алкины5)алкены
- 10. Органическое соединение(класс)Характерная химическая реакция(тип)а) пропенб) пентанв) 2,3 – дихлорбутанг)бензол1)дегидрохлорирования2)гидрирования3)р-я дегидрирования4)обесцвечивание бромной воды
Задание 21 № 579К 104 г раствора с массовой долей хлорида бария 9% добавили избыток раствора фосфорной кислоты. Вычислите массу образовавшегося осадка. Ответ округлите до целых.Задание 21 № 580К 296 г раствора с массовой долей нитрата магния 6% добавили избыток
Слайд 2Задание 21 № 579
К 104 г раствора с массовой долей хлорида бария 9%
добавили избыток раствора фосфорной кислоты. Вычислите массу образовавшегося осадка. Ответ округлите до целых.
Задание 21 № 580
К 296 г раствора с массовой долей нитрата магния 6% добавили избыток раствора фосфорной кислоты. Вычислите массу образовавшегося осадка.
Задание 21 № 601
К 250 г раствора карбоната натрия добавляли раствор хлорида бария до прекращения выделения осадка. Масса отфильтрованного и высушенного осадка составила 39,4 г. Рассчитайте массовую долю карбоната натрия в исходном растворе.
Задание 21 № 580
К 296 г раствора с массовой долей нитрата магния 6% добавили избыток раствора фосфорной кислоты. Вычислите массу образовавшегося осадка.
Задание 21 № 601
К 250 г раствора карбоната натрия добавляли раствор хлорида бария до прекращения выделения осадка. Масса отфильтрованного и высушенного осадка составила 39,4 г. Рассчитайте массовую долю карбоната натрия в исходном растворе.
Слайд 4Задание 21 № 603
К раствору сульфита натрия массой 252 г и массовой долей
5% добавили избыток раствора соляной кислоты. Вычислите объем (н. у.) выделившегося газа.
Задание 21 № 624
К 150 г раствора карбоната натрия добавили избыток разбавленной серной кислоты, и раствор нагрели до окончания выделения газа. Всего выделилось 3,36 л газа (н. у.). Рассчитайте массовую долю карбоната натрия в исходном растворе.
Задание 21 № 646
Через 5%-ный раствор сульфата меди(II) пропускали сероводород до прекращения выделения чёрного осадка. Масса осадка составила 14,4 г. Чему равна масса раствора сульфата меди(II)?
Задание 21 № 624
К 150 г раствора карбоната натрия добавили избыток разбавленной серной кислоты, и раствор нагрели до окончания выделения газа. Всего выделилось 3,36 л газа (н. у.). Рассчитайте массовую долю карбоната натрия в исходном растворе.
Задание 21 № 646
Через 5%-ный раствор сульфата меди(II) пропускали сероводород до прекращения выделения чёрного осадка. Масса осадка составила 14,4 г. Чему равна масса раствора сульфата меди(II)?
Слайд 5Задание 21 № 668
Через 10%-ный раствор серной кислоты пропускали аммиак до полного образования
средней соли. Всего израсходовано 11,2 л (н. у.) аммиака. Определите массу исходного раствора серной кислоты.
Задание 21 № 690
170 г раствора нитрата серебра смешали с избытком раствора хлорида натрия. Выпал осадок массой 8,61 г. Вычислите массовую долю соли в растворе нитрата серебра.
Задание 21 № 814
К 252 г раствора сульфита натрия с массовой долей соли 5,0 % добавили избыток соляной кислоты. Вычислите объём (н. у.) выделившегося газа.
Задание 21 № 690
170 г раствора нитрата серебра смешали с избытком раствора хлорида натрия. Выпал осадок массой 8,61 г. Вычислите массовую долю соли в растворе нитрата серебра.
Задание 21 № 814
К 252 г раствора сульфита натрия с массовой долей соли 5,0 % добавили избыток соляной кислоты. Вычислите объём (н. у.) выделившегося газа.
Слайд 6Задание 21 № 880
К 125 г раствора серной кислоты добавили избыток гидрокарбоната натрия.
Общий объём выделившегося газа составил 11,2 л (н. у.). Определите массовую долю серной кислоты в растворе
Задание 21 № 914
Для полной нейтрализации серной кислоты к 250 г её раствора потребовалось добавить 280 г 10-процентного раствора гидроксида натрия. Определите массовую долю серной кислоты в исходном растворе
Задание 21 № 936
Для полной нейтрализации гидроксида бария к 250 г его раствора потребовалось добавить 50 г 7,3-процентной соляной кислоты. Определите массовую долю гидроксида бария в исходном растворе.
Задание 21 № 914
Для полной нейтрализации серной кислоты к 250 г её раствора потребовалось добавить 280 г 10-процентного раствора гидроксида натрия. Определите массовую долю серной кислоты в исходном растворе
Задание 21 № 936
Для полной нейтрализации гидроксида бария к 250 г его раствора потребовалось добавить 50 г 7,3-процентной соляной кислоты. Определите массовую долю гидроксида бария в исходном растворе.
Слайд 7Из данного перечня веществ выберите те, с которыми взаимодействует натрий: вода,
водород, магний, кислород, соляная кислота. Напишите уравнения реакций, составьте электронный баланс.
Из данного перечня веществ выберите те, с которыми взаимодействует магний: сера, аргон, хлор, кислород, соляная кислота. Напишите уравнения реакций, составьте электронный баланс.
Из данного перечня веществ выберите те, с которыми взаимодействует магний: сера, аргон, хлор, кислород, соляная кислота. Напишите уравнения реакций, составьте электронный баланс.
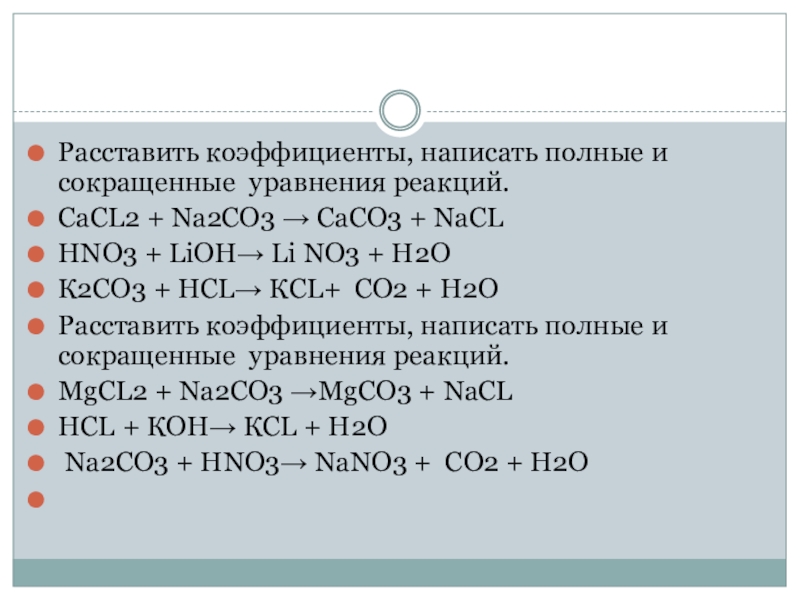
Слайд 8Расставить коэффициенты, написать полные и сокращенные уравнения реакций.
СаСL2 + Na2CО3
СаСО3 + NaСL
HNO3 + LiОН Li NO3 + Н2О
К2CО3 + НСL КСL+ СО2 + Н2О
Расставить коэффициенты, написать полные и сокращенные уравнения реакций.
MgСL2 + Na2CО3 MgСО3 + NaСL
HСL + КОН КСL + Н2О
Na2CО3 + НNO3 NaNO3 + СО2 + Н2О
HNO3 + LiОН Li NO3 + Н2О
К2CО3 + НСL КСL+ СО2 + Н2О
Расставить коэффициенты, написать полные и сокращенные уравнения реакций.
MgСL2 + Na2CО3 MgСО3 + NaСL
HСL + КОН КСL + Н2О
Na2CО3 + НNO3 NaNO3 + СО2 + Н2О
Слайд 9Часть В. Установите соответствие
10.
Название органического соединения
Класс органического соединения
а)толуол
б)гексан
в)ацетилен
г)бутадиен -1,3
1)алканы
2)алкадиены
3)арены
4)алкины
5)алкены
Слайд 10Органическое соединение(класс)
Характерная химическая реакция(тип)
а) пропен
б) пентан
в) 2,3 – дихлорбутан
г)бензол
1)дегидрохлорирования
2)гидрирования
3)р-я дегидрирования
4)обесцвечивание
бромной воды