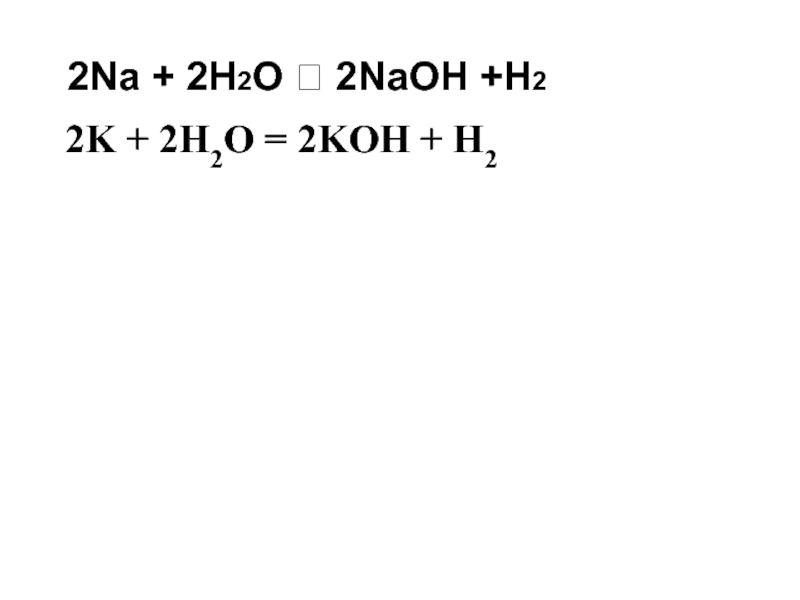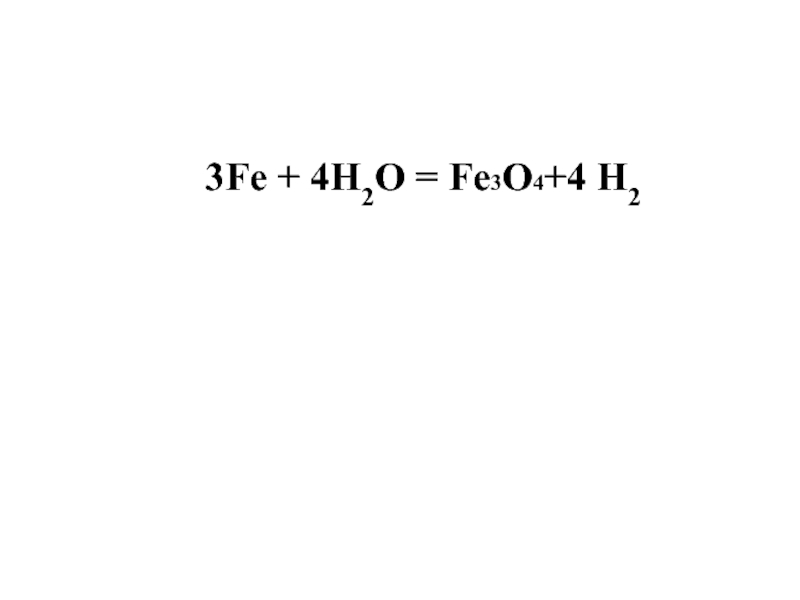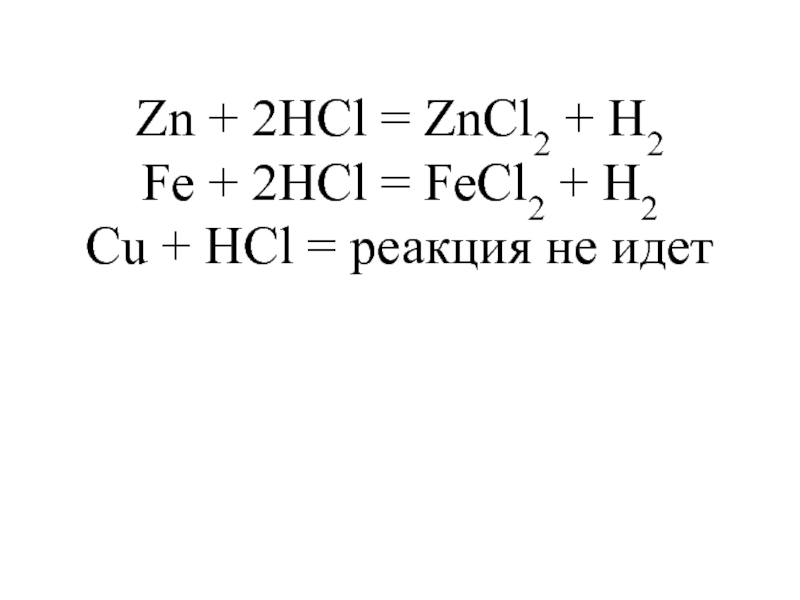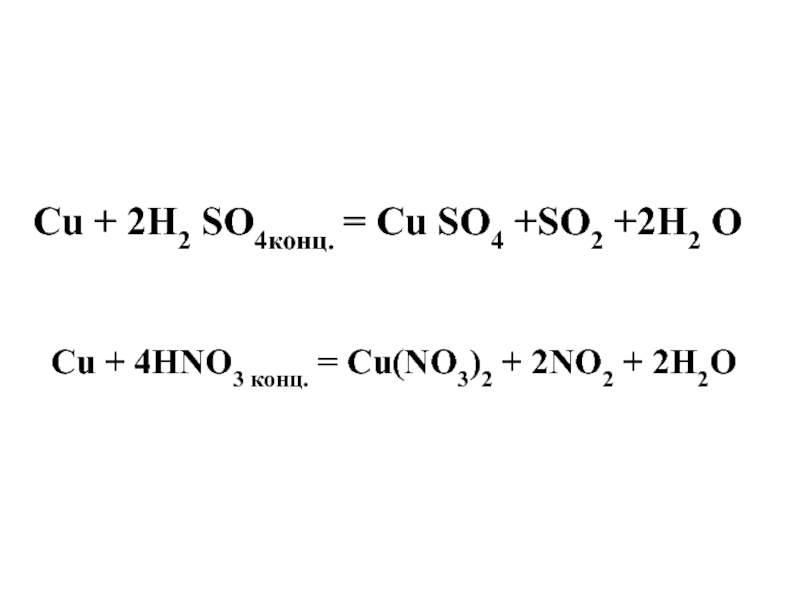- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Общие свойства метеллов (9 класс, 11 класс)
Содержание
- 1. Презентация по химии Общие свойства метеллов (9 класс, 11 класс)
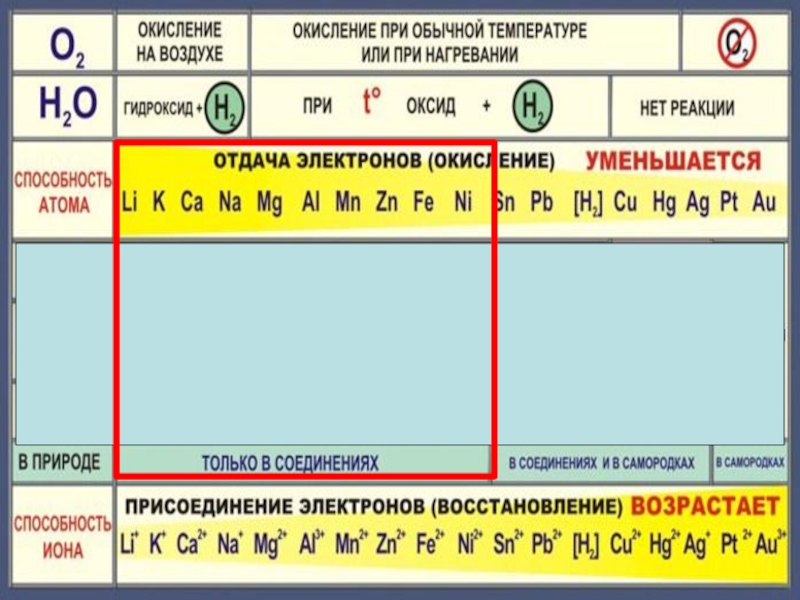
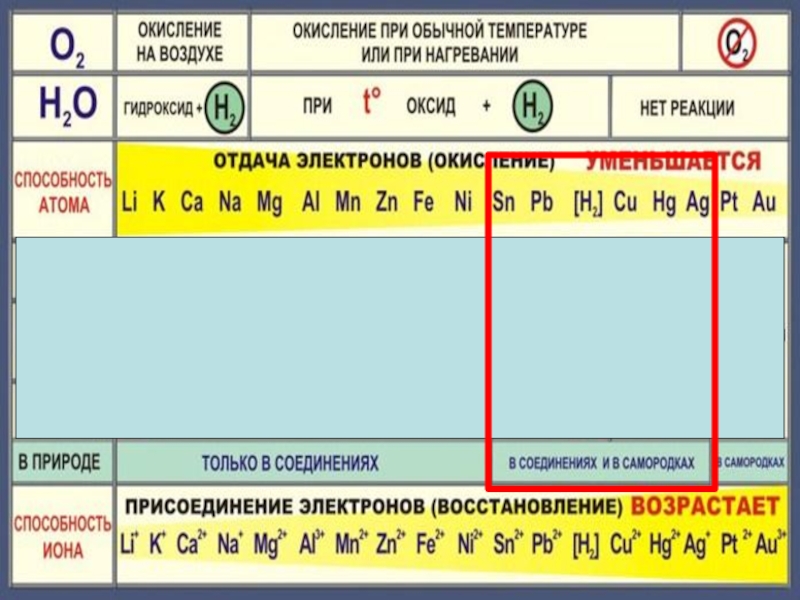
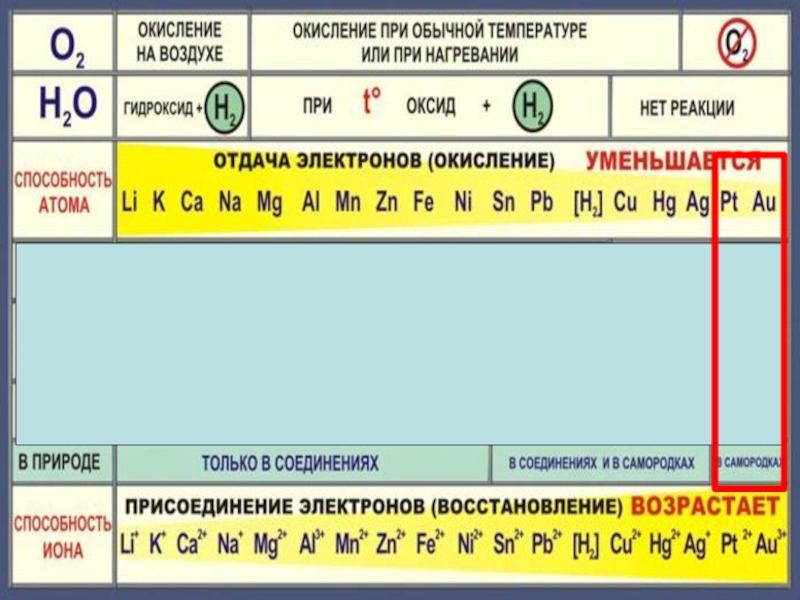
- 2. Слайд 2
- 3. Слайд 3
- 4. Слайд 4
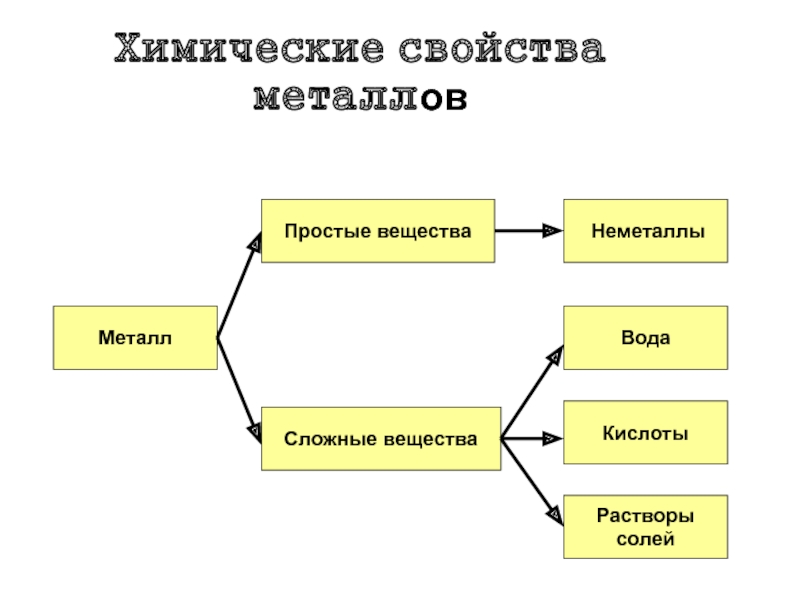
- 5. Химические свойства металловМеталлПростые веществаСложные вещества НеметаллыВодаКислотыРастворысолей
- 6. Cu + Cl2 =CuCl22Mg + CO2 = 2MgO + CС неметалламиС кислотными оксидамиFe + S =FeS
- 7. Слайд 7
- 8. Слайд 8
- 9. Слайд 9
- 10. 4Na + O2 = 2Na2O2Mg + O2
- 11. Слайд 11
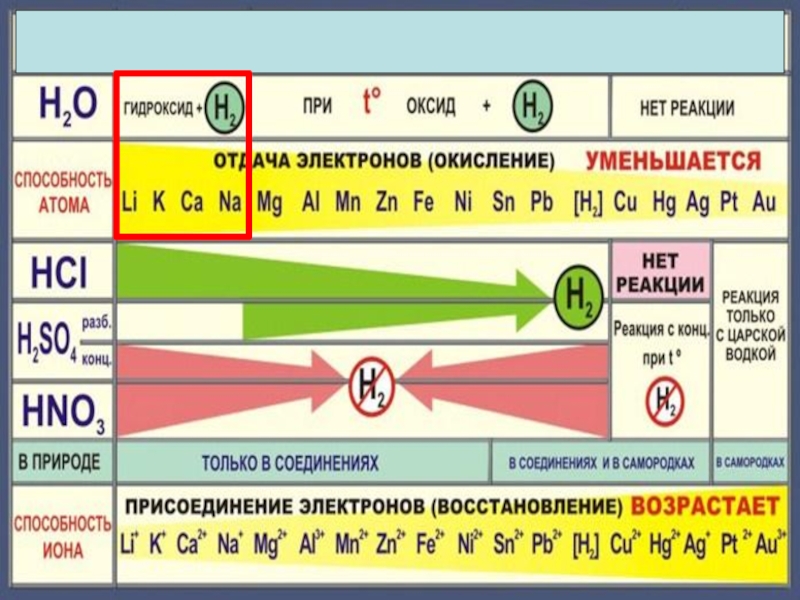
- 12. 2Na + 2H2O 2NaOH +H2 2K + 2H2O = 2KOH + H2
- 13. Слайд 13
- 14. 3Fe + 4H2O = Fe3O4+4 H2
- 15. Слайд 15
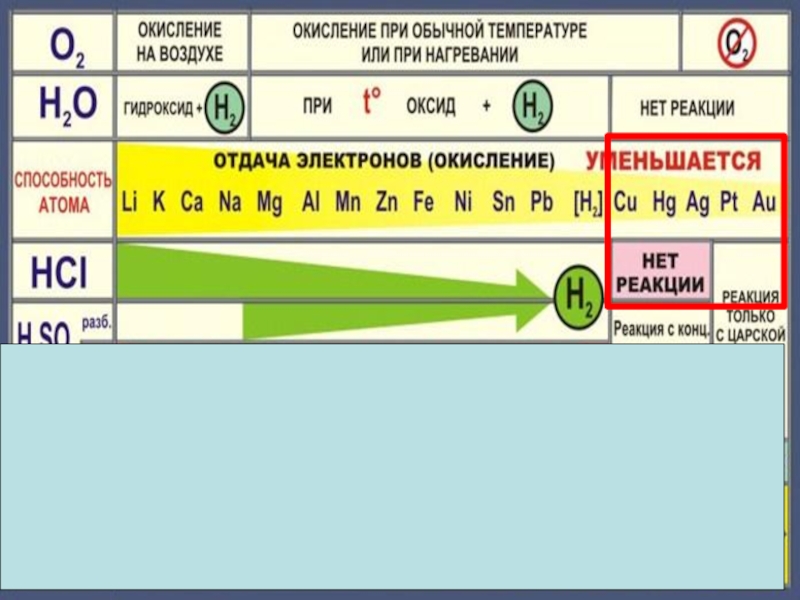
- 16. Cu + H2О = реакция не идет
- 17. Слайд 17
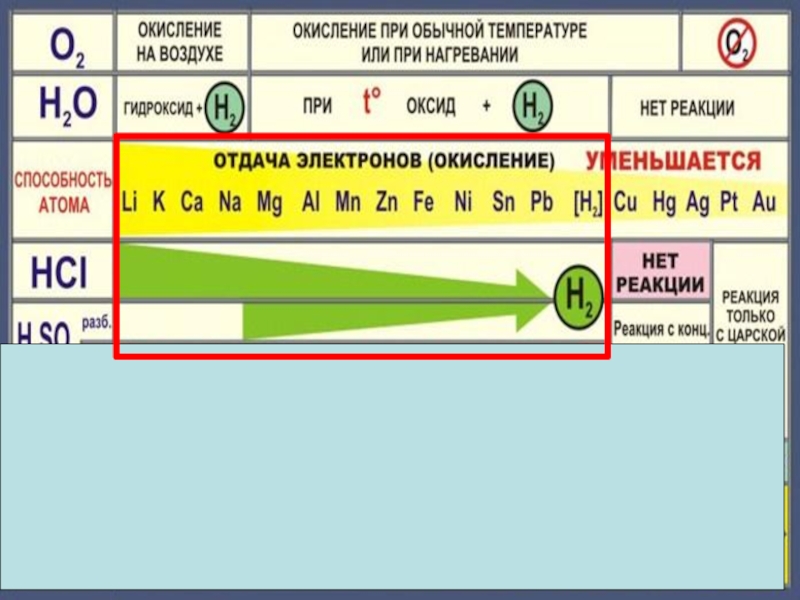
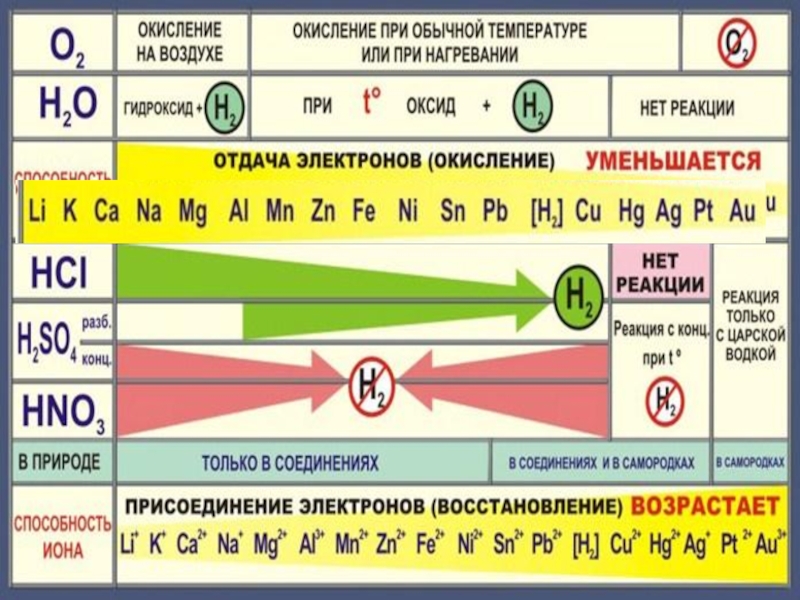
- 18. Zn + 2HCl = ZnCl2 + H2Fe
- 19. Слайд 19
- 20. Слайд 20
- 21. Слайд 21
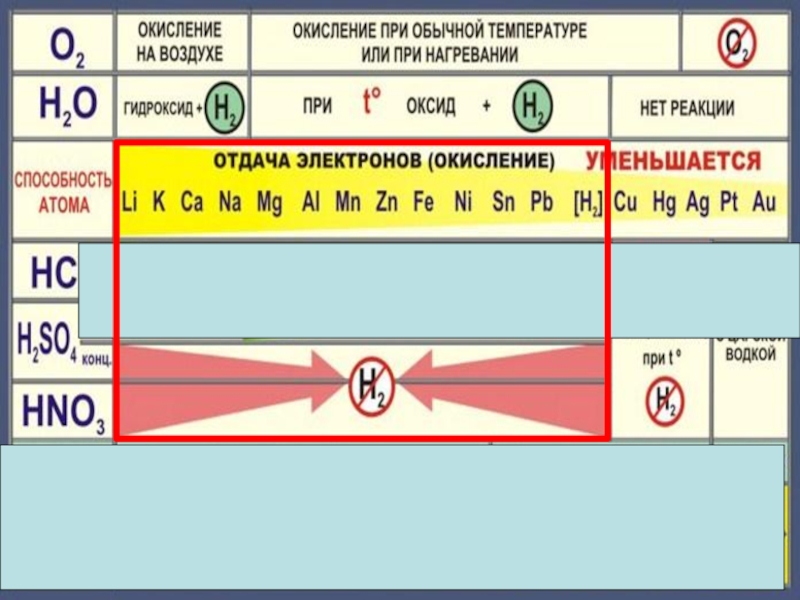
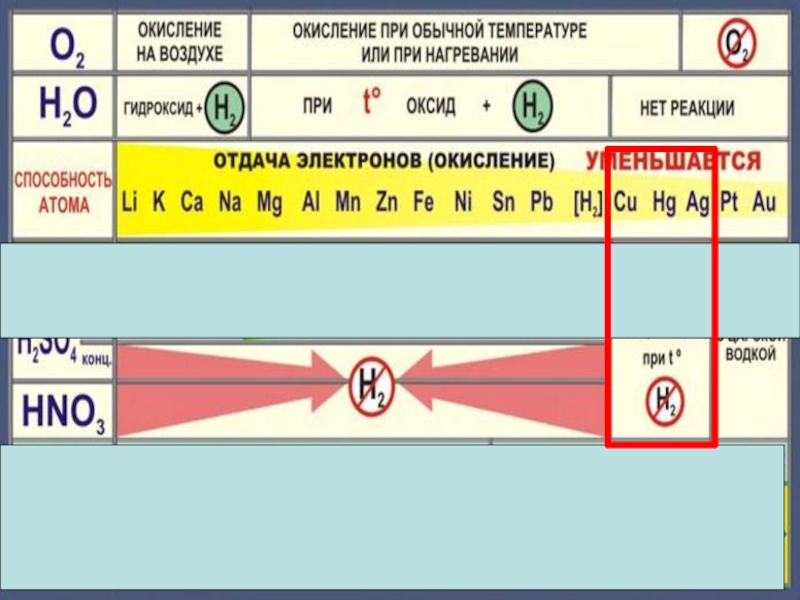
- 22. Cu + 2H2 SO4конц. = Cu SO4
- 23. Состав «царской водки»:смесь концентрированных азотной HNO3 (65-68
- 24. Слайд 24
- 25. Слайд 25
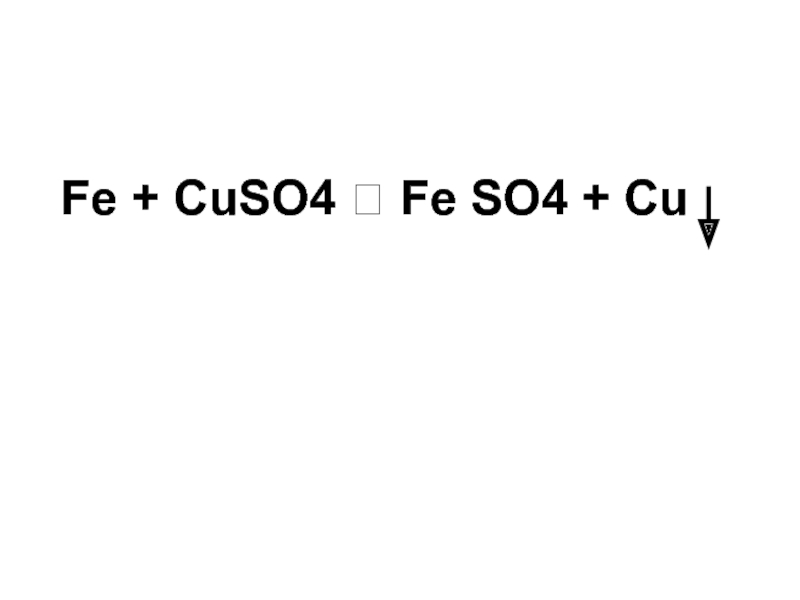
- 26. Fe + CuSO4 Fe SO4 + Cu
- 27. Домашнее задание:§8, в. 6.
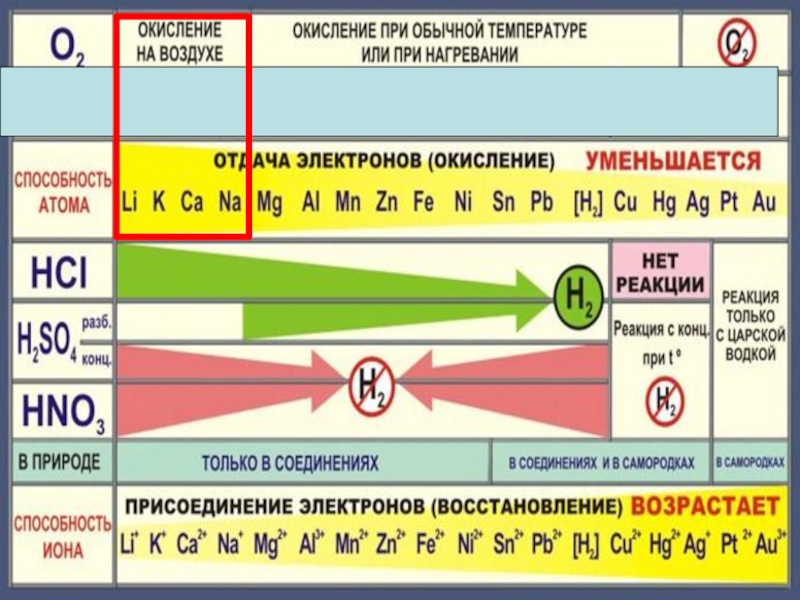
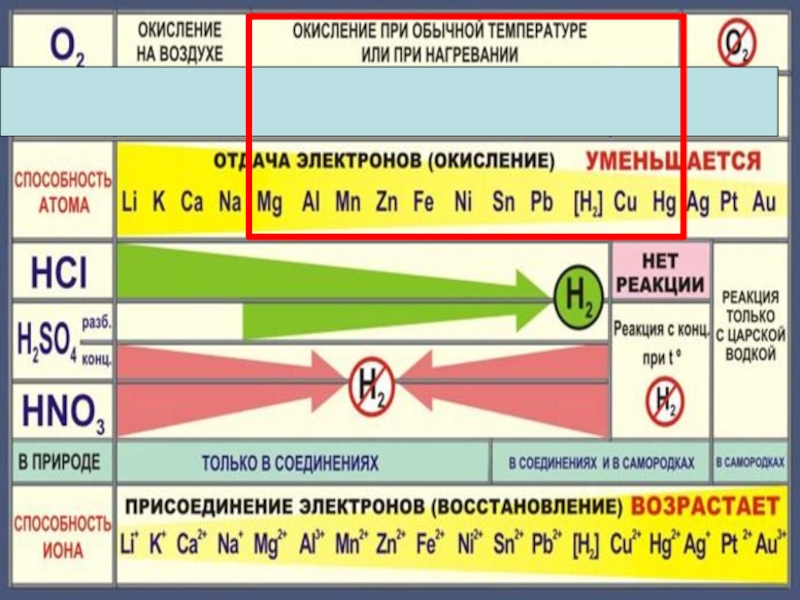
Химические свойства металловМеталлПростые веществаСложные вещества НеметаллыВодаКислотыРастворысолей
Слайд 5Химические свойства металлов
Металл
Простые вещества
Сложные вещества
Неметаллы
Вода
Кислоты
Растворы
солей
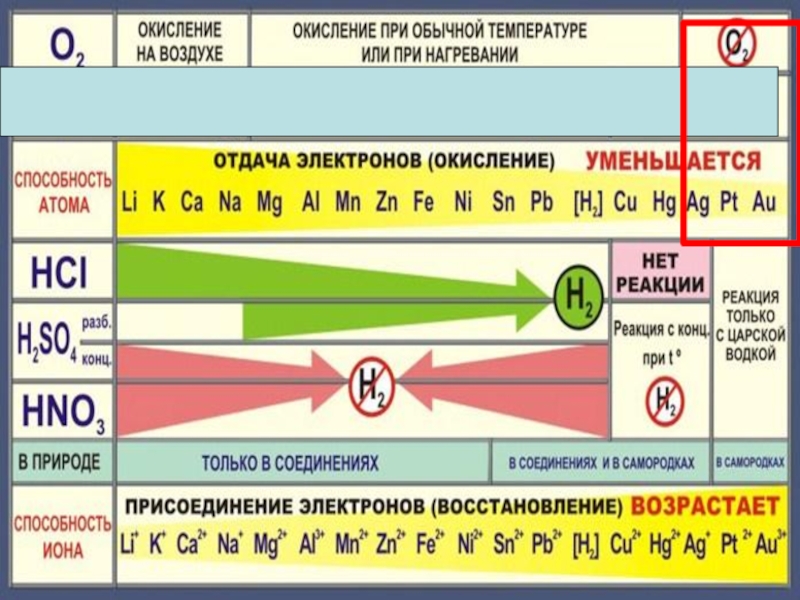
Слайд 104Na + O2 = 2Na2O
2Mg + O2 = 2MgO при нагревании
4Ag
+ O2 = 2Ag2O
при электрическом разряде
и повышенной влажности
при электрическом разряде
и повышенной влажности
4Au + O2 =
Слайд 23Состав «царской водки»:
смесь концентрированных азотной HNO3 (65-68 % масс.) и соляной
HCl (32-35 % масс.) кислот, взятых в соотношении 1:3 по объёму (массовое соотношение, в пересчёте на чистые вещества.