Учитель химии: Шишкова Любовь Викторовна
Ново-Харитоновская СОШ №10 с УИОП
Раменский район Московской области
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Вывод формулы вещества(11 класс)
Содержание
- 1. Презентация по химии на тему Вывод формулы вещества(11 класс)
- 2. Слайд 2
- 3. Алгоритм решения расчётных задач Для вывода формулы
- 4. Задача №1. Установите молекулярную формулу углеводорода,
- 5. РешениеДано:ω(С)=82,75%ρ(СxHy)=2,59 г/лНайти: СxHy-формула
- 6. АлгоритмНайдём молярную массу через плотность: М=ρ·VmЧерез соотношение
- 7. Алгоритм4. Находим количество вещества атомов углерода и
- 8. Алгоритм5. Находим соотношение количества вещества атомов углерода
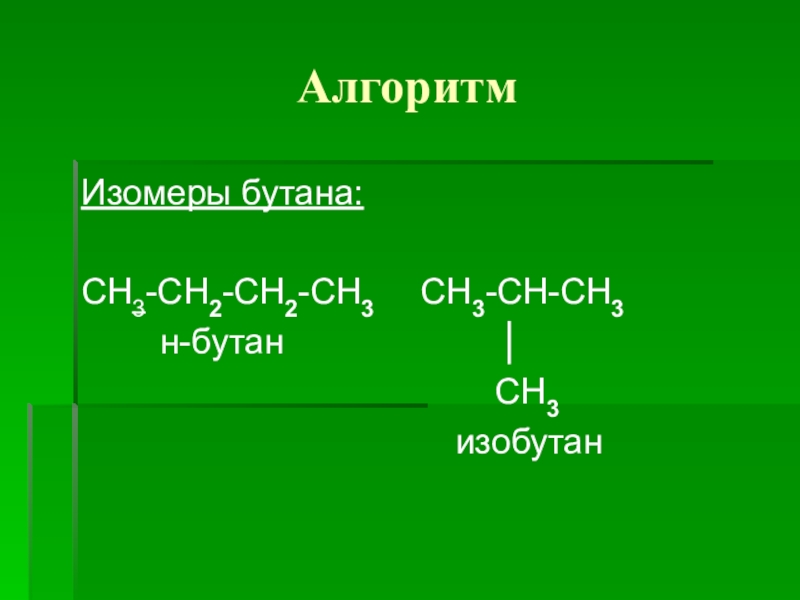
- 9. АлгоритмИзомеры бутана:СН3-СН2-СН2-СН3 СН3-СН-СН3
- 10. Задание в классе
- 11. Домашнее задание
Цель: Научиться выводить формулу вещества по его относительной плотности и массовым долям элементов.
Слайд 1Вывод формулы вещества по его относительной плотности и массовым долям элементов
(11 класс)
Слайд 2
Цель: Научиться выводить формулу вещества по его относительной плотности и массовым долям элементов.
Слайд 3Алгоритм решения расчётных задач
Для вывода формулы вещества надо знать:
Молярную массу вещества.
Она
задаётся в задачах:
В готовом виде
Через плотность(М=ρ·Vm)
3. Через DГ2(Г1);
М(Г1)= D(Г2)·М(Г2)
Через соотношение
m и V ; n=m/M ; n=V/Vm ;
m/M=V/Vm
В готовом виде
Через плотность(М=ρ·Vm)
3. Через DГ2(Г1);
М(Г1)= D(Г2)·М(Г2)
Через соотношение
m и V ; n=m/M ; n=V/Vm ;
m/M=V/Vm
Соотношение числа атомов элементов в молекуле.
Оно задаётся:
Указанием класса веществ
Через массовые доли элементов в веществе:
n=ω/Ar
3. Через мольные доли элементов в веществе:
ψ: С3Н8: ψ(С)=3; ψ(Н)=8
4. Через количества продуктов реакции, в которой участвует искомое вещество(продуктов сгорания).
Слайд 4Задача №1.
Установите молекулярную формулу углеводорода, в котором массовая доля
углерода равна 82,75%.Плотность углеводорода равна 2,59 г/л(н.у.). Составьте структурные формулы возможных изомеров и назовите их.
Слайд 6Алгоритм
Найдём молярную массу через плотность: М=ρ·Vm
Через соотношение n=m/M найдём массу
1моль вещества : m=M·n
Определим массы углерода и водорода в 1 моль вещества: m(C)=ω(C)·m(CxHy) m(H)=ω(H)·m(CxHy)
Определим массы углерода и водорода в 1 моль вещества: m(C)=ω(C)·m(CxHy) m(H)=ω(H)·m(CxHy)
Слайд 7Алгоритм
4. Находим количество вещества атомов углерода и водорода в 1 моль
вещества:
n(C)=m(C)/A(C)
n(H)=m(H)/A(H)
n(C)=m(C)/A(C)
n(H)=m(H)/A(H)
Слайд 8Алгоритм
5. Находим соотношение количества вещества атомов углерода и водорода:
n(C) : n(H)
Ответ: Формула вещества
Ответ: Формула вещества