- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Спирты
Содержание
- 1. Презентация по химии на тему Спирты
- 2. Химический диктант «Сравнительная характеристика углеводородов» ОТВЕТЫАлкины, алкадиеныАлкиныАлкеныАлканыАлкиныАлкеныАцетилен, алкиныАреныАлкеныАлканыАлканыАцетилен, пропанАлканыАлкеныАлканы
- 3. «Вино губит телесное здоровье людей, губит умственные
- 4. Спирты
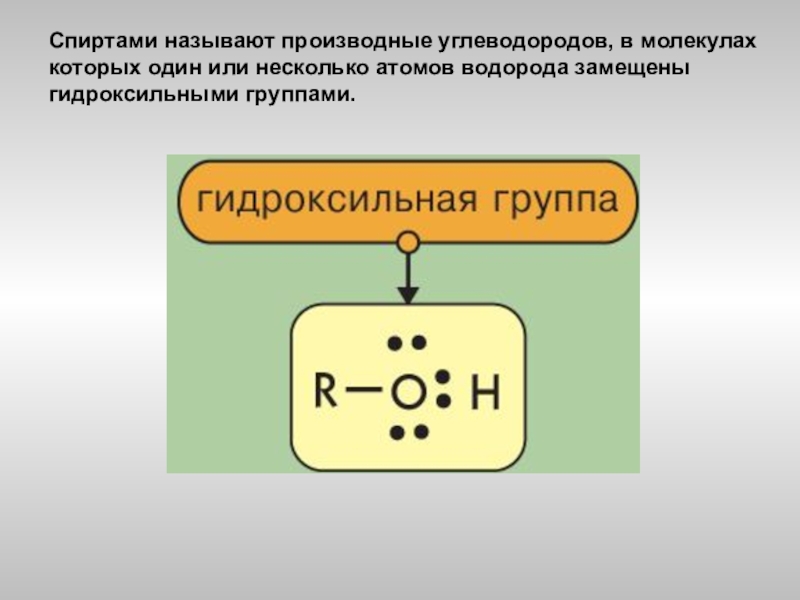
- 5. Спиртами называют производные углеводородов, в молекулах которых один или несколько атомов водорода замещены гидроксильными группами.
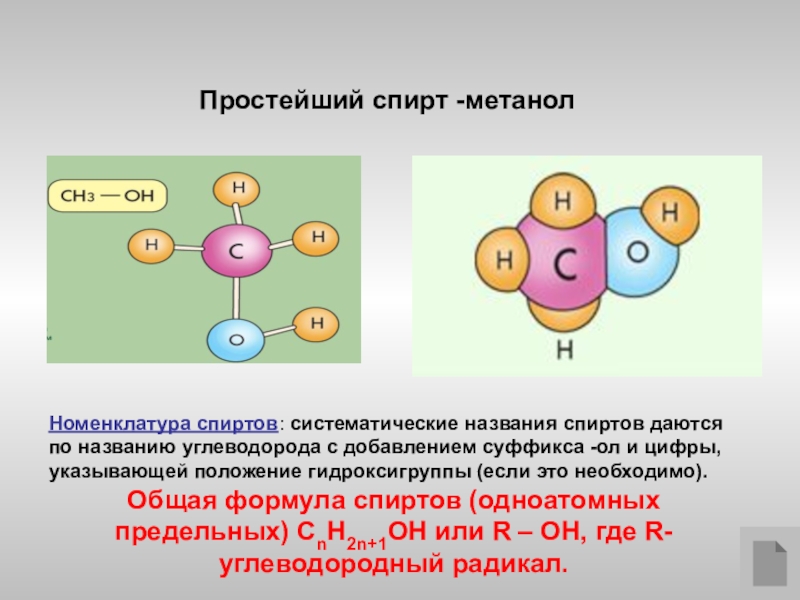
- 6. Простейший спирт -метанолНоменклатура спиртов: систематические названия спиртов
- 7. Номенклатура спиртов. К названию углеводорода добавляют количество
- 8. Классификация спиртов 1. По числу гидроксильных групп
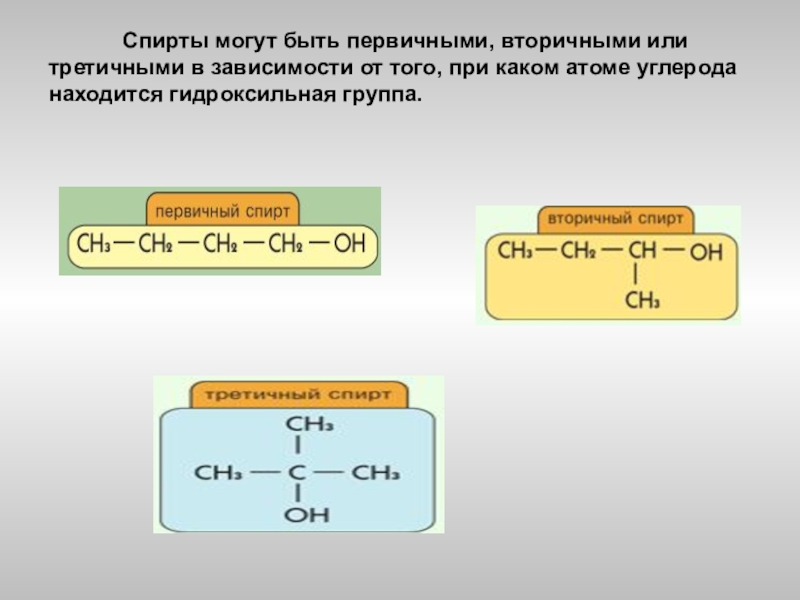
- 9. Спирты
- 10. Изомерия изомерия положения ОН - группы, (начиная
- 11. Физические свойства Первые представители, содержащие от одного
- 12. Следствием полярности связи О–Н и наличия неподеленных
- 13. Одноатомные спирты
- 14. Реакции замещения водорода функциональной группыРеакции замещения функциональной группыРеакции элиминированияРеакции окисленияРеакции этерификацииХимические свойства спиртов
- 15. Реакции замещения Одноатомные спирты реагируют с активными
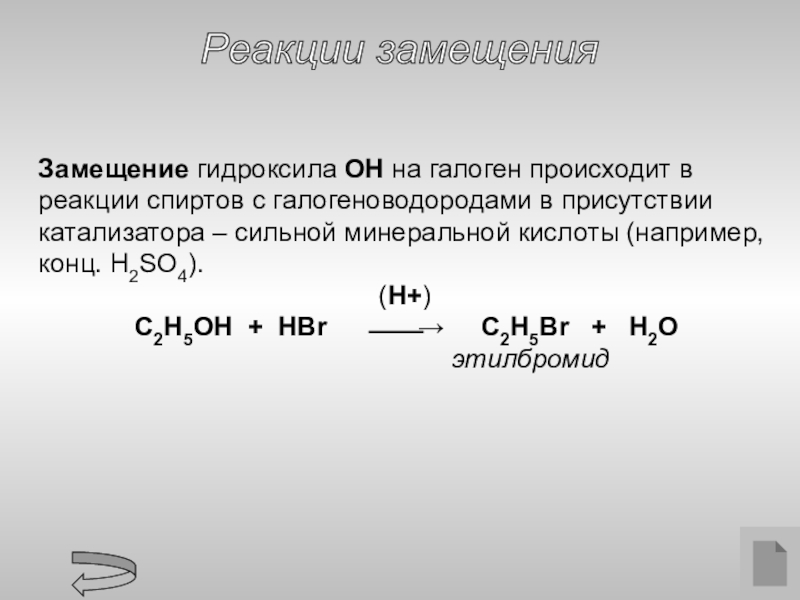
- 16. Реакции замещения Замещение гидроксила ОН на галоген
- 17. Реакции дегидратации Внутримолекулярная дегидратация спиртов с образованием
- 18. Реакции окисления При действии окислителей (KMnO4, K2Cr2O7+H2SO4,
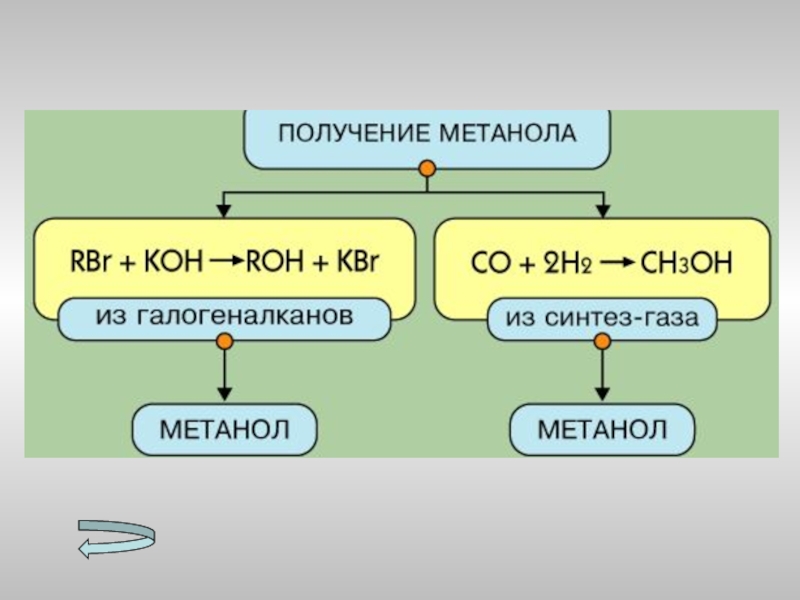
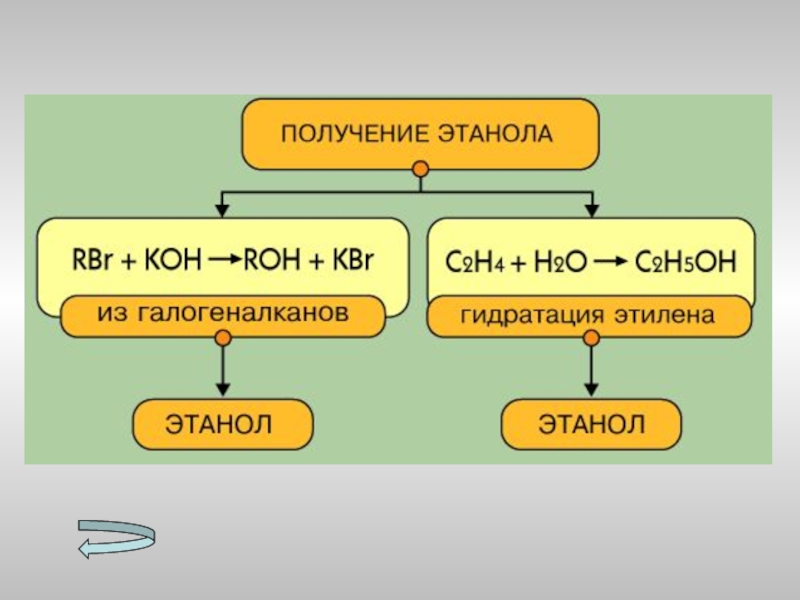
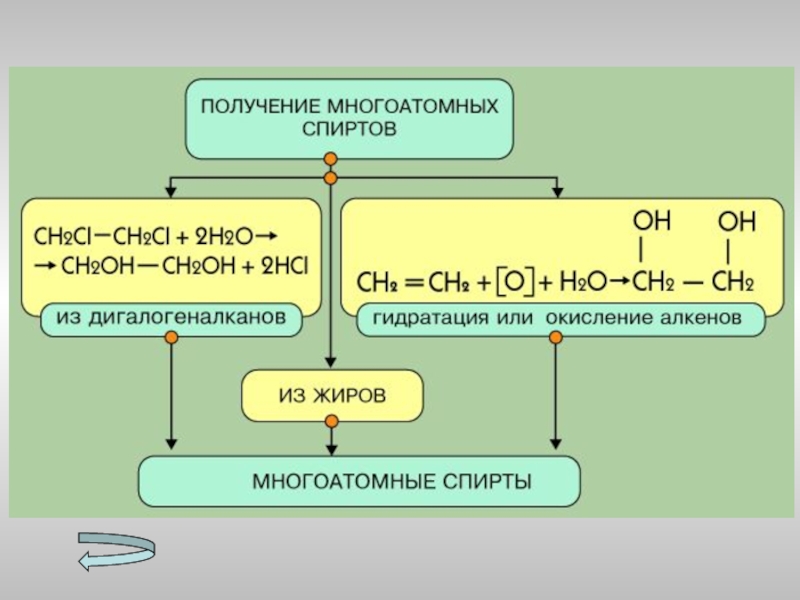
- 19. Получение спиртов МетанолаЭтанолаМногоатомных спиртов
- 20. Слайд 20
- 21. Слайд 21
- 22. Слайд 22
- 23. Применение спиртов Метанол CH3OH -производство формальдегида, муравьиной
- 24. Применение спиртов Этиленгликоль HOCH2-CH2OH - производство пластмасс;
- 25. Вопросы для контроля Какие вещества относят к
Слайд 1Химический диктант «Сравнительная характеристика углеводородов»
Общая формула этого класса веществ CnH2n –
Основной представитель этого класса ацетилен.
В молекулах этих углеводородов одна двойная связь.
Общая формула этого класса веществ CnH2n + 2.
В молекулах этих веществ имеется одна тройная связь.
Один из важнейших представителей этого класса – этилен.
Одно из веществ этого класса получают карбидным способом.
Основное химическое свойство этих веществ, вступать в реакции замещения.
Общая формула этих веществ CnH2n .
Основным представителем этого класса является метан.
Представители этого класса веществ имеют формулы: C2H6, C3H8, C4H10.
Вещество этого класса применяют при сварке и резке металлов.
При дегидрировании этого класса веществ получают алкины.
Представители этого класса веществ имеют формулы: C2H4, C3H6.
Какому классу не характерна реакция присоединения.
Слайд 2Химический диктант «Сравнительная характеристика углеводородов»
ОТВЕТЫ
Алкины, алкадиены
Алкины
Алкены
Алканы
Алкины
Алкены
Ацетилен, алкины
Арены
Алкены
Алканы
Алканы
Ацетилен, пропан
Алканы
Алкены
Алканы
Слайд 3«Вино губит
телесное здоровье людей, губит умственные способности, губит благосостояние семей
Лев Николаевич Толстой
Слайд 5Спиртами называют производные углеводородов, в молекулах которых один или несколько атомов
Слайд 6Простейший спирт -метанол
Номенклатура спиртов: систематические названия спиртов даются по названию углеводорода
Общая формула спиртов (одноатомных предельных) СnH2n+1OH или R – OH, где R- углеводородный радикал.
Слайд 7Номенклатура спиртов.
К названию углеводорода добавляют количество гидроксогрупп (префикс), затем –
Порядок построения названия:
1. Углеродная цепь нумеруется с конца к которому ближе находится группа –ОН.
2. Основная цепь содержит 7 атомов С, значит соответствующий УВ гептан.
3. Число групп – ОН равно 2, префикс – «ди».
4. Гидроксильные группы находятся при 2 и 3 атомах углерода, n = 2 и 4.
Слайд 8
Классификация спиртов
1. По числу гидроксильных групп спирты подразделяются на одноатомные
Современное название многоатомных спиртов - полиолы (диолы, триолы ит.д).
Примеры:
двухатомный спирт – этиленгликоль (этандиол)
HO–СH2–CH2–OH
трехатомный спирт – глицерин (пропантриол-1,2,3)
HO–СH2–СН(ОН)–CH2–OH
2. По строению радикалов, связанных с атомом кислорода, различают
спирты:
предельные, или алканолы (например, СH3CH2–OH)
непредельные, или алкенолы (CH2=CH–CH2–OH)
ароматические (C6H5CH2–OH) (фенилметанол).
Слайд 9 Спирты могут быть первичными, вторичными
Слайд 10
Изомерия
изомерия положения ОН - группы, (начиная с С3) ;
углеродного
межклассовая изомерия с простыми эфирами.
Например, одну и ту же молекулярную формулу
С2H6O имеют:
СН3CH2–OH и CH3–O–CH3
этиловый спирт диметиловый эфир
Слайд 11
Физические свойства
Первые представители, содержащие от одного до 11-ти атомов углерода,
Высшие спирты (начиная с C12H25OH) при комнатной температуре – твердые вещества.
Низшие спирты имеют характерный алкогольный запах и жгучий вкус, хорошо растворимы в воде. По мере увеличения углеводородного радикала растворимость в воде уменьшается.
Следовательно, возможно образование водородных связей между молекулами спирта и молекулами спирта и воды.
Слайд 12Следствием полярности связи О–Н и наличия неподеленных пар электронов на атоме
R R R
/ / /
H − O:δ- ⋅ ⋅ ⋅ Hδ+ − O:δ- ⋅ ⋅ ⋅ Hδ+ −O:
Это объясняет, почему даже низшие спирты - жидкости с относительно высокой температурой кипения (т.кип. метанола +64,5 °С).
Физические свойства
Слайд 14Реакции замещения водорода функциональной группы
Реакции замещения функциональной группы
Реакции элиминирования
Реакции окисления
Реакции этерификации
Химические
Слайд 15Реакции замещения
Одноатомные спирты реагируют с активными металлами (Na, K, Mg,
2R–OH + 2K → 2RO– K + H2
2C2H5OH + 2Na → 2C2H5O– Na + H2
этилат натрия
Слайд 16
Реакции замещения
Замещение гидроксила ОН на галоген происходит в реакции спиртов
(H+)
C2H5OH + HBr ⎯⎯→ C2H5Br + H2O
этилбромид
Слайд 17Реакции дегидратации
Внутримолекулярная дегидратация спиртов с образованием алкенов
идет в присутствии
выше 140 °С.
Например:
H2SO4
CH3−CH−CH2 ⎯⎯⎯→ CH3−CH=CH2 + H2O
| | t > 140°C
H OH
H2SO4
CH3−CH−CH−CH3 ⎯⎯⎯→ CH3−CH=CH−CH3 + H2O
| | t > 140°C бутен-2
H OH
Межмолекулярная дегидратация с образованием простых эфиров (при нагревании ниже 140 °С):
C2H5OH + HOC2H5 → C2H5-O-C2H5 + H2O
Слайд 18
Реакции окисления
При действии окислителей (KMnO4, K2Cr2O7+H2SO4, O2+катализатор)
группа >СH–О–Н превращается в
а гидроксисоединение – в карбонильное соединение.
Первичные спирты при окислении образуют альдегиды, которые затем
легко окисляются до карбоновых кислот:
[O] [O]
R–СН2–OH ⎯⎯→ R–СН=O ⎯⎯→ R–СOOH
-H2O альдегид карбоновая кислота
Например, окисление этилового спирта K2Cr2O7 / H2SO4 :
3C2H5OH + 2K2Cr2O7 + 8H2SO4 → 3CH3COOH + 2Cr2(SO4)3 + 2K2SO4 + 11H2O
Слайд 23
Применение спиртов
Метанол CH3OH
-производство формальдегида, муравьиной кислоты;
- растворитель.
Этанол С2Н5ОН
- производство ацетальдегида, уксусной кислоты, бутадиена,
простых и сложных эфиров;
- растворитель для красителей, лекарственных и парфюмерных средств;
- производство ликеро-водочных изделий;
- дезинфицирующее средство в медицине;
- горючее для двигателей, добавка к моторным топливам.
Слайд 24Применение спиртов
Этиленгликоль HOCH2-CH2OH
- производство пластмасс;
- компонент антифризов;
Глицерин HOCH2-CH(OH)-CH2OH
- фармацевтическая и парфюмерная промышленность;
- смягчитель кожи и тканей;
- производство взрывчатых веществ.
Слайд 25Вопросы для контроля
Какие вещества относят к спиртам?
На какие группы классифицируют
Назовите виды изомерии у предельных одноатомных спиртов.
Какую роль оказывают водородные связи на физические свойства спиртов?
Какие химические свойства характерны для спиртов?
Перечислите способы получения спиртов.
Назовите основные области применения спиртов.