- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Спирты
Содержание
- 1. Презентация по химии на тему Спирты
- 2. Спирты Спирты – производные углеводородов, в которых
- 3. Строение Строение самого простого спирта — метилового
- 4. Номенклатура При образовании названий спиртов к названию
- 5. Например :1. Углеродная цепь нумеруется с конца
- 6. Классификация спиртов По числу гидроксильных групп спирты
- 7. Классификация спиртов2. По строению радикалов , связанных
- 8. Классификация спиртов3. По характеру атома углерода, с которым связана гидроксильная группа:Первичные: R-CH2-OH Вторичные: R2СН-ОН Третичные R2C-OH
- 9. Получение спиртовЩелочной гидролиз галогеналканов (лабораторный способ): C2H5Cl
- 10. Изомерия Виды изомерииПоложение функциональной группы Углеродного скелета Межклассовая
- 11. Изомерия Изомерия положения ОН-группы (начиная с С3)
- 12. Изомерия Межклассовая изомерия с простыми эфирами этиловый спирт СН3CH2–OH и диметиловый эфир CH3–O–CH3
- 13. Физические свойства Температуры плавления и кипения спиртов,
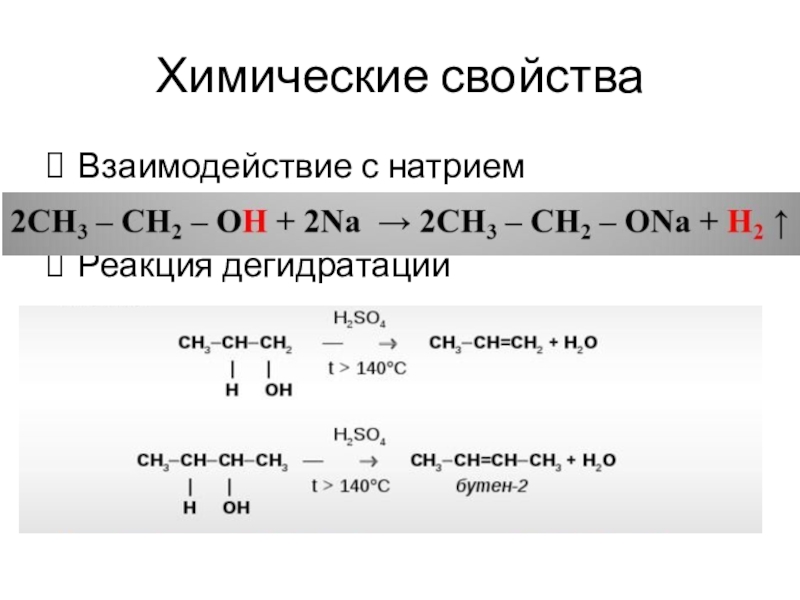
- 14. Химические свойства Взаимодействие с натрием Реакция дегидратации
- 15. Химические свойства Взаимодействие спиртов с галогеноводородами. Замещение
- 16. Свойства метанолаПри окислении метанола кислородом в присутствии
- 17. Свойства этанола Этанол легко воспламеняется, горит слабо
- 18. Свойства этанолаДегидрированиеCH3-CH2-OH → CH3-C(O)H + H2↑ (катализатор
- 19. Свойства глицерина Глицерин имеет и специфические свойства,
- 20. Свойства глицерина Важнейшей в практическом отношении является реакция нитрования глицерина, в результате которой образуется тринитроглицерин C3H5(ONO2)3:
- 21. Свойства глицерина Глицерин вступает в реакцию с
- 22. Применение Дезинфицирующие средства Лекарственные препаратыБензин Синтетический каучукРастворитель Алкогольные напитки Парфюмерные средства
- 23. Спасибо за сотрудничество!
Спирты Спирты – производные углеводородов, в которых один или несколько атомов водорода заменены на функциональную группу -OH (гидроксил)Общая формула CnH2n + 1 OH или R – OH, где R - углеводородный радикал СН3ОН - метанол (метиловый
Слайд 2Спирты
Спирты – производные углеводородов, в которых один или несколько атомов
водорода заменены на функциональную группу -OH (гидроксил)
Общая формула CnH2n + 1 OH или R – OH,
где R - углеводородный радикал
СН3ОН - метанол (метиловый спирт)
СН3СН2ОН - этанол (этиловый спирт)
Общая формула CnH2n + 1 OH или R – OH,
где R - углеводородный радикал
СН3ОН - метанол (метиловый спирт)
СН3СН2ОН - этанол (этиловый спирт)
Слайд 3Строение
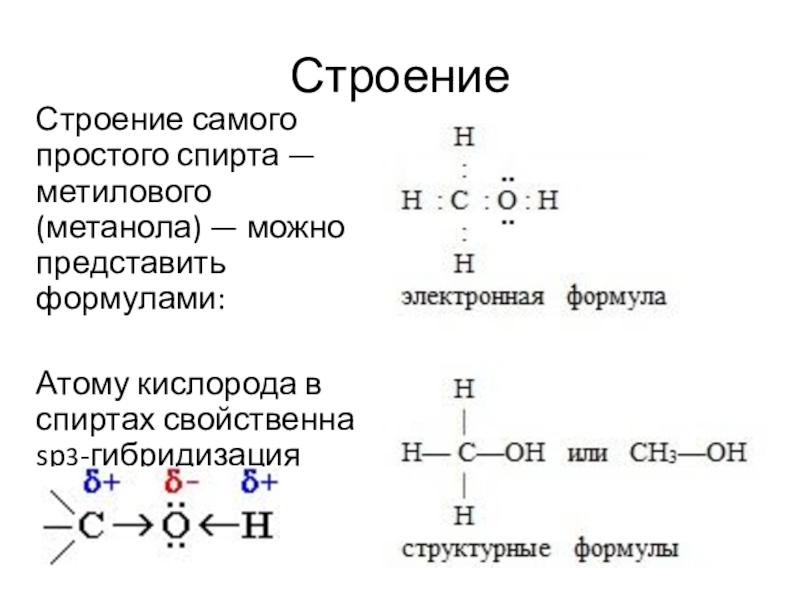
Строение самого простого спирта — метилового (метанола) — можно представить
формулами:
Атому кислорода в спиртах свойственна sp3-гибридизация
Атому кислорода в спиртах свойственна sp3-гибридизация
Слайд 4Номенклатура
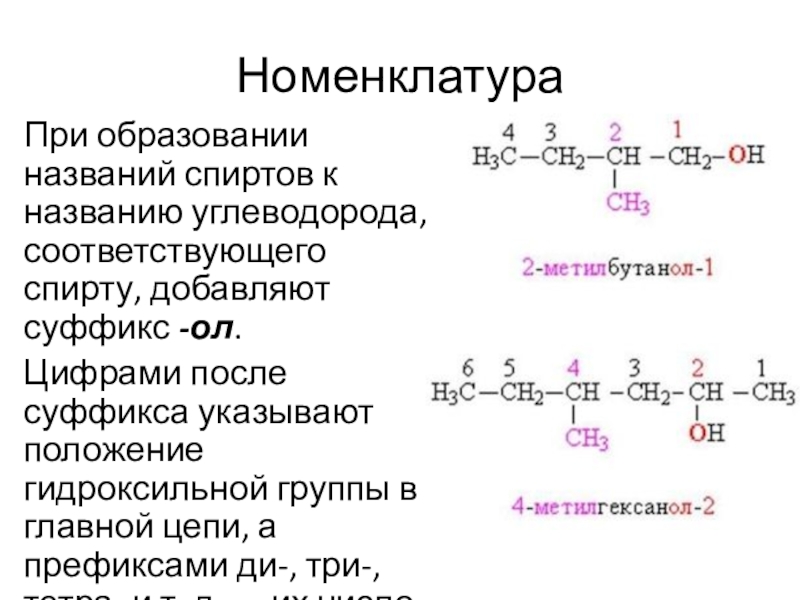
При образовании названий спиртов к названию углеводорода, соответствующего спирту, добавляют
суффикс -ол.
Цифрами после суффикса указывают положение гидроксильной группы в главной цепи, а префиксами ди-, три-, тетра- и т. д. — их число
Цифрами после суффикса указывают положение гидроксильной группы в главной цепи, а префиксами ди-, три-, тетра- и т. д. — их число
Слайд 5Например :
1. Углеродная цепь нумеруется с конца к которому ближе находится
группа –ОН.
2. Основная цепь содержит 7 атомов С, значит соответствующий УВ гептан.
3. Число групп –ОН равно 2, префикс – «ди».
4. Гидроксильные группы находятся при 2 и 4 атомах углерода
Название спирта гептандиол-2,4
2. Основная цепь содержит 7 атомов С, значит соответствующий УВ гептан.
3. Число групп –ОН равно 2, префикс – «ди».
4. Гидроксильные группы находятся при 2 и 4 атомах углерода
Название спирта гептандиол-2,4
Слайд 6Классификация спиртов
По числу гидроксильных групп спирты подразделяются на одноатомные (одна
группа -ОН) и многоатомные (две и более групп -ОН).
Слайд 7Классификация спиртов
2. По строению радикалов , связанных с атомом кислорода, различают
спирты:
Предельные (насыщенные) спирты:
CH3-CH2-OH (этанол)
Непредельные (ненасыщенные) спирты:
Н2С=СН—CН2OН (аллиловый спирт)
Ароматические спирты: (бензиловый спирт)
Предельные (насыщенные) спирты:
CH3-CH2-OH (этанол)
Непредельные (ненасыщенные) спирты:
Н2С=СН—CН2OН (аллиловый спирт)
Ароматические спирты: (бензиловый спирт)
Слайд 8Классификация спиртов
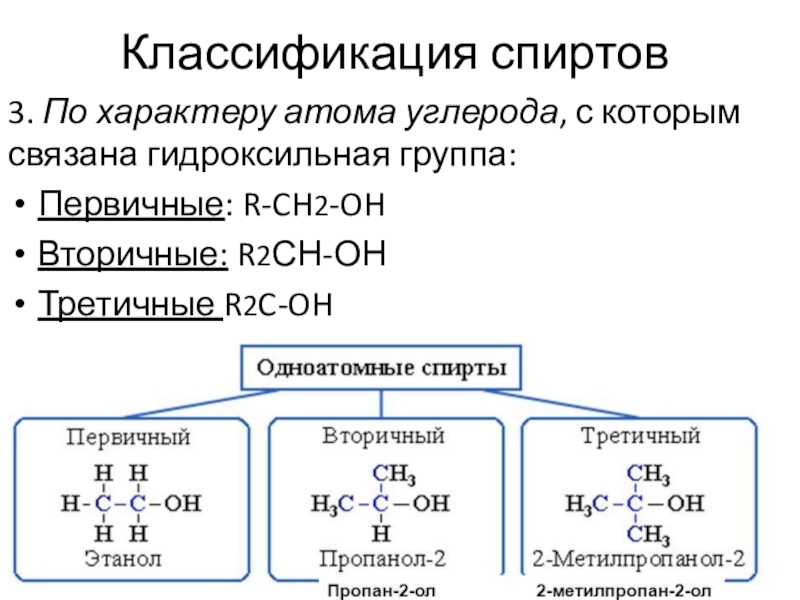
3. По характеру атома углерода, с которым связана гидроксильная группа:
Первичные:
R-CH2-OH
Вторичные: R2СН-ОН
Третичные R2C-OH
Вторичные: R2СН-ОН
Третичные R2C-OH
Слайд 9Получение спиртов
Щелочной гидролиз галогеналканов (лабораторный способ): C2H5Cl + NaOH C2H5OH + NaCl.
Гидратация
алкенов: C2H4 + H2O C2H5OH.
Брожение глюкозы : C6H12O6 2C2H5OH + 2CO2.
Синтез метанола: CO + 2H2 CH3OH
Брожение глюкозы : C6H12O6 2C2H5OH + 2CO2.
Синтез метанола: CO + 2H2 CH3OH
Слайд 11Изомерия
Изомерия положения ОН-группы (начиная с С3)
Углеродного скелета (начиная с
С4)
Например, изомеры углеродного
скелета для C4H9OH:
Например, изомеры углеродного
скелета для C4H9OH:
Слайд 12Изомерия
Межклассовая изомерия с простыми эфирами
этиловый спирт СН3CH2–OH и диметиловый эфир CH3–O–CH3
Слайд 13Физические свойства
Температуры плавления и кипения спиртов, так же как и
углеводородов, увеличиваются с ростом числа атомов углерода в молекуле
Спирты растворимы в воде гораздо лучше углеводородов. Метиловый и этиловый спирты смешиваются с водой в любых соотношениях
Низшие спирты имеют характерный алкогольный запах и жгучий вкус.
Например, кошачий запах связан с тем, что в этот запах основным компонентом входит изопропиловый спирт.
Низшие и средние члены ряда предельных одноатомных спиртов, содержащие от одного до одиннадцати атомов углерода, — жидкости.
Высшие спирты (начиная с С12Н25ОН) при комнатной температуре — твердые вещества.
Спирты растворимы в воде гораздо лучше углеводородов. Метиловый и этиловый спирты смешиваются с водой в любых соотношениях
Низшие спирты имеют характерный алкогольный запах и жгучий вкус.
Например, кошачий запах связан с тем, что в этот запах основным компонентом входит изопропиловый спирт.
Низшие и средние члены ряда предельных одноатомных спиртов, содержащие от одного до одиннадцати атомов углерода, — жидкости.
Высшие спирты (начиная с С12Н25ОН) при комнатной температуре — твердые вещества.
Слайд 15Химические свойства
Взаимодействие спиртов с галогеноводородами. Замещение гидроксильной группы на галоген
приводит к образованию галогеналканов.
С2Н5ОН + НВг <-> С2Н5Вг + Н2O
Горение: C2H5OH + 3O2 2CO2 +3H2O + Q
Реакции с щелочными и щелочноземельными металлами ("кислотные" свойства):
2Na + 2H—O—H 2NaOH + H2
Окисление CH3CH2OH + CuO CH3—CHO + Cu + H2O
С2Н5ОН + НВг <-> С2Н5Вг + Н2O
Горение: C2H5OH + 3O2 2CO2 +3H2O + Q
Реакции с щелочными и щелочноземельными металлами ("кислотные" свойства):
2Na + 2H—O—H 2NaOH + H2
Окисление CH3CH2OH + CuO CH3—CHO + Cu + H2O
Слайд 16Свойства метанола
При окислении метанола кислородом в присутствии катализатора образуется формальдегид:
СНзОН +
0,5СО2 НСНО + Н2О
Действие щелочей
2СНзОН + 2Na 2CH3ONa + 2Н2
Вода омыляет его до метанола и щелочи:
СН3ОNa + Н2О СНзОН + NaOH
Действие щелочей
2СНзОН + 2Na 2CH3ONa + 2Н2
Вода омыляет его до метанола и щелочи:
СН3ОNa + Н2О СНзОН + NaOH
Слайд 17Свойства этанола
Этанол легко воспламеняется, горит слабо светящимся голубоватым пламенем: С2Н5ОН
+ 3О2 2СО2 + 3Н2О
Взаимодействие с активными металлами
2C2H5OH + 2Na → 2C2H5ONa + H2↑
Взаимодействие с галогеноводородами
C2H5OH + HCl → C2H5Cl + H2O (ZnCl2, t ).
Взаимодействие с тригалогенидами фосфора
3C2H5OH + PBr3→ 3C2H5Br + H3PO3.
Взаимодействие с активными металлами
2C2H5OH + 2Na → 2C2H5ONa + H2↑
Взаимодействие с галогеноводородами
C2H5OH + HCl → C2H5Cl + H2O (ZnCl2, t ).
Взаимодействие с тригалогенидами фосфора
3C2H5OH + PBr3→ 3C2H5Br + H3PO3.
Слайд 18Свойства этанола
Дегидрирование
CH3-CH2-OH → CH3-C(O)H + H2↑ (катализатор = Cu, температура )
Окисление
CH3-CH2-OH
+ 2[O] → CH3-COOH + H2O (катализатор температура )
Внутримолекулярная дегидратация
CH3-CH2-OH → CH2=CH2 + H2O (Al2O3, температура)
Внутримолекулярная дегидратация
CH3-CH2-OH → CH2=CH2 + H2O (Al2O3, температура)
Слайд 19Свойства глицерина
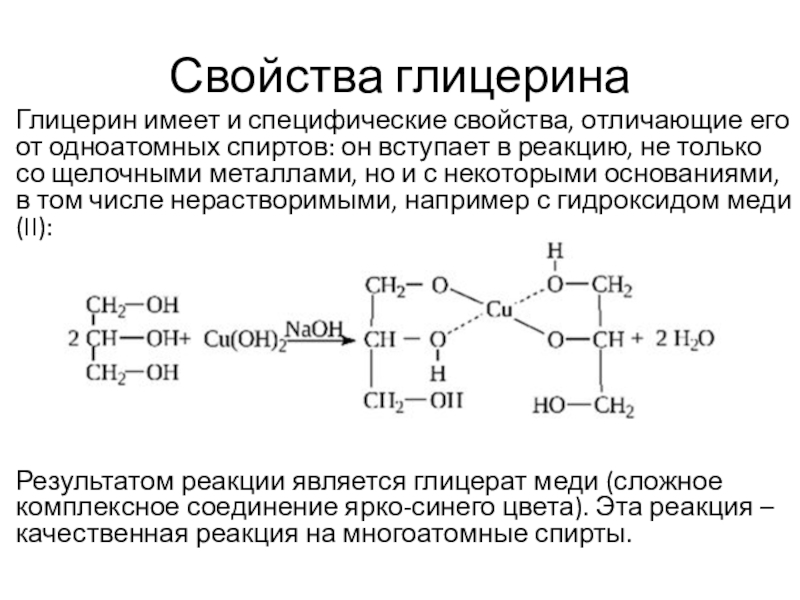
Глицерин имеет и специфические свойства, отличающие его от одноатомных
спиртов: он вступает в реакцию, не только со щелочными металлами, но и с некоторыми основаниями, в том числе нерастворимыми, например с гидроксидом меди (II):
Результатом реакции является глицерат меди (сложное комплексное соединение ярко-синего цвета). Эта реакция – качественная реакция на многоатомные спирты.
Результатом реакции является глицерат меди (сложное комплексное соединение ярко-синего цвета). Эта реакция – качественная реакция на многоатомные спирты.
Слайд 20Свойства глицерина
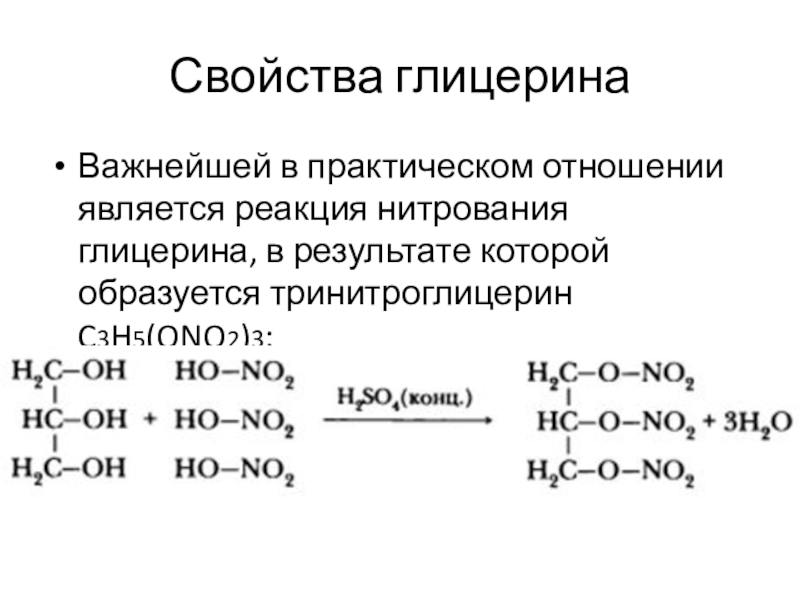
Важнейшей в практическом отношении является реакция нитрования глицерина, в
результате которой образуется тринитроглицерин C3H5(ONO2)3:
Слайд 21Свойства глицерина
Глицерин вступает в реакцию с галогеноводнямы:
CH2OH-CHOH-CH2OH + HCl →
CH2OH-CHOH-CH2Cl + H2O и с азотистой кислотой.
Он горит с образованием CO2 и воды
Он горит с образованием CO2 и воды












![Презентация по химии на тему Спирты Свойства этанолаДегидрированиеCH3-CH2-OH → CH3-C(O)H + H2↑ (катализатор = Cu, температура )ОкислениеCH3-CH2-OH Свойства этанолаДегидрированиеCH3-CH2-OH → CH3-C(O)H + H2↑ (катализатор = Cu, температура )ОкислениеCH3-CH2-OH + 2[O] → CH3-COOH + H2O](/img/tmb/8/714261/b29f6308094e69b33a134487de1f2449-800x.jpg)