- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Составление формул бинарных соединений
Содержание
- 1. Презентация по химии на тему Составление формул бинарных соединений
- 2. «Составление формул бинарных соединений»
- 3. Выполним тест1.Степень окисления - это величинаа) постояннаяб)
- 4. Проверка теста1.Степень окисления - это величинав) постоянная
- 5. Слайд 5
- 6. H2O
- 7. CO2
- 8. Al2O3
- 9. CaO
- 10. Алгоритм составления формулы бинарного соединения1.На первом месте
- 11. Составить формулы между элементамиCa и Сl, AL и O.Проверка:CaCL2 AL2O3
- 12. Правила составления названия бинарных веществ. 1.Названия состоят
- 13. Составьте формулы веществ состоящих из Fe+3 и
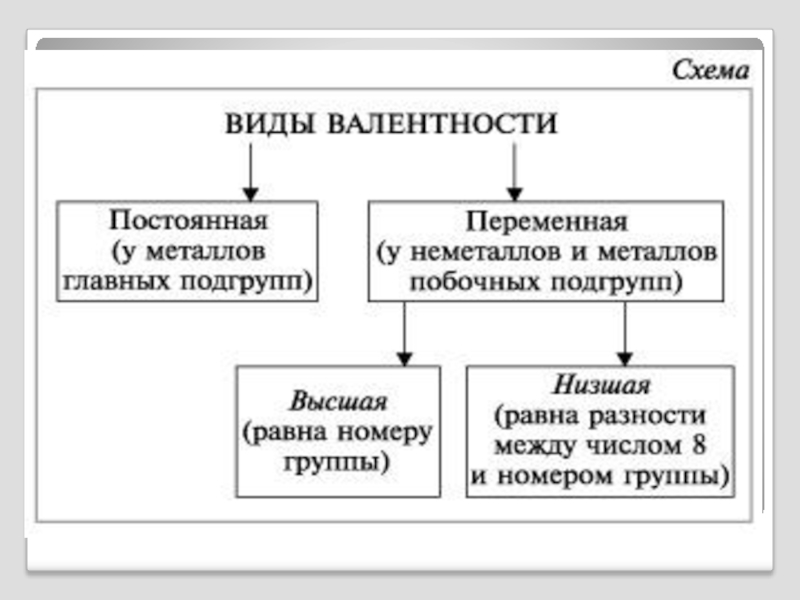
- 14. Валентность – это число связей, которые атом
- 15. Таблица постоянных валентностей. Валентности
- 16. Слайд 16
- 17. 1. Запиши рядом знаки химических элементов, которые
- 18. 2. Над знаками химических элементов поставь их
- 19. 3. Определи Н.О.К. чисел выражающих валентность этих
- 20. 4. Раздели Н.О.К. на валентность каждого элемента. Запиши полученный индекс.Пример: Составить химическую формулу оксида бора.BOIIIII23623Формула составлена66IIIII::==
- 21. Составьте формулу фосфида кальцияСа3Р2Составьте формулу оксида свинца (IV)PbO2
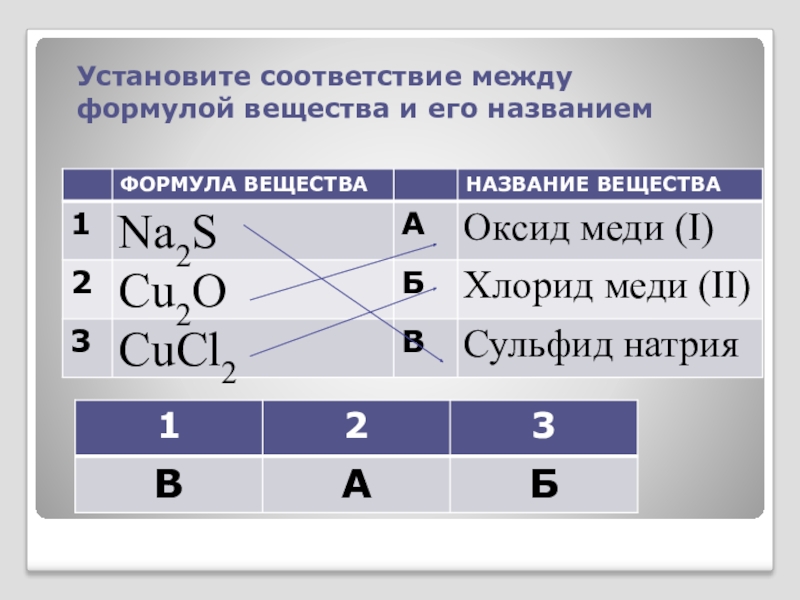
- 22. Установите соответствие между формулой вещества и его названием
- 23. Домашнее задание:На «3»
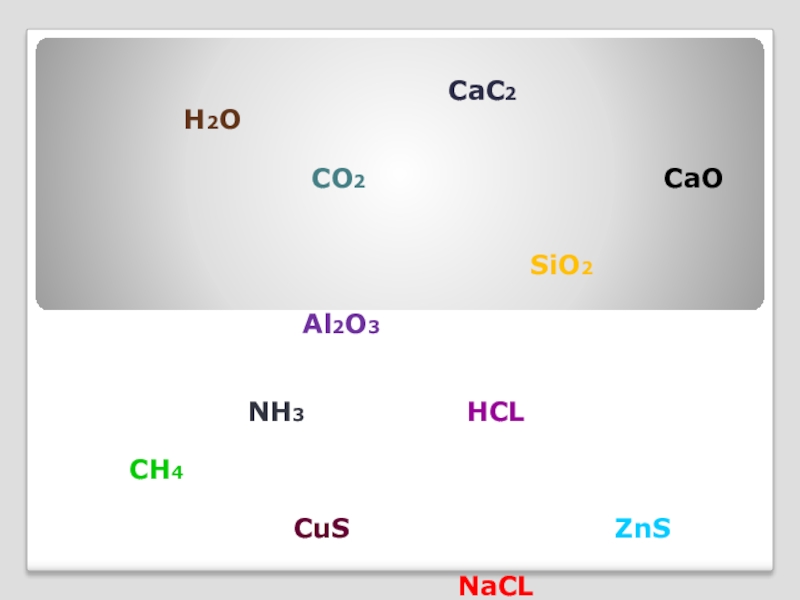
Слайд 1 SO3
HCL
H2O H2SO4 CO2
«Химические формулы говорят целую историю вещества».
Д.И.Менделеев
NH3 NaOH Fe2O3
SiO2 Na2CO3
Слайд 3Выполним тест
1.Степень окисления - это величина
а) постоянная
б) переменная
в) постоянная и переменная
2.
а) номеру группы, т.е. 5,
б) нулю,
в) трем.
3. Степень окисления хлора равна -1 в:
а) Cl2O3,
б) PCl5,
в) Cl2.
4.В каком соединении степень окисления определена не верно:
а) Mg+2 O-2
б) Р2+2 O5-3
в) H+1 CL-1
5.Степени окисления марганца в соединениях MnO, MnO2, Mn2O7 соответственно равны:
а)+1,+2,+7
б)+2,+4,+7
в)+1,+2,+2
Слайд 4Проверка теста
1.Степень окисления - это величина
в) постоянная и переменная
2. Высшая степень
а) номеру группы, т.е. 5,
3. Степень окисления хлора равна -1 в:
б) PCl5,
4.В каком соединении степень окисления определена не верно:
б) P2+2 O5-3
5.Степени окисления марганца в соединениях MnO, MnO2, Mn2O7 соответственно равны:
б)+2,+4,+7
Слайд 10Алгоритм составления формулы бинарного соединения
1.На первом месте пишется элемент с меньшей
П-р: AL S
2.Элемент написанный на первом месте имеет положительный заряд, а на втором отрицательный.Указать для каждого элемента степень окисления.
П-р: AL+3S-2
3.Найти наименьшее общее кратное для значений степеней окисления.
П-р: НОК: 3х2=6
4.Разделить наименьшее общее кратное на значение степени окисления и полученные индексы приписать внизу справа после символа соответствующего элемента.
П-р: AL 6:3=2
S 6:2=3
5.Проверка. Суммарное значение степеней окисления равно 0.
AL2S3
+3х2+(-2)х3=6
Слайд 12Правила составления названия бинарных веществ.
1.Названия состоят из двух слов.
2.Первое слово
3.Второе слово обозначает электроположительную часть – металл или менее электроотрицательный элемент, его название в родительном падеже.
AL2S3 - сульфид алюминия
CaCl2- хлорид кальция
AL2O3 – оксид алюминия
Запомнить!
ЭxHy - гидриды
ЭxOy - оксиды
ЭxSy -сульфиды
ЭxCly -хлориды
ЭxBry -бромиды
ЭxFy - фториды
ЭxPy- фосфиды
ЭxNy -нитриды
ЭxIy –йодиды
ЭxCy -карбиды
ЭxSiy -силициды
Слайд 13
Составьте формулы веществ состоящих из
Fe+3 и Cl-, Fe+2 и Cl-.
Проверка:
FeCl3
FeCl2 - хлорид железа (II)
Слайд 14Валентность – это число связей, которые атом образует с другими атомами.
Валентность
I I I II III I IV I
НCl H2O NH3 CH4
Слайд 15Таблица постоянных валентностей.
Валентности Элементы
I
II O, Be, Mg, Ca, Sr, Ba, Zn, Cd
III B, Al, Ga, In
Слайд 171. Запиши рядом знаки химических элементов, которые входят в состав вещества.
Пример:
B
O
Оксиды - это сложные вещества, которые состоят из двух элементов один из которых кислород.
Первый пункт выполнили переходим ко второму
Слайд 182. Над знаками химических элементов поставь их валентность.
Пример: Составить химическую формулу
B
O
III
II
Второй пункт выполнили переходим к третьему
Слайд 193. Определи Н.О.К. чисел выражающих валентность этих элементов. Запиши Н.О.К. в квадратике
Пример: Составить химическую формулу оксида бора.
B
O
III
II
6
Третий пункт выполнили переходим ко четвертому
Н.О.К. (наименьшее общее кратное) – это число, которое делится на исходные числа без остатка.
Слайд 204. Раздели Н.О.К. на валентность каждого элемента.
Запиши полученный индекс.
Пример: Составить химическую
B
O
III
II
2
3
6
2
3
Формула составлена
6
6
III
II
:
:
=
=
Слайд 23
Домашнее задание:
На «3» - §17,упр.2
На «4» -
На «5» - §17,упр.2,3 и 5
Спасибо за внимание!!!