- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Сера и ее свойства. Аллотропия серы (9 класс).
Содержание
- 1. Презентация по химии на тему: Сера и ее свойства. Аллотропия серы (9 класс).
- 2. ОТКРЫТИЕ
- 3. Сера в природеСера широко распространена в
- 4. Самородная сера, серный колчедан FeS2, медный колчедан
- 5. СЕРА
- 6. ФИЗИЧЕСКИЕ СВОЙСТВА СЕРЫ Сера – твердое кристаллическое
- 7. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ СЕРЫ Сера ромбическаяСера пластическая
- 8. Видеофрагмент
- 9. Физминутка «Дождь».В классе три группы. Первая группа
- 10. ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ S Реагирует с металлами
- 11. Видеофрагменты.
- 12. ПРИМЕНЕНИЕ СЕРЫ S
- 13. Домашнее задание § 9,10, выполнить упр. 3-6, задача 2, стр.31
Слайд 1Сера и ее свойства.
Аллотропия серы.
Презентацию подготовил учитель химии
ГБОУ СОШ
Слайд 2
ОТКРЫТИЕ СЕРЫ
Сера (англ. Sulfur,
Слайд 3 Сера в природе
Сера широко распространена в природе. Она составляет 0,05%
Сера часто встречается в виде соединений с другими элементами. Важнейшими ее природными соединениями являются сульфиды металлов: FeS2– железный колчедан, или пирит; HgS – киноварь и др., а также соли серной кислоты (кристаллогидраты):CaSO4*2H2O – гипс,Na2SO4*ּ10H2O– глауберова соль,MgSO4*ּ7H2O– горькая соль и др.
Слайд 4
Самородная сера, серный колчедан FeS2, медный колчедан CuFeS2, свинцовый блеск PbS
Ангидрит CaSO4, гипс CaSO4∙2H2O и гипс пластинчатый
СОЕДИНЕНИЯ СЕРЫ
Слайд 5СЕРА
nº=16
ē=16
Z=+16
Степени окисления серы: −2 (окислительные свойства); 0;
+2, +4, +6 (восстановительные свойства).
Сера входит в главную подгруппу шестой группы, третий период (малый).
Сера – неметалл
1s22s22p63s23p4
Слайд 6ФИЗИЧЕСКИЕ СВОЙСТВА СЕРЫ
Сера – твердое кристаллическое вещество желтого цвета, не
Не растворяется в воде. Хорошо растворяется в сероуглероде, толуоле.
Плохо проводит тепло и
электричество.
Она типичный
диэлектрик (изолятор)
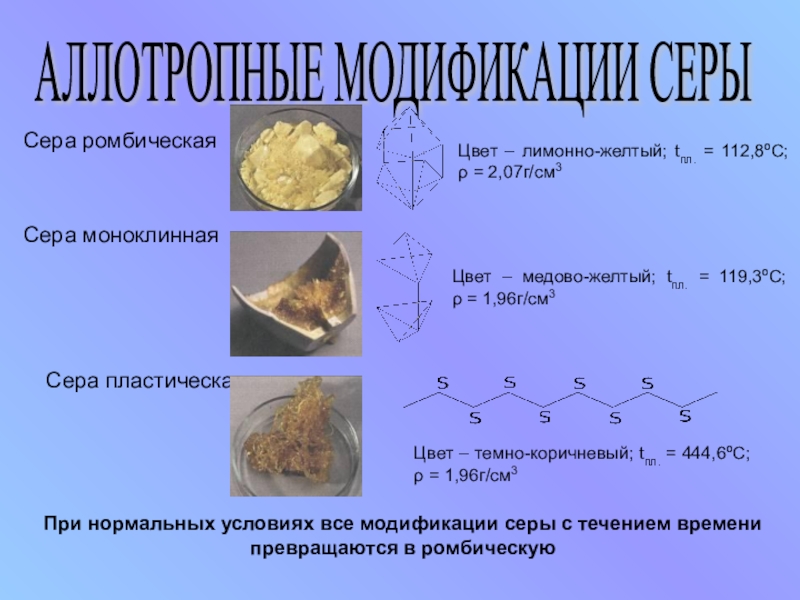
Слайд 7АЛЛОТРОПНЫЕ МОДИФИКАЦИИ СЕРЫ
Сера ромбическая
Сера пластическая
Сера моноклинная
Цвет – лимонно-желтый;
Цвет – медово-желтый; tпл. = 119,3ºС; ρ = 1,96г/см3
Цвет – темно-коричневый; tпл. = 444,6ºС; ρ = 1,96г/см3
При нормальных условиях все модификации серы с течением времени превращаются в ромбическую
Слайд 9Физминутка «Дождь».
В классе три группы. Первая группа по сигналу учителя начинает
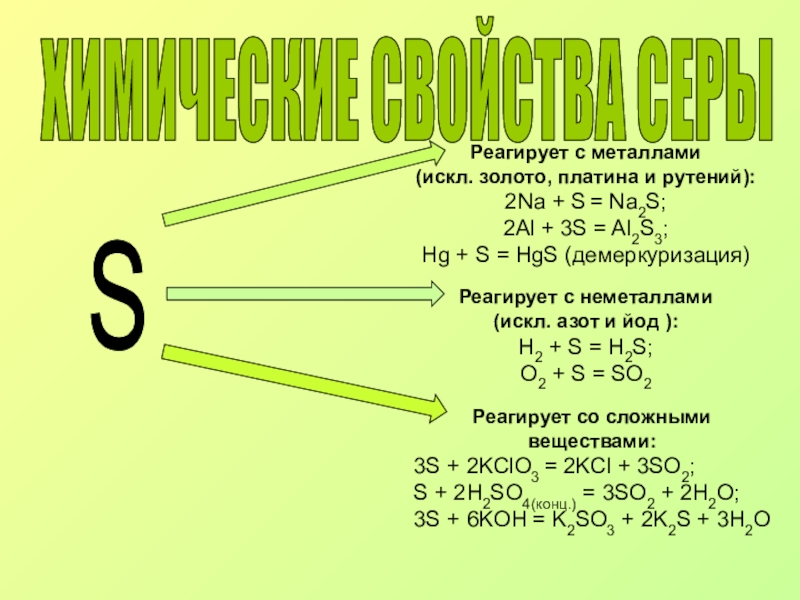
Слайд 10ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ
S
Реагирует с металлами
(искл. золото, платина и
2Na + S = Na2S;
2Al + 3S = Al2S3;
Нg + S = HgS (демеркуризация)
Реагирует с неметаллами (искл. азот и йод ):
H2 + S = H2S;
O2 + S = SO2
Реагирует со сложными веществами:
3S + 2KClO3 = 2KCl + 3SO2;
S + 2H2SO4(конц.) = 3SO2 + 2H2O;
3S + 6KOH = K2SO3 + 2K2S + 3H2O