- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Обобщающий урок Атомы химических элементов
Содержание
- 1. Презентация по химии на тему Обобщающий урок Атомы химических элементов
- 2. « АТОМЫ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ»ОБОБЩАЮЩИЙ УРОК
- 3. Цели: Повторить, обобщить и систематизировать сведения
- 4. КОМАНДА«АТОМ» КОМАНДА«МОЛЕКУЛА»
- 5. Станция «Строение атома»
- 6. Разновидности атомов одного и того же химического
- 7. Задание№1. Для атома фосфора определить чему равен
- 8. Строение атомаЯдро1s орбиталь2s орбиталь2p орбиталь3s орбиталь3p орбиталь3d орбитальЭЛЕКТРОННАЯОБОЛОЧКА
- 9. Распределение электронов по энергетическим уровням. Составление электронных
- 10. Станция: «Периодическая система химических элементов Д.И.Менделеева и строение атома»
- 11. Задание№1. Расположите элементы в порядке увеличения их
- 12. Увеличиваются заряды атомных ядер;Число электронов на внешнем
- 13. Увеличиваются заряды атомных ядер;Увеличивается число электронов на
- 14. Станция«Химическая связь»
- 15. ЗАДАНИЯ-Запишите механизм образования ковалентной неполярной связи для
- 16. Ионы и ионная химическая связь. Химическая связь,
- 17. Ковалентная неполярная связьХимическая связь, возникающая в результате
- 18. Ковалентная полярная связьСвязь возникающая между атомами разныхХимических
- 19. МЕТАЛЛИЧЕСКАЯ СВЯЗЬМеталлическая связь- это связь возникающая в металлах между ионами и атомами посредством обобществлённых электронов.Na+NaNaNaNaNaNaNaNaNaNa+Na+Na+NaNaNa+Na+Na+Na+Na+NaNaNa+Na+Me0-ne-—Me+nMe+n+ne—Me0
- 20. Станция: «Периодическая система химических элементов Д.И.Менделеева и строение атома»Станция «Строение атома» Станция«Химическая связь
- 21. Задачи: - отработать навыки владения «химическим языком»-
- 22. С П А С И Б О ЗА У Р О К!
Слайд 3 Цели: Повторить, обобщить и систематизировать сведения о строении атома, структуре периодической
Задачи:
-отработать умения определять число электронов, протонов, нейтронов в атомах химических элементов
-закрепить умения составлять электронные схемы и электронные формулы для атомов химических элементов,
-определять, как изменяются металлические и неметаллические свойства атомов химических элементов в группе и периоде.
-определять вид химической связи в веществах;
-изображать механизм образования ионной, ковалентной, металлической связи;
Цели и задачи урока.
Слайд 6Разновидности атомов одного и того же химического элемента, имеющие одинаковый заряд
H
1
1
ПРОТИЙ
H
2
1
ДЕЙТЕРИЙ
H
3
1
ТРИТИЙ
АТОМНАЯ МАССА
ЗАРЯД ЯДРА
Слайд 7Задание№1. Для атома фосфора определить чему равен заряд ядра, число электронов,
Задание №2. Запишите для атома алюминия электронную схему и формулу. Сколько энергетических уровней в атоме алюминия? Почему? Сколько внешних электронов у атома и численно они равны……………….?
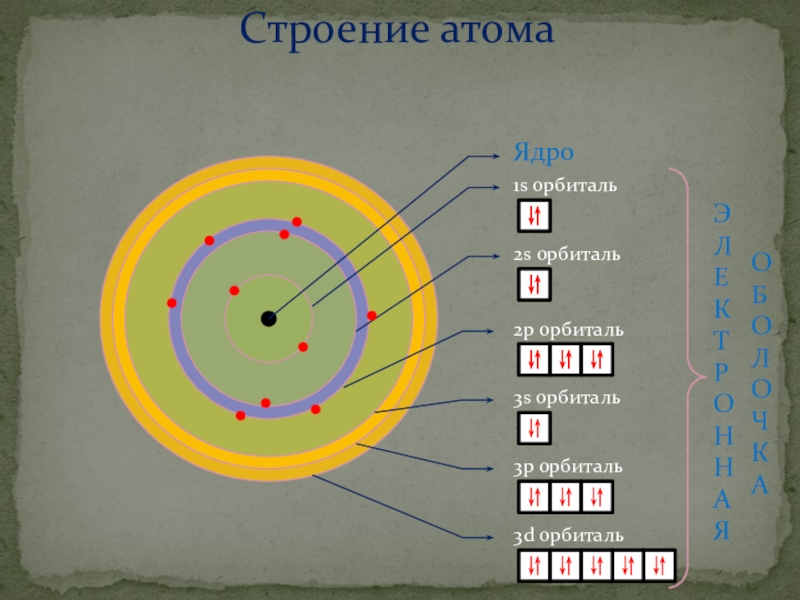
Слайд 8Строение атома
Ядро
1s орбиталь
2s орбиталь
2p орбиталь
3s орбиталь
3p орбиталь
3d орбиталь
Э
Л
Е
К
Т
Р
О
Н
Н
А
Я
О
Б
О
Л
О
Ч
К
А
Слайд 9Распределение электронов по энергетическим уровням.
Составление электронных схем
Номер периода совпадает с числом
Период
3
Группа
V
3
Число электронов (N) на уровне рассчитывается по формуле.
N = 2n2 , n –номер энергетического уровня.
n = 1, N = 2 . 12 = 2
2
n = 2, N = 2 . 22 = 8
8
Номер группы совпадает с числом электронов на последнем энергетическом уровне.
5
15
Проверка
15
Слайд 11Задание№1. Расположите элементы в порядке увеличения их металлических свойств: Sr, Mg,
Задание№2. Расположите элементы в порядке увеличения их неметаллических свойств: Si, Na, Al, Cl . Кто является самым сильным неметаллом?
В классе после контрольной работы учителем было найдено 2 шпаргалки. В одной из них была записана электронная формула, а в другой электронная схема неизвестных атомов химических элементов.
Определите:
-номер группы,
-номер периода,
-порядковый номер
-название химического элемента
Задание №2 1s 2s 2p 3s 3p
2 2 6 2 2
Задание №2 ) ) ) )
2 8 8 2
Слайд 12Увеличиваются заряды атомных ядер;
Число электронов на внешнем энергетическом уровне остаётся неизменным;
Увеличивается
Увеличивается радиус атома.
В пределах одной и той же группы
( в главной подгруппе)
сверху вниз
металлические свойства усиливаются , а не металлические – ослабевают, так как:
Слайд 13Увеличиваются заряды атомных ядер;
Увеличивается число электронов на внешнем энергетическом уровне;
Число энергетических
Радиус атома уменьшается
В пределах одного и того же периода
слева на право
металлические свойства ослабевают, а не металлические – усиливаются, так как:
Слайд 15ЗАДАНИЯ
-Запишите механизм образования ковалентной неполярной связи для O2
-Запишите механизм образования металлической
-Даны вещества: BaCl2, F2, Al, H2S.
Определите вид химической связи для каждого вещества. Запишите механизм образования химической связи для одного любого из веществ.
-Запишите механизм образования ионной связи для вещества:
CaO
-Запишите механизм образования ковалентной полярной связи для вещества:
HCl
.
Слайд 16Ионы и ионная химическая связь.
Химическая связь, образующуюся между ионами, называется ионной.
Ион – это частица образующаяся в результате отдачи или принятия электрона. Ионная связь как правило возникает между металлом и неметаллом.
Пример:
NaCl – хлорид натрия (поваренная, пищевая соль)
+
-1
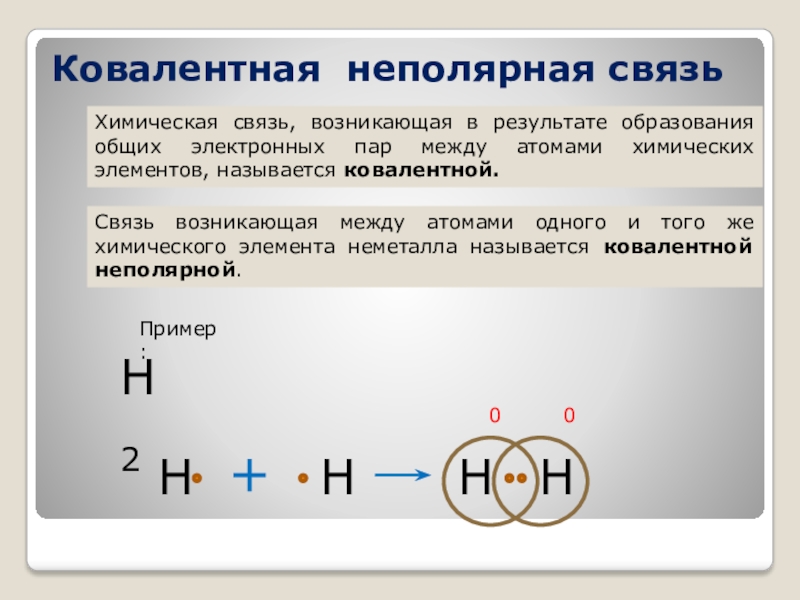
Слайд 17Ковалентная неполярная связь
Химическая связь, возникающая в результате образования общих электронных пар
Связь возникающая между атомами одного и того же химического элемента неметалла называется ковалентной неполярной.
Пример:
Н2
Н
Н
+
Н
Н
0
0
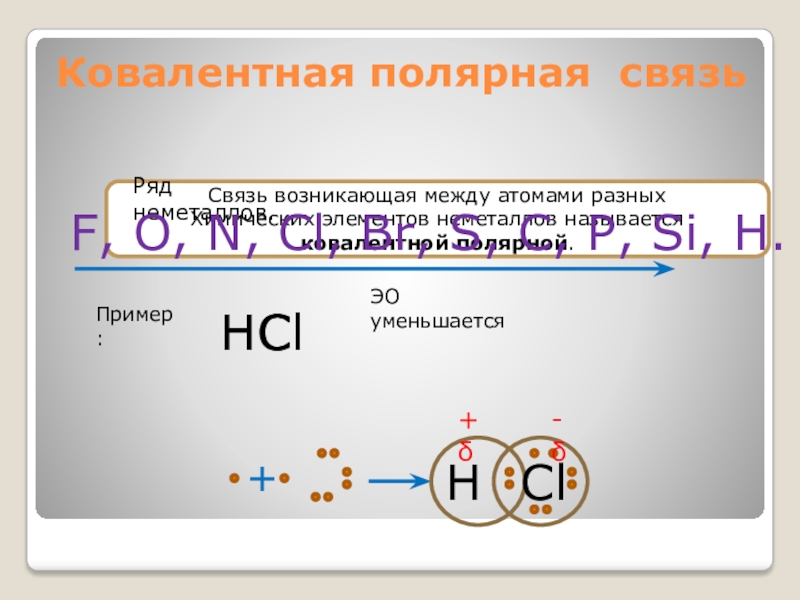
Слайд 18Ковалентная полярная связь
Связь возникающая между атомами разных
Химических элементов неметаллов называется ковалентной
Ряд неметаллов.
F, O, N, Cl, Br, S, C, P, Si, H.
ЭО уменьшается
Пример:
+
Н
- δ
+ δ
HCl
H
Cl
Cl
Слайд 19МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
Металлическая связь- это связь возникающая в металлах между ионами и
Na+
Na
Na
Na
Na
Na
Na
Na
Na
Na
Na+
Na+
Na+
Na
Na
Na+
Na+
Na+
Na+
Na+
Na
Na
Na+
Na+
Me
0
-ne
-
—
Me
+n
Me
+n
+ne
—
Me
0
Слайд 20Станция: «Периодическая система химических элементов Д.И.Менделеева и строение атома»
Станция «Строение атома»
Станция
«Химическая
Слайд 21Задачи: - отработать навыки владения «химическим языком»
- уметь определять число электронов,
-закрепить умения составлять электронные схемы и электронные формулы для атомов химических элементов,
-повторить структуру периодической таблицы Д.И.Менделеева и периодичность в изменении свойств атомов химических элементов
-определять вид химической связи в веществах;
-изображать механизм образования ионной, ковалентной, металлической связи;
ЗАДАЧИ УРОКА