- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Кислородсодержащие соединения фосфора
Содержание
- 1. Презентация по химии на тему Кислородсодержащие соединения фосфора
- 2. Слайд 2
- 3. Слайд 3
- 4. Фосфор образует: Оксид фосфора (V) Оксид фосфора (III) Фосфорную кислоту
- 5. Оксид фосфора (V) – представляет собой белое
- 6. При сжигании белого или красного фосфора в
- 7. «Белый и красный фосфор»
- 8. Фосфаты: Р2О5 + 3CaO = Ca3(PO4)2 Р2О5 + 6 NaOH = 2Na3PO4 + 3H2O
- 9. При взаимодействии оксид фосфора (V) с водой
- 10. Слайд 10
- 11. Диссоциация фосфорной кислоты: Н3РО4 → Н+ +
- 12. Химические свойства 1) Взаимодействие фосфорной кислоты с
- 13. Качественная реакция на фосфат-ионы: Na3PO4 +
- 14. «Качественная реакция на фосфат-ионы»
- 15. Слайд 15
- 16. Применение азотной кислоты и нитратов
- 17. Осуществите цепочку превращений: Р2О5 → Н3РО4 → Na3PO4 → Ca3(PO4)2 → H3PO4
- 18. Задание 1 1) P2O5 + 3H2O = 2H3PO4 2)
- 19. Домашнее задание: Параграф 44, задания 4,5.
- 20. Слайд 20
- 21. СПАСИБО ЗА ВНИМАНИЕ!!!
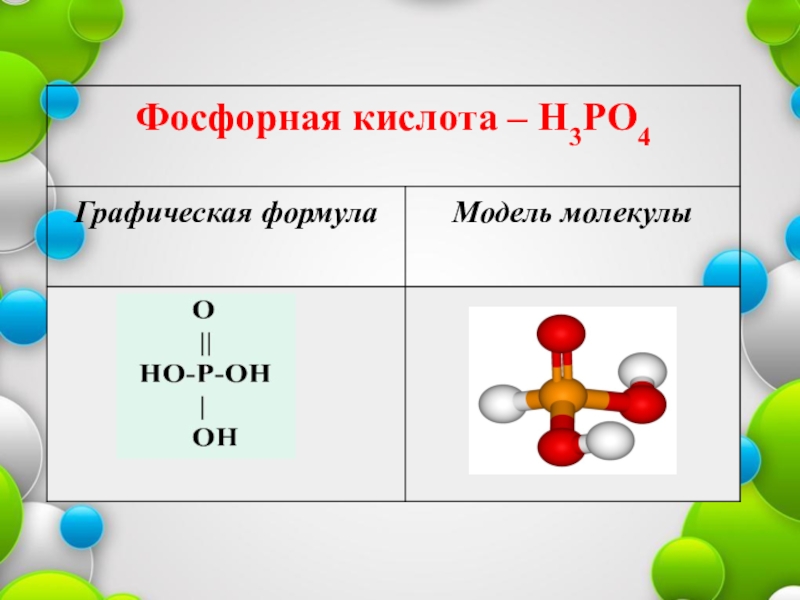
Фосфор образует: Оксид фосфора (V) Оксид фосфора (III) Фосфорную кислоту
Слайд 5Оксид фосфора (V) – представляет собой белое вещество, обладает гидроскопичностью, при
попадании на кожу может вызывать сильные ожоги.
Слайд 6При сжигании белого или красного фосфора в кислороде образуется оксид фосфора
(V) в виде белого дыма.
t
4Р + 5О2 = 2Р2О5
Слайд 9При взаимодействии оксид фосфора (V) с водой получается ортофосфорная кислота : Р2О5
+ 3Н2О = 2Н3РО4
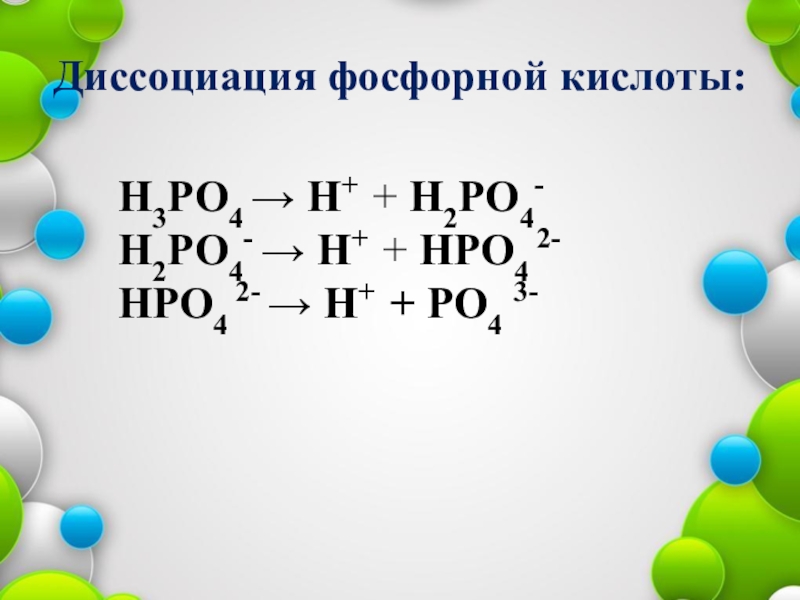
Слайд 11Диссоциация фосфорной кислоты:
Н3РО4 → Н+ + Н2РО4-
Н2РО4- → Н+ +
НРО4 2-
НРО4 2- → Н+ + РО4 3-
НРО4 2- → Н+ + РО4 3-
Слайд 12Химические свойства 1) Взаимодействие фосфорной кислоты с металлами, находящимися в ряду активности
до водорода:
3Mg + 2Н3РО4 = Mg3(РО4)2↓ + 3H2 ↑
2) C основными оксидами:
3BaO + 2Н3РО4 = Ba3(PO4)2↓ + 3H2O
3) C основаниями:
3NaOH + Н3РО4 = Na3PO4 + 3H2O
Слайд 13Качественная реакция на фосфат-ионы: Na3PO4 + 3AgNO3 = Ag3PO4↓ + 3NaNO3 PO43- +
3Ag+ = AgPO4↓
Слайд 17Осуществите цепочку превращений: Р2О5 → Н3РО4 → Na3PO4 → Ca3(PO4)2 → H3PO4 Установите соответствие между исходными веществами и продуктами
реакции:
a) 3Mg + 2Н3РО4 1) 2H3PO4
b) P2O5 + 3H2O 2) 2Na3PO4 + 3H2O + 3CO2↑
c) H3PO4 + 2NH3 3) Mg3(РО4)2↓ + 3H2 ↑
d) 2H3PO4+3Na2CO3 4) (NH3)2HPO4
Слайд 18Задание 1 1) P2O5 + 3H2O = 2H3PO4 2) H3PO4 + 3NaOH = Na3PO4 + 3H2O 3) 2Na3PO4 +
3CaCI2 = Ca3(PO4)2 + 6NaCl
4) Ca3(PO4)2 + 3H2SO4 = 3CaSO4 + 2H3PO4
Задание 2
Ключ: а) – 3; б) – 1; c) – 4; d) – 2.
Слайд 20 -те,
кто считает, что хорошо понял тему и поработал на уроке;
«Цветовой индекс»
-те, кто считает, что ему еще нужно работать над данной темой;
-те, кто считает, что недостаточно понял тему.