- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Кислород (8 класс)
Содержание
- 1. Презентация по химии на тему Кислород (8 класс)
- 2. Кислород – это вещество, вокруг которого
- 3. КИСЛОРОД
- 4. Цели урока:Знать…Уметь…Понимать…Применять…
- 5. .
- 6. Он повсюду и везде:В земле, в воздухе,
- 7. Слайд 7
- 8. Химический элементХимический знак – Положение в ПС
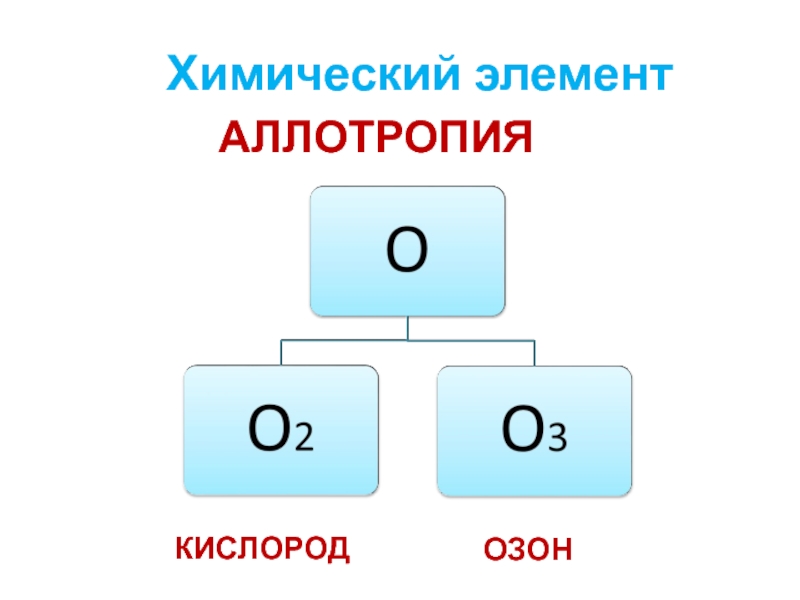
- 9. Химический элементКИСЛОРОДОЗОНАЛЛОТРОПИЯ
- 10. Простое веществоХимическая формула – O2Модель молекулы:Строение:молекулярноеMr (O2) =32
- 11. Химический элемент
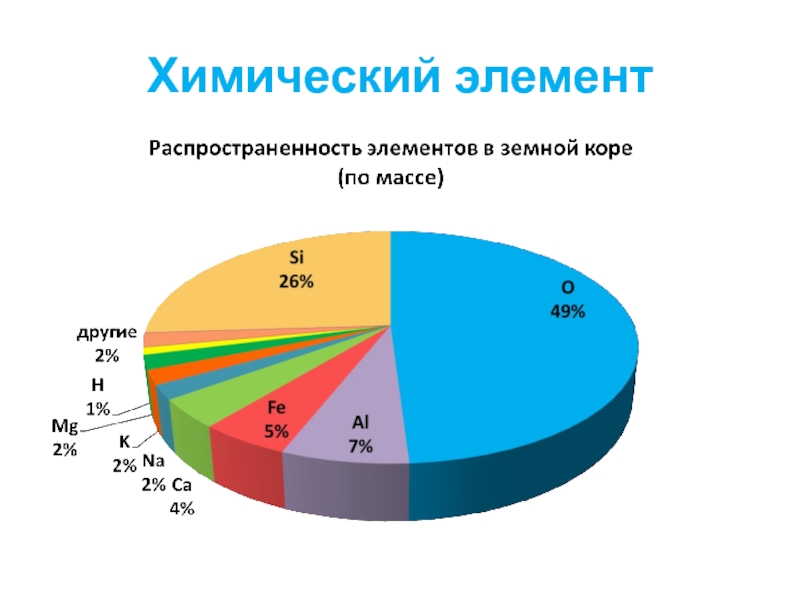
- 12. На долю кислорода приходится приблизительно половина всей
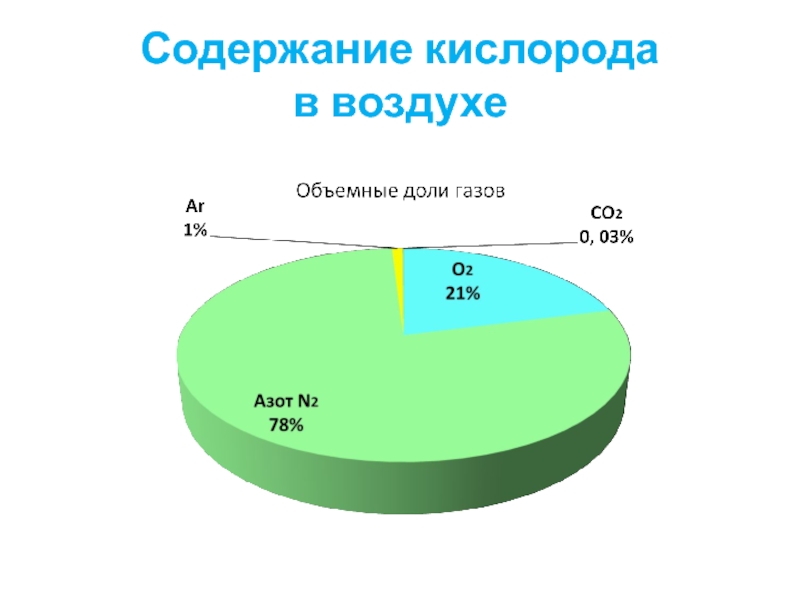
- 13. Содержание кислорода в воздухе
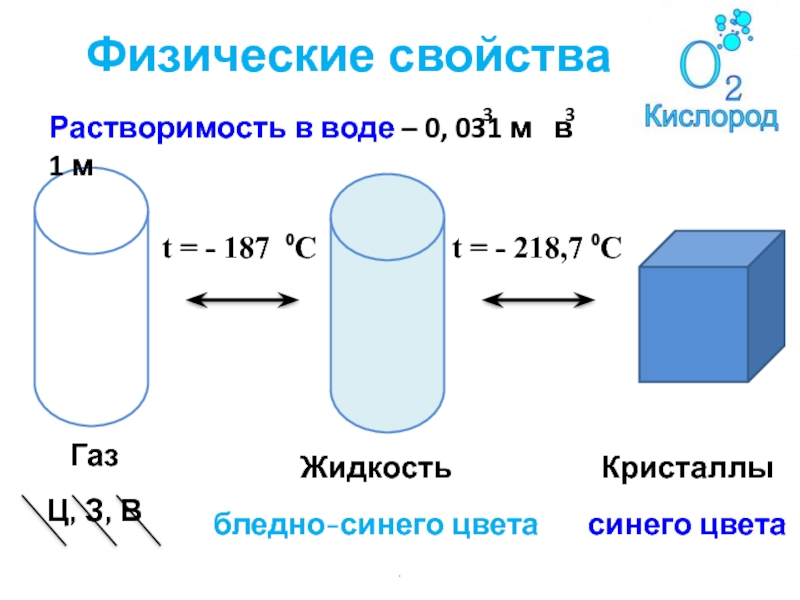
- 14. Физические свойстваt = - 187 ⁰Ct = - 218,7 ⁰CЖидкостьбледно-синего цветаКристаллысинего цвета.
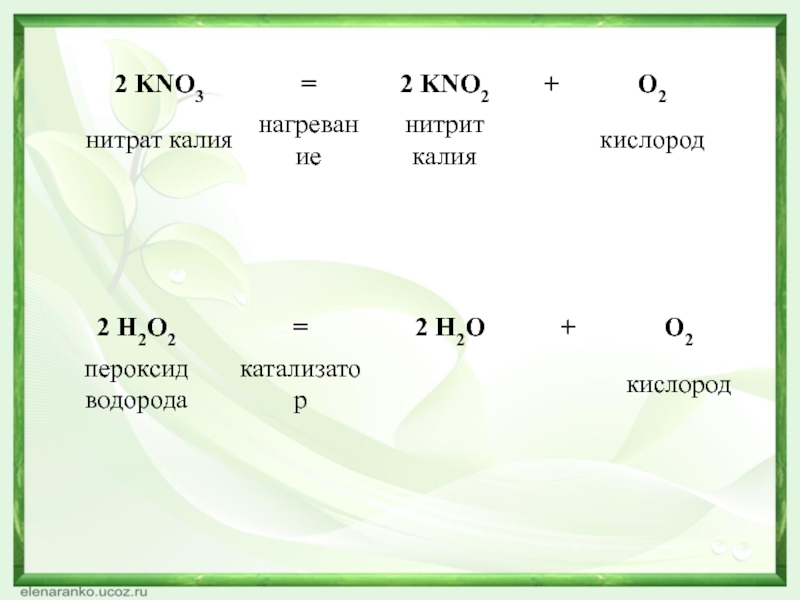
- 15. 2HgO=2Hg+O2↑История открытия кислорода1772 -1774 г. – швед.
- 16. Открытие кислорода.Кислород был получен им многими способами:
- 17. Джозеф Пристли (Joseph Priestley, 1733-1804)Джозеф Пристли В 1774 г получен английским ученым Дж. Пристли
- 18. Повторив опыты Пристли, Лавуазье заключил, что атмосферный
- 19. 1) В природе кислород образуется в процессе
- 20. Получение кислорода в лаборатории.Чаще всего кислород получают
- 21. Слайд 21
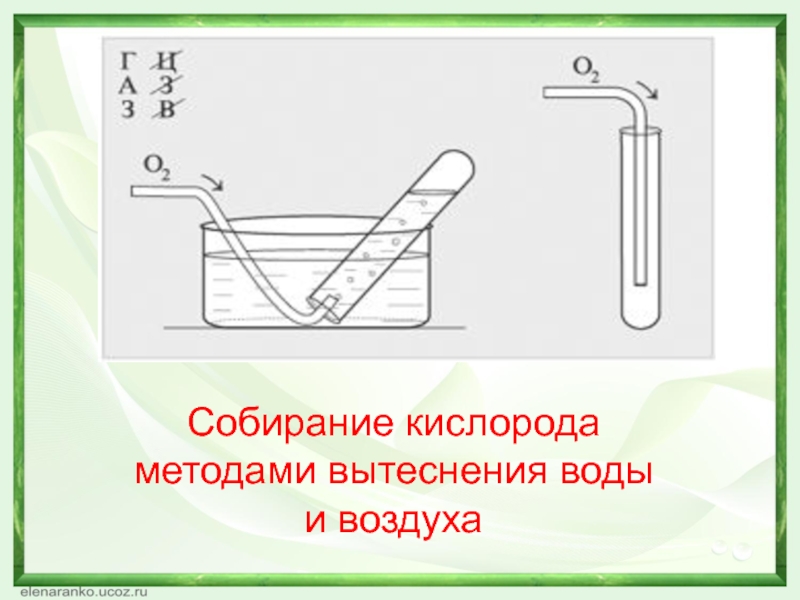
- 22. Собирание кислородаметодами вытеснения водыи воздуха
- 23. Как проверить, собрался ли кислород в сосуде?
- 24. Слайд 24
- 25. .
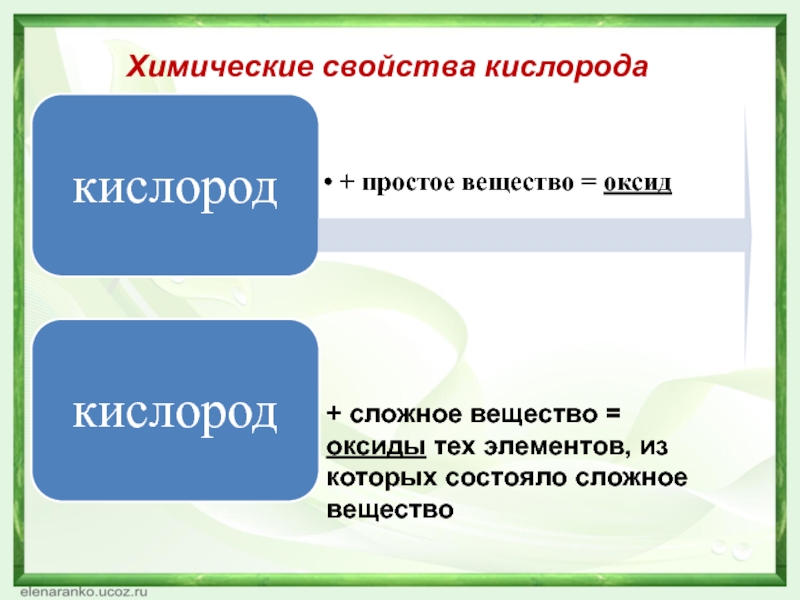
- 26. Химические свойства кислорода+ сложное вещество = оксиды тех элементов, из которых состояло сложное вещество
- 27. Химические свойства кислорода Допишите уравнения реакций:Ca +
- 28. Реакции с участием кислородаРеакции взаимодействия веществ с
- 29. Применение кислорода.
- 30. Круговорот кислорода в природе.
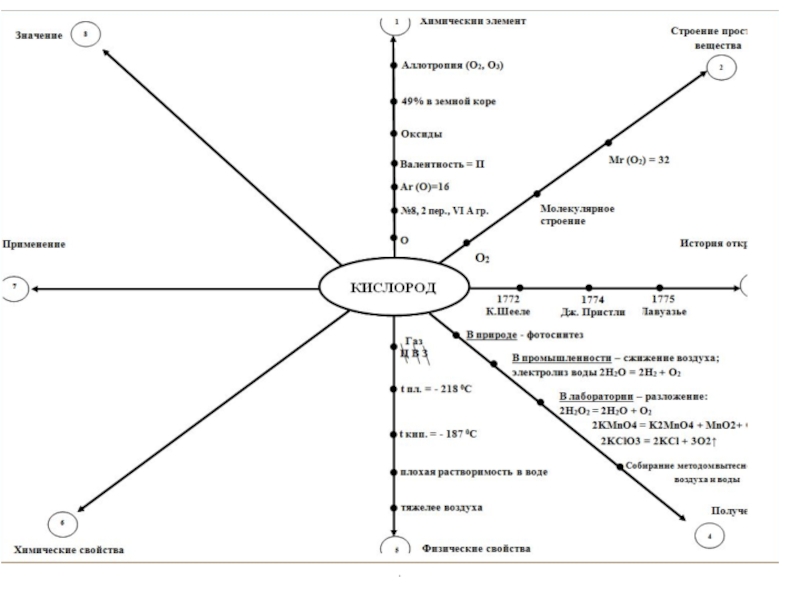
- 31. Схема-лабиринт «Общая характеристика кислорода, распространение кислорода в природе».
- 32. Правила техники безопасности. Осторожно обращайтесь с химическим
- 33. РефлексияСегодня я узнал (а) … Было трудно
Слайд 8Химический элемент
Химический знак –
Положение в ПС –
Аr (O) =
Валентность =
Соединения элементов с кислородом–
O
2 период, VI А группа
порядковый номер №8
16
II
оксиды
.
Слайд 12На долю кислорода приходится приблизительно половина всей массы земной коры. В почвах
Слайд 14Физические свойства
t = - 187 ⁰C
t = - 218,7 ⁰C
Жидкость
бледно-синего цвета
Кристаллы
синего
.
Слайд 152HgO=2Hg+O2↑
История открытия кислорода
1772 -1774 г. – швед. ученый
Карл Шееле
1774 год
англ. ученый Джозеф Пристли
1775 год –
франц. ученый Лавуазье
.
Слайд 16Открытие кислорода.
Кислород был получен им многими способами: прокаливанием оксида ртути (как
Слайд 17Джозеф Пристли
(Joseph Priestley,
1733-1804)
Джозеф Пристли
В 1774 г получен английским
Слайд 18Повторив опыты Пристли, Лавуазье заключил, что атмосферный воздух состоит из смеси
Антуан Лавуазье
(Lavoisier, Antoine Laurent,
1743-1794)
Слайд 191) В природе кислород образуется в процессе фотосинтеза
2) В промышленности его
3.Электролиз воды:
2H2O = 2H2↑ + O2↑
Способы получения кислорода
Слайд 20Получение кислорода в лаборатории.
Чаще всего кислород получают нагреванием таких веществ (в
Слайд 26Химические свойства кислорода
+ сложное вещество = оксиды тех элементов, из которых
Слайд 27Химические свойства кислорода
Допишите уравнения реакций:
Ca + O2 →
Na + O2
Al + O2 →
S + O2 →
H2S + O2 →
CH4 + O2→
Слайд 28Реакции с участием кислорода
Реакции взаимодействия веществ с кислородом относятся к реакциям
Реакции взаимодействия веществ с кислородом, протекающие с выделением большого количества тепла и света, называются реакциями горения
Слайд 32Правила техники безопасности.
Осторожно обращайтесь с химическим оборудованием!
Помните! Пробирку прогревают, держа ее
Тушите спиртовку только колпачком. Запрещается зажигать одну спиртовку с помощью другой. Запрещается передавать спиртовку в зажженном виде. Запрещается пробовать вещество на вкус. Работу проводить только над столом.
Слайд 33Рефлексия
Сегодня я узнал (а) …
Было трудно …
Теперь я могу …
Я понял,
Заключение.
Кислород – это…