Изучение условий протекания химических реакций между растворами электролитов до конца
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Изучение условий протекания химических реакций между растворами электролитов до конца
Содержание
- 1. Презентация по химии на тему Изучение условий протекания химических реакций между растворами электролитов до конца
- 2. Закрепить знания об условиях, при которых химические
- 3. Пробирки; растворы сульфата меди (II) (2 %),
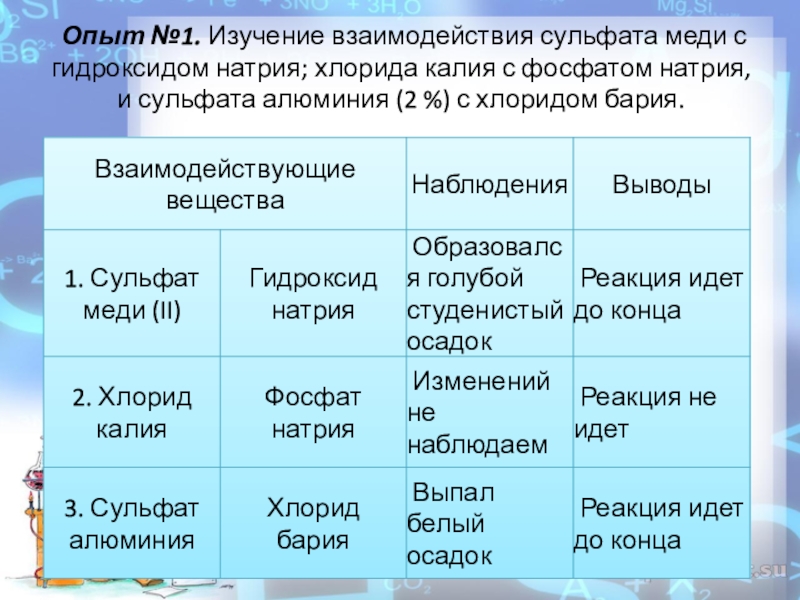
- 4. Опыт №1. Изучение взаимодействия сульфата меди
- 5. Слайд 5
- 6. CuSO₄+2NaOH →Cu(OH)₂↓ +Na₂SO₄ Cu²⁺ +SO₄²⁻+2Na⁺+2OH⁻→Cu(OH)₂↓+2Na⁺+SO₄²⁻ Cu²⁺+2OH⁻→Cu(OH)↓
- 7. Опыт №2. Изучение взаимодействия сульфита натрия и карбоната натрия с азотной кислотой.
- 8. Слайд 8
- 9. Na₂S+HNO₃→2NaNO₃+H₂S↑ 2Na⁺+S²⁻+2H⁺+2NO₃⁻→2Na⁺+2NO₃⁻+H₂S↑ S²⁻+2H⁺→H₂S↑ Na₂CO₃+2HNO₃→2NaNO₃+H₂O+CO₂↑ 2Na⁺+CO₃²⁻+2H⁺+2NO₃⁻→2Na⁺+2NO₃⁻+H₂O+CO₂↑
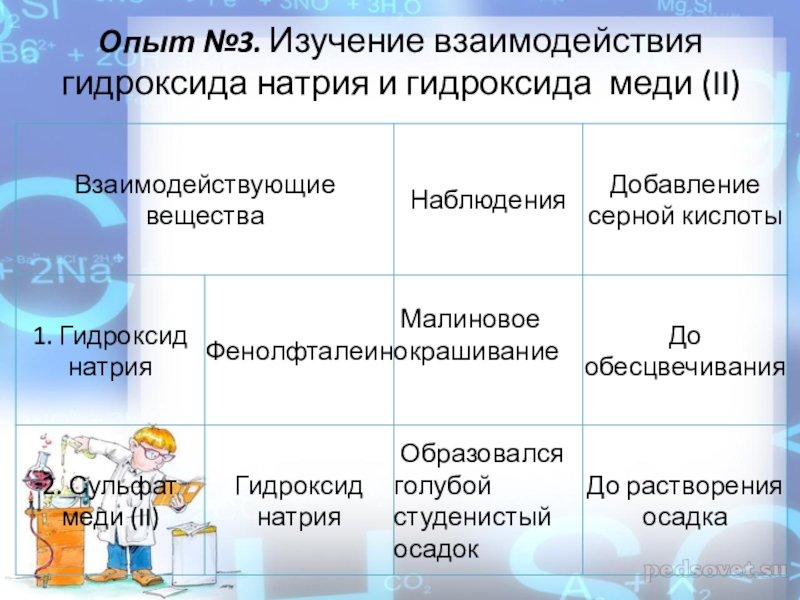
- 10. Опыт №3. Изучение взаимодействия гидроксида натрия и гидроксида меди (II)
- 11. Слайд 11
- 12. 2NaOH+H₂SO₄→Na₂SO₄+2H₂O 2Na⁺+2OH⁻+2H⁺+SO₄²⁻→2Na⁺+SO₄²⁻+2H₂O 2H⁺+2OH⁻→2H₂O H⁺+OH⁻→H₂O CuSO₄+2NaOH→Cu(OH)₂↓+Na₂SO₄ Cu²⁺+SO₄²⁻+2Na⁺+2OH⁻→Cu(OH)₂↓+2Na⁺+SO₄²⁻
- 13. 1.При взаимодействии гидроксида натрия с серной кислотой
Закрепить знания об условиях, при которых химические реакции между растворами электролитов идут до конца; продолжить формирование умений работать с растворами веществ.Цель работы:
Слайд 1Работу выполнили ученики
9 «А» класса
МБОУ СОШ №4 г.Пикалева
им. А.П.Румянцева
Слайд 2Закрепить знания об условиях, при которых химические реакции между растворами электролитов
идут до конца; продолжить формирование умений работать с растворами веществ.
Цель работы:
Слайд 3Пробирки; растворы сульфата меди (II) (2 %), хлорида калия (2 %),
сульфата алюминия (2 %), гидроксида натрия (10%), фосфата натрия (2 %), хлорида бария (2 %), сульфита натрия (2 %), азотной кислоты (1:3), серной кислоты (1:5), фенолфталеина.
Оборудование
и реактивы:
Слайд 4 Опыт №1. Изучение взаимодействия сульфата меди с гидроксидом натрия; хлорида
калия с фосфатом натрия, и сульфата алюминия (2 %) с хлоридом бария.
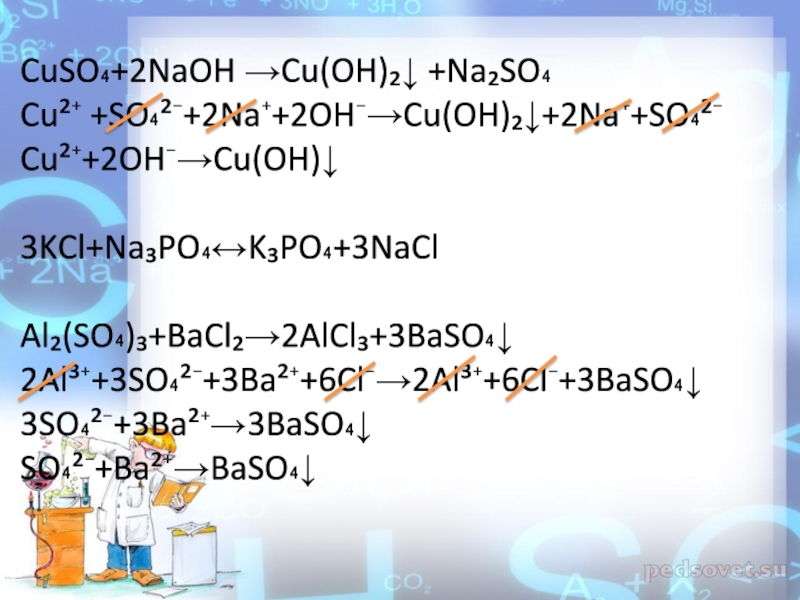
Слайд 6CuSO₄+2NaOH →Cu(OH)₂↓ +Na₂SO₄
Cu²⁺ +SO₄²⁻+2Na⁺+2OH⁻→Cu(OH)₂↓+2Na⁺+SO₄²⁻
Cu²⁺+2OH⁻→Cu(OH)↓
3KCl+Na₃PO₄↔K₃PO₄+3NaCl
Al₂(SO₄)₃+BaCl₂→2AlCl₃+3BaSO₄↓
2Al³⁺+3SO₄²⁻+3Ba²⁺+6Cl⁻→2Al³⁺+6Cl⁻+3BaSO₄↓
3SO₄²⁻+3Ba²⁺→3BaSO₄↓
SO₄²⁻+Ba²⁺→BaSO₄↓
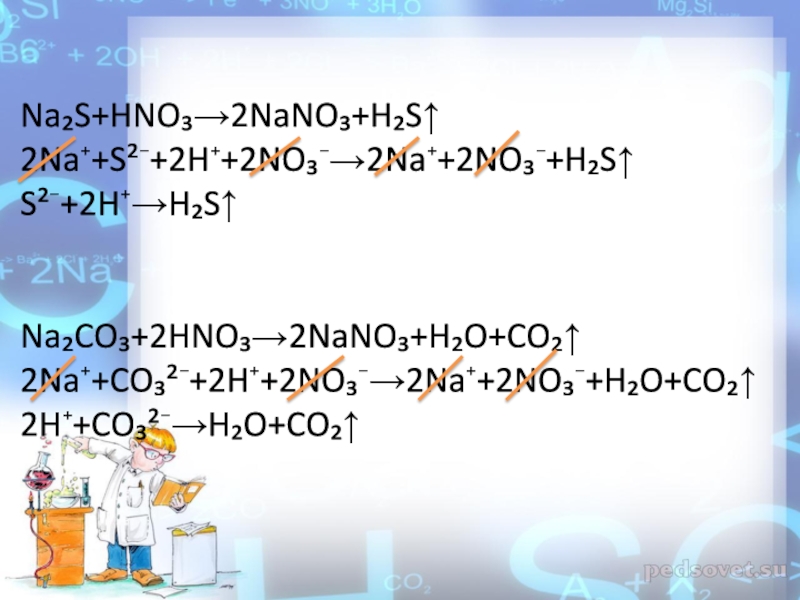
Слайд 9Na₂S+HNO₃→2NaNO₃+H₂S↑
2Na⁺+S²⁻+2H⁺+2NO₃⁻→2Na⁺+2NO₃⁻+H₂S↑
S²⁻+2H⁺→H₂S↑
Na₂CO₃+2HNO₃→2NaNO₃+H₂O+CO₂↑
2Na⁺+CO₃²⁻+2H⁺+2NO₃⁻→2Na⁺+2NO₃⁻+H₂O+CO₂↑
2H⁺+CO₃²⁻→H₂O+CO₂↑
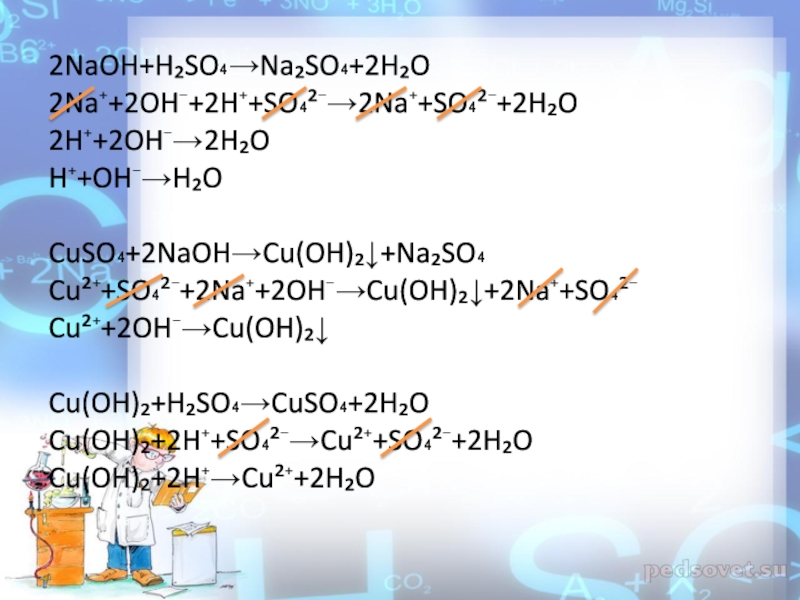
Слайд 122NaOH+H₂SO₄→Na₂SO₄+2H₂O
2Na⁺+2OH⁻+2H⁺+SO₄²⁻→2Na⁺+SO₄²⁻+2H₂O
2H⁺+2OH⁻→2H₂O
H⁺+OH⁻→H₂O
CuSO₄+2NaOH→Cu(OH)₂↓+Na₂SO₄
Cu²⁺+SO₄²⁻+2Na⁺+2OH⁻→Cu(OH)₂↓+2Na⁺+SO₄²⁻
Cu²⁺+2OH⁻→Cu(OH)₂↓
Cu(OH)₂+H₂SO₄→CuSO₄+2H₂O
Cu(OH)₂+2H⁺+SO₄²⁻→Cu²⁺+SO₄²⁻+2H₂O
Cu(OH)₂+2H⁺→Cu²⁺+2H₂O
Слайд 131.При взаимодействии гидроксида натрия с серной кислотой наблюдаем обесцвечивание фенолфталеина –
это реакция нейтрализации. Образуется соль и вода.
При взаимодействии гидроксида меди (II) с серной кислотой наблюдаем растворение осадка – это реакция нейтрализации. Образуется соль и вода.
2.Растворимые и нерастворимые основания взаимодействуют с кислотами. Это реакции ионного обмена, протекающие до конца.
При взаимодействии гидроксида меди (II) с серной кислотой наблюдаем растворение осадка – это реакция нейтрализации. Образуется соль и вода.
2.Растворимые и нерастворимые основания взаимодействуют с кислотами. Это реакции ионного обмена, протекающие до конца.