сажи и 5,6л водорода. Определите формулу этого вещества.
ρ(в-ва)= 3,482 г/л
m(С)= 6 г
V(Н2)= 5,6 л
СХНУ – ?
Решение:
ν(С)= m/M= 6/12=0.5моль
ν (Н2)= V/Vm=5.6/22.4=0.25моль; ν(Н)= 2*0,25=0,5моль
Х:У=0,5:0,5=1:1 СН – простейшая формула
М(СХНУ)= ρ(в-ва)* Vm= 3,482*22,4=77,996≈78г/моль
М(СН)=13г/моль
n= М(СХНУ)/ М(СН)= 78/13=6
Ответ: С6Н6
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Арены
Содержание
- 1. Презентация по химии на тему: Арены
- 2. Задача II группа:Задача: При сжигании 0,78г вещества
- 3. Углеводороды Предельные Непредельные Алканы Алкены Алкины
- 4. Майкл Фарадей (1791 - 1867)Английский физик и
- 5. Фридрих Август Кекуле 1829 - 1896Немецкий химик-органик.
- 6. Слайд 6
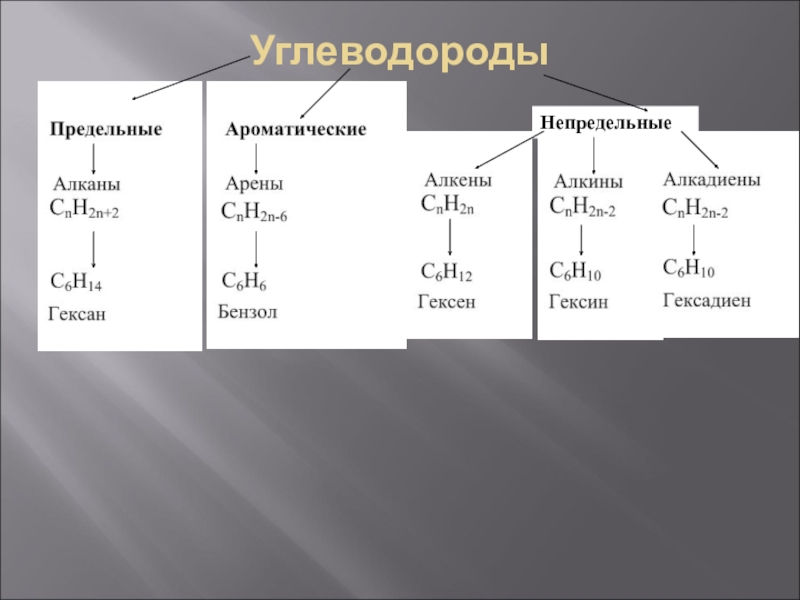
- 7. Углеводороды Непредельные
Задача II группа:Задача: При сжигании 0,78г вещества получено 1,344л углекислого газа и 0,54г воды. Определите формулу этого вещества.m(в-ва)=0,78гV(СО2)=1,344лm(H2O)=0.54гDH2(в-ва)=39СХНУ – ?Решение:ν(СО2)=V/Vm= 1.344/22.4=0.06 моль; ν(С)=0,06 мольν(Н2О)=m/M=0.54/18=0.03моль, ν(Н)=0,03*2=0,06 мольm(в-ва)= m(C)+ m(H) = ν(С)*12 + ν(Н)*10.78= 0.06*12+0.06*10.78=0.78Других элементов, кроме углерода
Слайд 2Задача
II группа:
Задача: При сжигании 0,78г вещества получено 1,344л углекислого газа
и 0,54г воды. Определите формулу этого вещества.
m(в-ва)=0,78г
V(СО2)=1,344л
m(H2O)=0.54г
DH2(в-ва)=39
СХНУ – ?
Решение:
ν(СО2)=V/Vm= 1.344/22.4=0.06 моль; ν(С)=0,06 моль
ν(Н2О)=m/M=0.54/18=0.03моль, ν(Н)=0,03*2=0,06 моль
m(в-ва)= m(C)+ m(H) = ν(С)*12 + ν(Н)*1
0.78= 0.06*12+0.06*1
0.78=0.78
Других элементов, кроме углерода и водорода, в составе вещества нет.
Х:У=0,06:0,06=1:1 СН – простейшая формула
М(СХНУ)= DH2(в-ва)* 2= 39*2=78 г/моль
М(СН)= 13 г/моль
n= М(СХНУ)/ М(СН)= 78/13=6
Ответ: С6Н6
m(в-ва)=0,78г
V(СО2)=1,344л
m(H2O)=0.54г
DH2(в-ва)=39
СХНУ – ?
Решение:
ν(СО2)=V/Vm= 1.344/22.4=0.06 моль; ν(С)=0,06 моль
ν(Н2О)=m/M=0.54/18=0.03моль, ν(Н)=0,03*2=0,06 моль
m(в-ва)= m(C)+ m(H) = ν(С)*12 + ν(Н)*1
0.78= 0.06*12+0.06*1
0.78=0.78
Других элементов, кроме углерода и водорода, в составе вещества нет.
Х:У=0,06:0,06=1:1 СН – простейшая формула
М(СХНУ)= DH2(в-ва)* 2= 39*2=78 г/моль
М(СН)= 13 г/моль
n= М(СХНУ)/ М(СН)= 78/13=6
Ответ: С6Н6
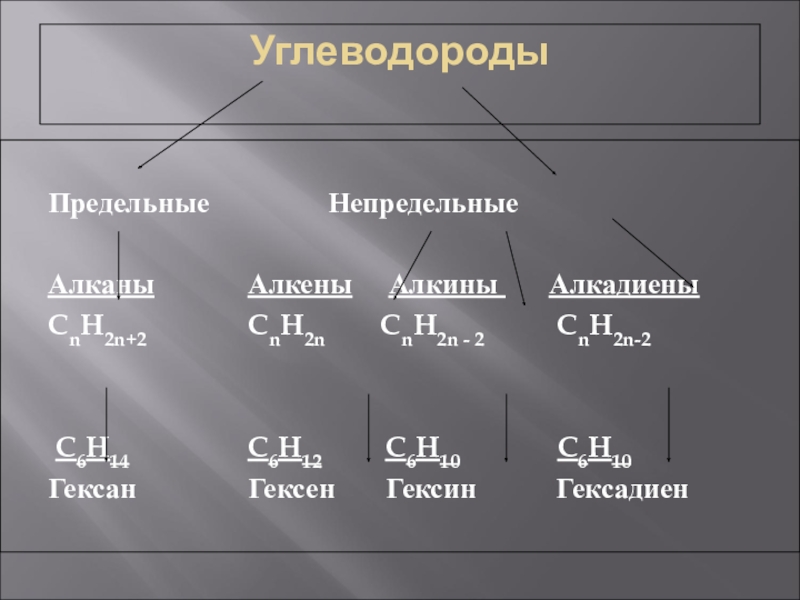
Слайд 3Углеводороды
Предельные Непредельные
Алканы Алкены Алкины Алкадиены
СnH2n+2 СnH2n
СnH2n - 2 СnH2n-2
C6H14 C6H12 C6H10 C6H10
Гексан Гексен Гексин Гексадиен
C6H14 C6H12 C6H10 C6H10
Гексан Гексен Гексин Гексадиен
Слайд 4Майкл Фарадей
(1791 - 1867)
Английский физик и химик, член Лондонского королевского общества.
Один из основателей количественной электрохимии. В 1823 г. впервые получил жидкие хлор, сероводород, оксид углерода(IV), аммиак, оксид азота(IV). В 1825 г. открыл бензол, изучил его физические и некоторые химические свойства. Положил начало исследованиям каучука. В 1833 - 1836 гг. установил количественные законы электролиза.
Слайд 5Фридрих Август Кекуле
1829 - 1896
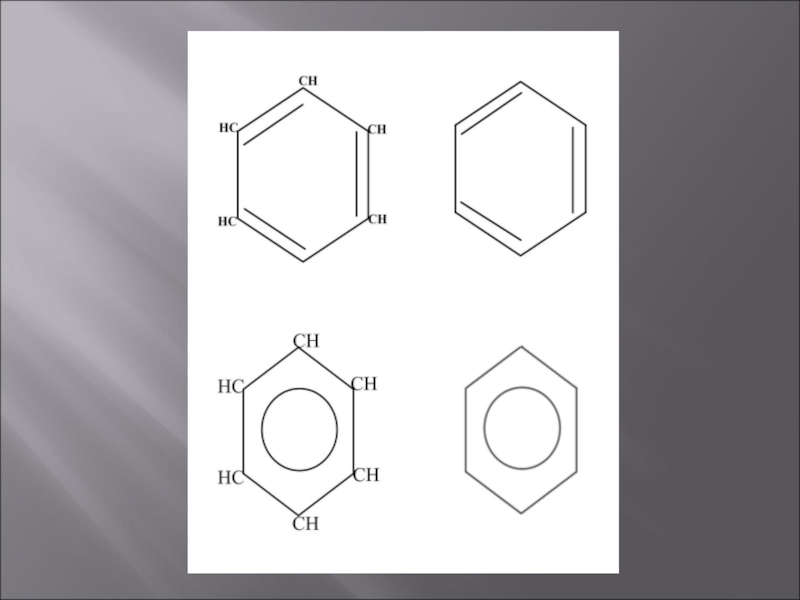
Немецкий химик-органик. Предложил структурную формулу молекулы бензола.
С целью проверки гипотезы о равноценности всех шести атомов водорода в молекуле бензола получил его галоген-, нитро-, амино- и карбоксипроизводные. Открыл перегруппировку диазоамино- в азоаминобензол, синтезировал трифенилметан и антрахинол.