- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Аминокислоты и БЖУ
Содержание
- 1. Презентация по химии на тему: Аминокислоты и БЖУ
- 2. Определение:Это органические кислоты или несколько аминогрупп с остатком NH6Общая формула аминокислот: H2N – R – COONАминокислоты.
- 3. По радикалу :1. Неполярные: глицин, аланин, валин,
- 4. По функциональным группам:1. Моноаминомонокарбоноые: глицин, аланин, валин,
- 5. По путями биосинтеза:1. Семейство аспартата: аспартат, аспарагин,
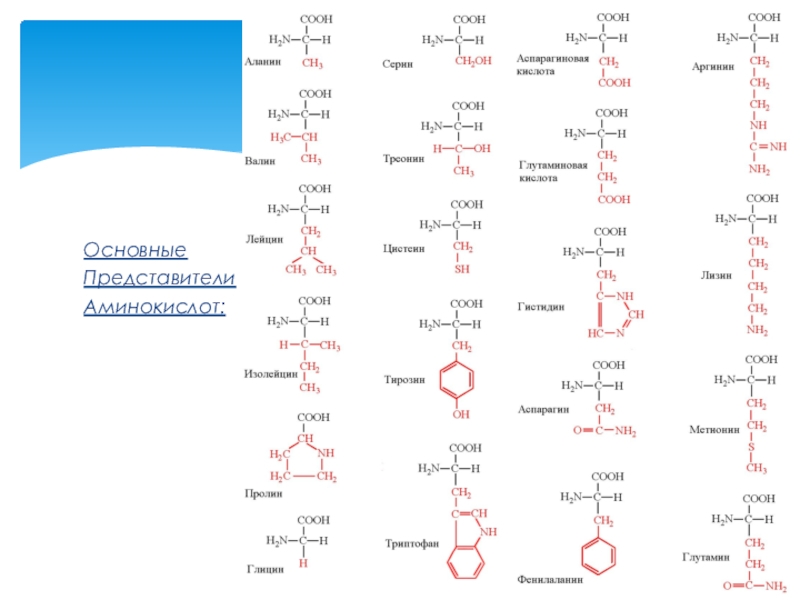
- 6. ОсновныеПредставителиАминокислот:
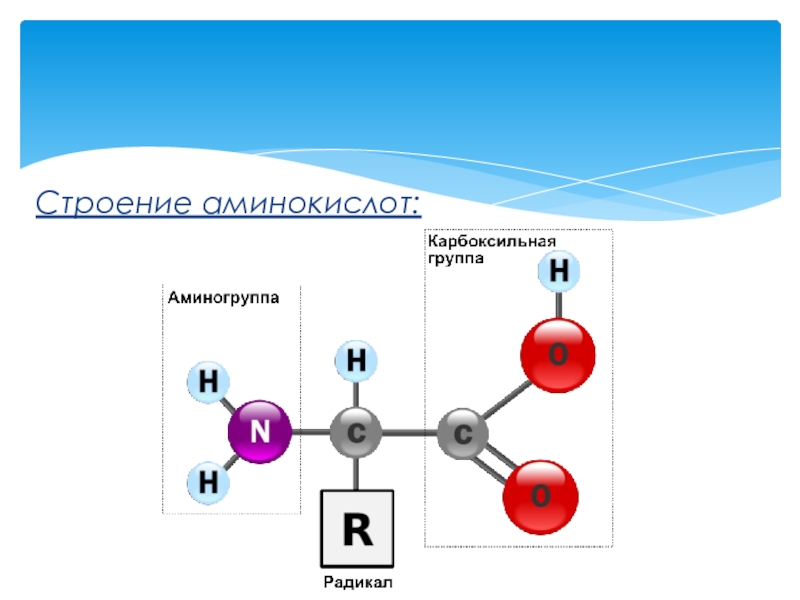
- 7. Строение аминокислот:
- 8. Физические свойства аминокислот:1. Цвитер-ионная форма.2. Хорошо кристаллизуется.3. Растворимы в воде.4. Высокая плотность.5. Высокая температура кипения.
- 9. Химические свойства аминокислот:1. Эфиры аминокислот под действием
- 10. Биологическая роль аминокислот:Наиб. интерес представляют 20 L-аминокислот
- 11. Определение:Это высокомолекулярные природные полимеры, построенные из остатков
- 12. Классификация:Простые белки: построены из остатков аминокислот и
- 13. Основные представители белков:1. Гликопротеиды2. Липотротеиды3. Металлопротеиды4. Нуклеопротеиды5. Фосфопротеиды6. Хромопротеиды
- 14. Физические свойства белков:1. Вязкие растворы2. Небольшая диффузия3.
- 15. Химические свойства белков:1. Амфотерность.2. Свободные COON-группы и
- 16. Биологическая роль белков:Белки - необходимая составная часть
- 17. Определение:Это вещество животного, растительного и микробного происхождения, состоящие с основном из триглицеридов. Жиры
- 18. Классификация; основные представители.Насыщенные:Стеариновая (С17H35COOH)Маргариновая (C16H33COOH)Пальмитиновая (C15H31COOH)Ненасыщенные:Пальмитолеиновая (C15H29COOH,
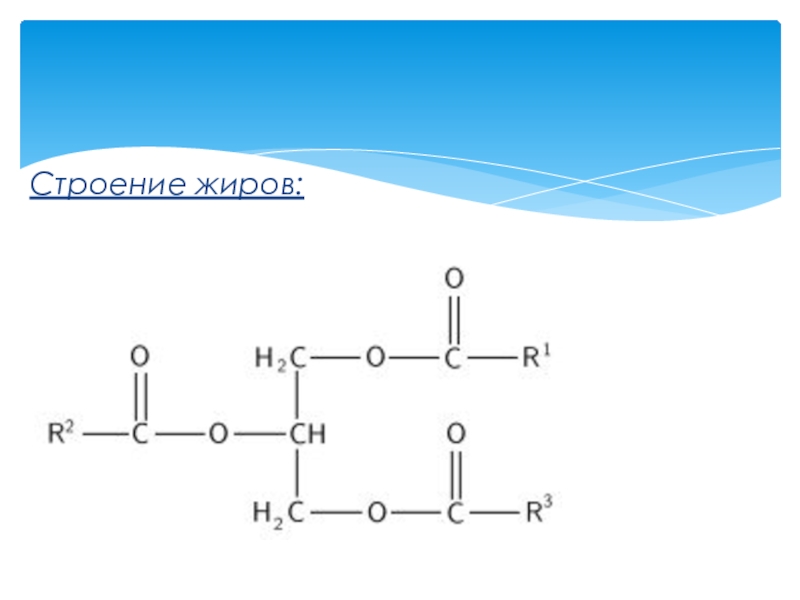
- 19. Строение жиров:
- 20. Физические свойства:1. Т-ры плавления индивидуальных триглицеридов, входящих
- 21. Химические свойства жиров:1. Пероксильные радикалы инициируют неразветвленные
- 22. Биологическая роль жиров:Жиры - одна из осн.
- 23. Определение:Это обширная группа полигодроксильнокрабонильных соединений, входящих в
- 24. Классификация.Моносахариды:Это углеводы, представляющие собой по-лигидроксиальдегиды (альдозы) и
- 25. Олигосахариды:Это углеводы, молекулы к-рых построены из неск.
- 26. Полисахариды: Полимерные углеводы, молекулы которых построены из
- 27. Физические свойства углеводов:Обилие полярных функц. групп в
- 28. Химические свойства углеводов:Полисахариды - гидрофильные полимеры, мн.
- 29. Биологическая роль углеводов:Биологическое значение углеводов:Углеводы выполняют структурную
Слайд 2Определение:
Это органические кислоты или несколько аминогрупп с остатком NH6
Общая формула аминокислот:
H2N – R – COON
Аминокислоты.
Слайд 3По радикалу :
1. Неполярные: глицин, аланин, валин, изолейцин, лейцин, пролин, метионин,
2. Полярные незаряженные: серин, треонин, цистеин, аспарагин, глутамин, тирозин.
3. Полярные заряженные положительно: глутат, аспартат.
4. Полярные заряженные отрицательно: лизин, аргинин, гистидин.
Классификация аминокислот :
Слайд 4По функциональным группам:
1. Моноаминомонокарбоноые: глицин, аланин, валин, изолейцин, лейцин.
2. Оксимоноаминокарбоновые: серин,
3. Моноаминодикарбоновые: аспаратат, глутомат.
4. Амиды моноаминодикарбоновые: аспаратен, глупамин.
5. Диаминомонокарбоновые: лизин, аргинин.
6. Серосодержащие: цистеин, метионин.
Слайд 5По путями биосинтеза:
1. Семейство аспартата: аспартат, аспарагин, треонин, изолейцин, метионин, лизин.
2.
3. Семейство терувата: аланин, валин, лейцин.
4. Семейство серина: серин, цистеин, глицин.
5. Семейство пентоз: гистизин, фенилаланин, тирозин, триптофан.
Слайд 8Физические свойства аминокислот:
1. Цвитер-ионная форма.
2. Хорошо кристаллизуется.
3. Растворимы в воде.
4. Высокая
5. Высокая температура кипения.
Слайд 9Химические свойства аминокислот:
1. Эфиры аминокислот под действием натрия или магнийорг. соед.
2. При окислении образуют альдегиды с укороченной углеродной цепочкой
3. Бетаины при нагр. могут обратимо превращ. в эфиры диметиламинокислот
4. С ионами переходных металлов (Си, Zn, Ni, Co, Pb, Ag, Hg, Cr). образуют прочные хелатные комплексы, что используется в комплексонах и в комплексообразующих ионообменных смолах на основе аминокарбоновых и аминофосфоновых к-т.
Слайд 10Биологическая роль аминокислот:
Наиб. интерес представляют 20 L-аминокислот (аланин, аргинин, аспарагин и
Слайд 11
Определение:
Это высокомолекулярные природные полимеры, построенные из остатков аминокислот, соединенных амидной (пептидной)
Общая формула белков:
NH2 – CH (R1) – CO – NH – CH (R2) – COON.
Белки.
Слайд 12Классификация:
Простые белки: построены из остатков аминокислот и при гидролизе распадаются только
Сложные белки: двухкомпонентные белки, которые состоят из какого-либо белка и небелкового компонента (про-сетестическая сетка)
Слайд 13Основные представители белков:
1. Гликопротеиды
2. Липотротеиды
3. Металлопротеиды
4. Нуклеопротеиды
5. Фосфопротеиды
6. Хромопротеиды
Слайд 14Физические свойства белков:
1. Вязкие растворы
2. Небольшая диффузия
3. Способность к набуханию
4. Подвижность
5. Низкое осмотическое давление
6. Способность к поглощению УФ-лучей
Слайд 15Химические свойства белков:
1. Амфотерность.
2. Свободные COON-группы и NH2
3. В ряде случаев
4. Боковые группы аминокислотных остатков способны вступать во многие р-ции.
5. Белки дают ряд цветных р-ций, обусловленных наличием определенных аминокислотных остатков или хим. группировок.
Слайд 16Биологическая роль белков:
Белки - необходимая составная часть продуктов питания. Проблема пищевого
В процессе пищеварения белки подвергаются гидролизу до аминокислот, к-рые и всасываются в кровь. Пищ. ценность белков зависит от их аминокислотного состава, содержания в них т. наз. незаменимых аминокислот, не синтезирующихся в организмах (для человека незаменимы триптофан, лейцин, изолейцин, валин, треонин, лизин, метионин и фенилаланин). В питательном отношении растит. белки менее ценны. чем животные; они беднее лизином, метионином и триптофаном, труднее перевариваются. Один из путей решения проблемы - добавление в растит. пищу синтетич. аминокислот. Наряду с этим выводят новые сорта растений, содержащие гены, ответственные за синтез недостающих аминокислот. Перспективно использование для этого методов генетич. инженерии. Чрезвычайно важное значение имеет широкое внедрение пром. микробиологического синтеза, напр. выращивание дрожжей на гидролизном этиловом спирте, прир. газе или нефти. Получаемые при этом белково-витаминные концентраты (БВК) используют в качестве добавок к корму с.-х. животных.
Слайд 17Определение:
Это вещество животного, растительного и микробного происхождения, состоящие с основном из
Жиры
Слайд 18Классификация; основные представители.
Насыщенные:
Стеариновая (С17H35COOH)
Маргариновая (C16H33COOH)
Пальмитиновая (C15H31COOH)
Ненасыщенные:
Пальмитолеиновая (C15H29COOH, 1 двойная связь)
Олеиновая (C17H33COOH,
Линолевая (C17H31COOH, 2 двойные связи)
Линоленовая (C17H29COOH, 3 двойные связи)
Арахидоновая (C19H31COOH, 4 двойные связи, реже встречается)
Слайд 20Физические свойства:
1. Т-ры плавления индивидуальных триглицеридов, входящих в состав жиров, зависят
2. При расщеплении выделяется 38 кДж/г (т.е. высокая энергетическая ценность)
3. Из-за сильного межмол. взаимод. жирно-кислотных цепей вязкость жиров высока.
4. Все жиры характеризуются значит. увеличением объема при плавлении.
5. При постепенном охлаждении жидкий жир частично кристаллизуется и приобретает форму твердого тела, обладающего пластичностью.
6. Жиры плохие проводники тепла и электричества.
Слайд 21Химические свойства жиров:
1. Пероксильные радикалы инициируют неразветвленные и разветвленные цепные р-ции,
2. Микроорганизмы, развивающиеся в жирах, выделяют др. ферменты - липооксидазы, под действием к-рых жирные к-ты окисляются до b-кетокислот.
3. Для замедления и предотвращения хим. прогоркания используют ингибиторы.
Слайд 22Биологическая роль жиров:
Жиры - одна из осн. групп в-в, входящих, наряду
Слайд 23Определение:
Это обширная группа полигодроксильнокрабонильных соединений, входящих в состав всех живых организмов.
Основные
Глюкоза: C6H12O6
Фруктоза: C6H12O6
Галактоза: C6H12O6
Сахароза: C12(H2O)11
Крахмал: [C6(H12O)5]n
Углеводы.
Слайд 24Классификация.
Моносахариды:
Это углеводы, представляющие собой по-лигидроксиальдегиды (альдозы) и полигидроксикетоны (ке-тозы) общей ф-лы
(п = 3-9), в которых каждый атом С (кроме карбонильного) связан с группой ОН, и производные этих соед., содержащие разл. др. функц. группы, а также атом Н вместо одного или неск. гидроксилов.
Моносахариды- бесцв. кристаллич. в-ва, легко раств. в воде, ДМСО, трудно-в этаноле, не раств. в неполярных орг. р-рителях. Важнейшие физ.-хим. характеристики моносахаридов -уд. вращение, используемое наряду с хроматографич. методами для идентификации природных моносахаридов, и спектры ПМР, с помощью к-рых можно определить относит. конфигурацию моносахаридов.
Для выяснения абс. конфигурации используют рентгеноструктурный анализ кристаллов или хим. трансформацию моносахаридов в более простые соед. с известной конфигурацией.
Хим. св-ва моносахаридов обусловлены наличием в их молекулах групп С=О (у ациклич. таутомера) и ОН.
При действии NaBH4 в водном р-ре карбонильная группа моносахаридов количественно восстанавливается до спиртовой; образующиеся полиолы в виде летучих ацетатов или триметилсилиловых эфиров можно использовать для количеств. анализа смесей моносахаридов с помощью ГЖХ.
Слайд 25Олигосахариды:
Это углеводы, молекулы к-рых построены из неск. моносахаридных остатков (от 2
В состав олигосахаридов могут входить остатки к.-л. одного моносахарида (гомоолигосахариды) или разных моносахаридов (гете-роолигосахариды).
Одна из ф-ций олигосахаридов группы лактозы - формирование бактериальной флоры в кишечнике новорожденных, необходимой для нормального пищеварения.
Синтез олигосахаридов - одна из сложнейших задач синтетич. химии углеводов. Для этой цели разработаны многочисл. приемы избират. защиты гидроксильных групп в молекулах моносахаридов и ряд весьма эффективных методов стереоспе-цифич. построения гликозидной связи.
Слайд 26Полисахариды:
Полимерные углеводы, молекулы которых построены из моносахаридных остатков, соединенных гликозидными
Степень полимеризации полисахаридов составляет от 10-20 до неск. тысяч остатков.
Линейные полисахариды имеют один невосстанавливающий и один восстанавливающий конец.
Большинство полисахаридов-бесцв. аморфные порошки, разлагающиеся при нагр. выше 200 °С.
Р-римость конкретного полисахарида определяет методику выделения его из прир. объекта.
Слайд 27Физические свойства углеводов:
Обилие полярных функц. групп в молекулах моносахаридов приводит к
Слайд 28Химические свойства углеводов:
Полисахариды - гидрофильные полимеры, мн. из них образуют высоковязкие
Слайд 29Биологическая роль углеводов:
Биологическое значение углеводов:
Углеводы выполняют структурную функцию, то есть участвуют
Углеводы выполняют защитную роль у растений (клеточные стенки, состоящие из клеточных стенок мертвых клеток защитные образования — шипы, колючки и др.).
Углеводы выполняют пластическую функцию — хранятся в виде запаса питательных веществ, а также входят в состав сложных молекул (например, пентозы (рибоза и дезоксирибоза) участвуют в построении АТФ, ДНК и РНК.
Углеводы являются основным энергетическим материалом. При окислении 1 грамма углеводов выделяются 4,1 ккал энергии и 0,4 г воды.
Углеводы участвуют в обеспечении осмотического давления и осморегуляции. Так, в крови содержится 100—110 мг/% глюкозы. От концентрации глюкозы зависит осмотическое давление крови.
Углеводы выполняют рецепторную функцию — многие олигосахариды входят в состав воспринимающей части клеточных рецепторов или молекул-лигандов.



















![Презентация по химии на тему: Аминокислоты и БЖУ Определение:Это обширная группа полигодроксильнокрабонильных соединений, входящих в состав всех живых организмов.Основные Определение:Это обширная группа полигодроксильнокрабонильных соединений, входящих в состав всех живых организмов.Основные представители:Глюкоза: C6H12O6Фруктоза: C6H12O6Галактоза: C6H12O6Сахароза: C12(H2O)11Крахмал: [C6(H12O)5]nУглеводы.](/img/tmb/3/209128/f8e99073d90c52dfd851b67455a3690d-800x.jpg)











