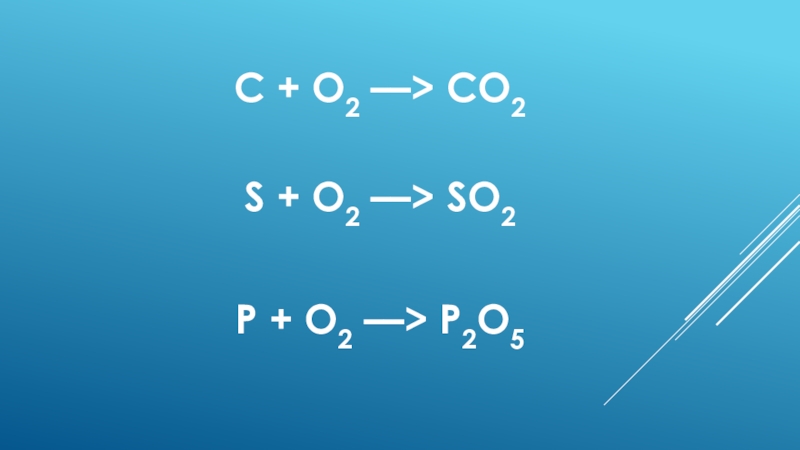- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к открытому уроку по химии Кислород - химические свойства кислорода
Содержание
- 1. Презентация к открытому уроку по химии Кислород - химические свойства кислорода
- 2. Поставьте знак «+», если предложенное утверждение подходит
- 3. Правильные ответы: Знак «+»: 1 3 4
- 4. «Гореть, светить и окисляться, Со мной в
- 5. 1. Узнать химические свойства кислорода 2.
- 6. Реакция окисления - реакция, в результате которой вещество реагирует с кислородом.
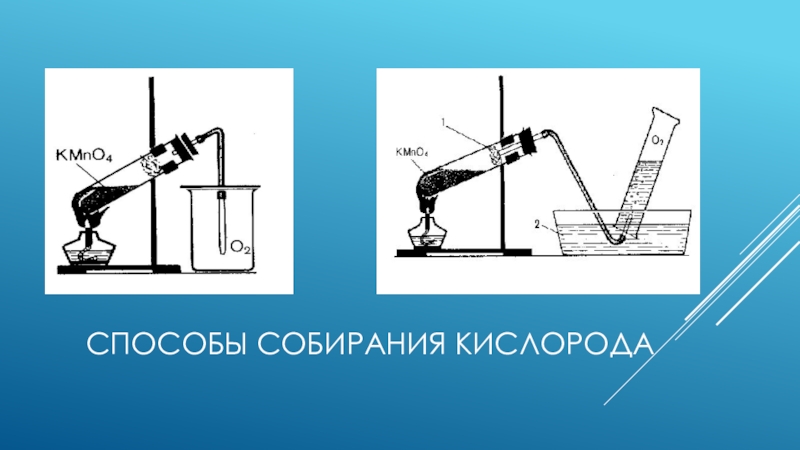
- 7. Способы собирания кислорода
- 8. №1- Вычислить массовую долю элемента кислорода (I
- 9. Слайд 9
- 10. Слайд 10
- 11. C + O2 ––> CO2 S + O2 ––> SO2P + O2 ––> P2O5
- 12. Реакция горения – реакция, при которой происходит окисление веществ с выделением теплоты и света.
- 13. ОксидыСложные вещества из атомов двух элементов один из которых кислород. Валентность кислорода в оксидах равна II.
- 14. CO2 - оксид углерода (IV) SO2 –
- 15. Слайд 15
- 16. Реакция медленного окисления – Реакция окисления, которая
Поставьте знак «+», если предложенное утверждение подходит кислороду, и знак «-», если не подходит. В промышленности получают из воздуха;Сложное вещество;При обычных условиях бесцветный газ;Собирают вытеснением воздуха;В природе встречается только в составе сложных веществ;Собирают в перевёрнутый вверх
Слайд 2Поставьте знак «+», если предложенное утверждение подходит кислороду, и знак
«-», если не подходит.
В промышленности получают из воздуха;
Сложное вещество;
При обычных условиях бесцветный газ;
Собирают вытеснением воздуха;
В природе встречается только в составе сложных веществ;
Собирают в перевёрнутый вверх дном сосуд;
В лаборатории получают из «марганцовки»;
Газ, имеющий запах;
Поддерживает горение;
Тяжелее воздуха;
При температуре – 183 0С превращается в жидкость;
Входит в состав минералов, горных пород, песка, воды;
При обычных условиях – жидкость;
Входит в состав воздуха;
Образуется в природе в процессе фотосинтеза.
В промышленности получают из воздуха;
Сложное вещество;
При обычных условиях бесцветный газ;
Собирают вытеснением воздуха;
В природе встречается только в составе сложных веществ;
Собирают в перевёрнутый вверх дном сосуд;
В лаборатории получают из «марганцовки»;
Газ, имеющий запах;
Поддерживает горение;
Тяжелее воздуха;
При температуре – 183 0С превращается в жидкость;
Входит в состав минералов, горных пород, песка, воды;
При обычных условиях – жидкость;
Входит в состав воздуха;
Образуется в природе в процессе фотосинтеза.
Слайд 3
Правильные ответы:
Знак «+»: 1 3 4 7 9 10 11
12 14 15
0-1 ошибка – оценка 5
2-3 ошибки – оценка 4
4-5 ошибок – оценка 3
0-1 ошибка – оценка 5
2-3 ошибки – оценка 4
4-5 ошибок – оценка 3
Слайд 4«Гореть, светить и окисляться, Со мной в оксиды превращаться. Да, будет свет,
тепло и жар,
Мой, кислорода, это дар!»
О2
Слайд 51. Узнать химические свойства кислорода 2. Научиться записывать уравнения химических реакций горения 3.
Научиться называть получившиеся вещества.
Тема: Химические свойства кислорода. Реакции горения.
Слайд 8№1- Вычислить массовую долю элемента кислорода
(I вариант) в перманганате калия
KMnO4
(II вариант) в хлорате калия (бертолетовой соли) KClO3
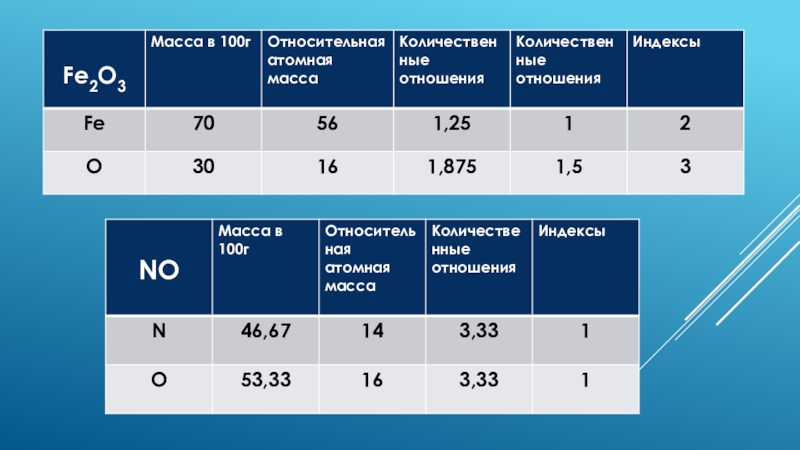
*** №2 - Составьте формулы соединений
Железа с кислородом, если массовая доля железа составляет 70% (I вариант)
Азота с кислородом, если массовая доля азота составляет 46,67% (II вариант)
(II вариант) в хлорате калия (бертолетовой соли) KClO3
*** №2 - Составьте формулы соединений
Железа с кислородом, если массовая доля железа составляет 70% (I вариант)
Азота с кислородом, если массовая доля азота составляет 46,67% (II вариант)
Слайд 12Реакция горения –
реакция, при которой происходит окисление веществ с выделением
теплоты и света.
Слайд 13Оксиды
Сложные вещества из атомов двух элементов один из которых кислород.
Валентность
кислорода в оксидах равна II.
Слайд 16Реакция медленного окисления –
Реакция окисления, которая идет медленно, с постепенным
выделением теплоты и не сопровождается выделением света.