- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Алкендер (11 класс)
Содержание
- 1. Презентация по химии на тему Алкендер (11 класс)
- 2. АЛКЕНДЕР – ҚАНЫҚПАҒАН КӨМІРСУТЕКТЕР. АЛЫНУЫ,ФИЗИКАЛЫҚ, ХИМИЯЛЫҚ ҚАСИЕТТЕРІ
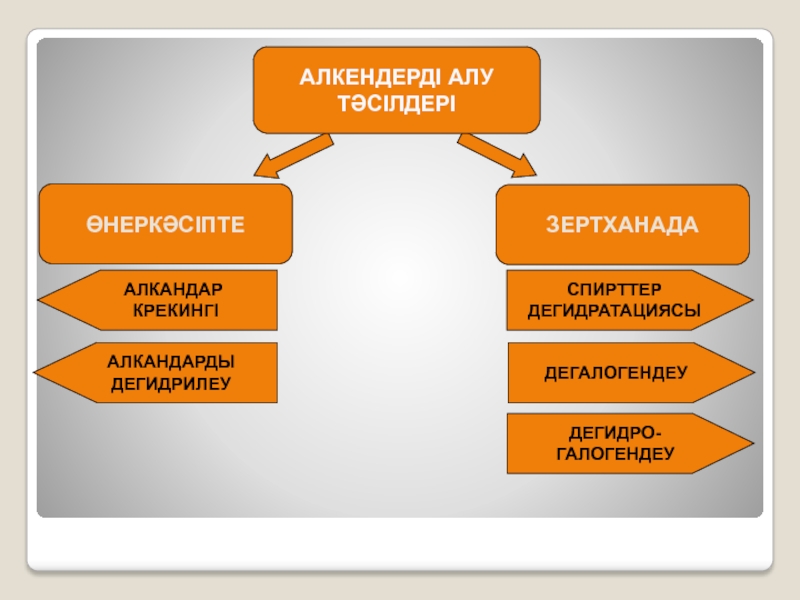
- 3. ӨНЕРКӘСІПТЕАЛКЕНДЕРДІ АЛУ ТӘСІЛДЕРІЗЕРТХАНАДААЛКАНДАР КРЕКИНГІ АЛКАНДАРДЫ ДЕГИДРИЛЕУСПИРТТЕР ДЕГИДРАТАЦИЯСЫДЕГАЛОГЕНДЕУДЕГИДРО-ГАЛОГЕНДЕУ
- 4. АЛКАНДАР КРЕКИНГІ АЛКАН → АЛКАН
- 5. АЛКАНДЫ ДЕГИДРЛЕУАЛКАН → АЛКЕН +
- 6. СПИРТТЕРДІҢ ДЕГИДРАТАЦИЯСЫСПИРТ → АЛКЕН + СУМЫСАЛ:
- 7. ДЕГАЛОГЕНДЕУМЫСАЛ:
- 8. ДЕГИДРОГАЛОГЕНДЕУ МЫСАЛ:
- 9. Алкендердің физикалық қасиеттеріАлкендер – түссіз, иіссіз заттар.
- 10. Бірдей молекулалардың үлкен молекулалы заттарға қосылу процесі.МЫСАЛ:
- 11. АЛКЕНДЕРДІҢ ЖАНУЫ МЫСАЛ:
- 12. ЖҰМСАҚ ТОТЫҒУ – калий перманганатының ерітіндісімен
- 13. Этиленнің қолданылуы
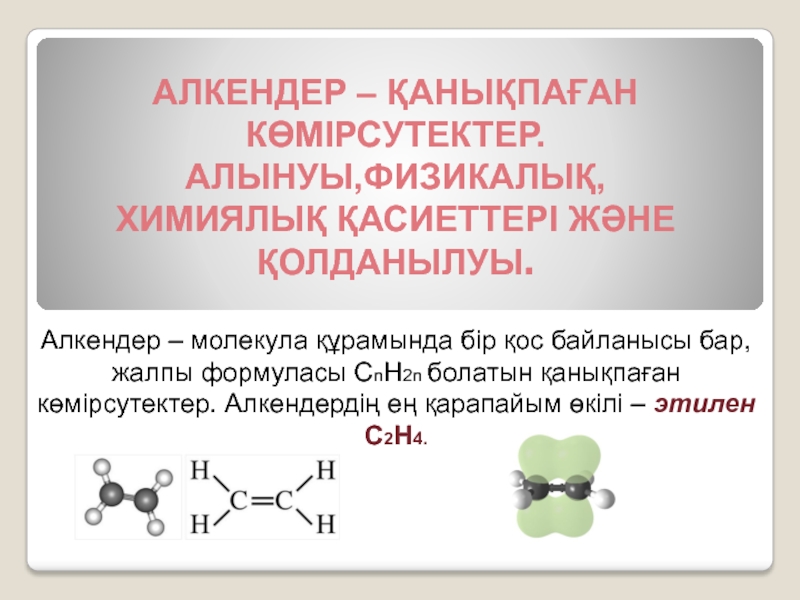
АЛКЕНДЕР – ҚАНЫҚПАҒАН КӨМІРСУТЕКТЕР. АЛЫНУЫ,ФИЗИКАЛЫҚ, ХИМИЯЛЫҚ ҚАСИЕТТЕРІ ЖӘНЕ ҚОЛДАНЫЛУЫ.Алкендер – молекула құрамында бір қос байланысы бар, жалпы формуласы СnH2n болатын қанықпаған көмірсутектер. Алкендердің ең қарапайым өкілі – этилен С2Н4.
Слайд 2АЛКЕНДЕР – ҚАНЫҚПАҒАН КӨМІРСУТЕКТЕР.
АЛЫНУЫ,ФИЗИКАЛЫҚ, ХИМИЯЛЫҚ ҚАСИЕТТЕРІ ЖӘНЕ ҚОЛДАНЫЛУЫ.
Алкендер – молекула құрамында
бір қос байланысы бар, жалпы формуласы СnH2n болатын қанықпаған көмірсутектер. Алкендердің ең қарапайым өкілі – этилен С2Н4.
Слайд 3ӨНЕРКӘСІПТЕ
АЛКЕНДЕРДІ АЛУ
ТӘСІЛДЕРІ
ЗЕРТХАНАДА
АЛКАНДАР
КРЕКИНГІ
АЛКАНДАРДЫ
ДЕГИДРИЛЕУ
СПИРТТЕР
ДЕГИДРАТАЦИЯСЫ
ДЕГАЛОГЕНДЕУ
ДЕГИДРО-
ГАЛОГЕНДЕУ
Слайд 4АЛКАНДАР КРЕКИНГІ
АЛКАН → АЛКАН + АЛКЕН
ҰЗЫН КӨМІРТЕК КІШІ КӨМІРТЕК
ТІЗБЕКТІ ТІЗБЕКТІ
МЫСАЛ:
t=400-700C
С10Н22 → C5H12 + C5H10
декан пентан пентен
ТІЗБЕКТІ ТІЗБЕКТІ
МЫСАЛ:
t=400-700C
С10Н22 → C5H12 + C5H10
декан пентан пентен
ӨНЕРКӘСІПТЕ АЛЫНУ ЖОЛДАРЫ
Слайд 5АЛКАНДЫ ДЕГИДРЛЕУ
АЛКАН → АЛКЕН + СУТЕК
МЫСАЛ:
Ni, t=500C
Н3С - СН3 → Н2С = СН2 + Н2
этан этен
(этилен)
Н3С - СН3 → Н2С = СН2 + Н2
этан этен
(этилен)
ӨНЕРКӘСІПТЕ АЛЫНУ ЖОЛДАРЫ
Слайд 6СПИРТТЕРДІҢ ДЕГИДРАТАЦИЯСЫ
СПИРТ → АЛКЕН + СУ
МЫСАЛ:
t≥140C,
Н Н Н2SO4(конц.)
Н-С – С-Н → Н2С = СН2 + Н2О
Н ОН этен
(этилен)
Н Н Н2SO4(конц.)
Н-С – С-Н → Н2С = СН2 + Н2О
Н ОН этен
(этилен)
ЗЕРТХАНАДА АЛЫНУ ЖОЛДАРЫ
Слайд 7ДЕГАЛОГЕНДЕУ
МЫСАЛ:
t
Н2С – СН2 + Zn → Н2С = СН2 + ZnBr2
Br Br этен
1,2-дибромэтан (этилен)
Н2С – СН2 + Zn → Н2С = СН2 + ZnBr2
Br Br этен
1,2-дибромэтан (этилен)
ЗЕРТХАНАДА АЛЫНУ ЖОЛДАРЫ
Слайд 8ДЕГИДРОГАЛОГЕНДЕУ
МЫСАЛ:
спирттік
H H ерітінді
Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O
Н Cl этен
хлорэтан (этилен)
H H ерітінді
Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O
Н Cl этен
хлорэтан (этилен)
ЗЕРТХАНАДА АЛЫНУ ЖОЛДАРЫ
Слайд 9Алкендердің физикалық қасиеттері
Алкендер – түссіз, иіссіз заттар. Гомологтардың молекулалық массаларының өсулеріне
байланысты балқу және қайнау температуралары мен тығыздықтары артады. Алкендердің алғашқы үш мүшесі (этен, пропен, бутен) газдар, пентеннен бастап сұйық, ал С18Н36 –дан бастап қатты заттар.
Алкендер судан жеңіл, суда нашар, органикалық еріткіштерде жақсы ериді.
Алкендер судан жеңіл, суда нашар, органикалық еріткіштерде жақсы ериді.
Слайд 10Бірдей молекулалардың үлкен молекулалы заттарға қосылу процесі.
МЫСАЛ: n CH2=CH2
(-CH2-CH2-)n
этилен полиэтилен
(мономер) (полимер)
n – полимеризация дәрежесі, жақша ішіндегі буындардың санын көрсетеді.
-CH2-CH2- структурлық буын
этилен полиэтилен
(мономер) (полимер)
n – полимеризация дәрежесі, жақша ішіндегі буындардың санын көрсетеді.
-CH2-CH2- структурлық буын
ПОЛИМЕРИЗАЦИЯ РЕАКЦИЯСЫ
Слайд 12 ЖҰМСАҚ ТОТЫҒУ – калий перманганатының ерітіндісімен әрекеттесуі
(Е.Е.Вагнер реакциясы)
Н2С=СН2 +
[O] + H2O H2C - CH2
OH OH
этиленгликоль
(этандиол-1,2)
! Қанықпаған көмірсутектердің қысқа байланысқа сапалық реакциясы.
OH OH
этиленгликоль
(этандиол-1,2)
! Қанықпаған көмірсутектердің қысқа байланысқа сапалық реакциясы.
ТОТЫҒУ РЕАКЦИЯСЫ









![Презентация по химии на тему Алкендер (11 класс) ЖҰМСАҚ ТОТЫҒУ – калий перманганатының ерітіндісімен әрекеттесуі (Е.Е.Вагнер реакциясы)Н2С=СН2 + ЖҰМСАҚ ТОТЫҒУ – калий перманганатының ерітіндісімен әрекеттесуі (Е.Е.Вагнер реакциясы)Н2С=СН2 + [O] + H2O H2C](/img/tmb/1/48727/c041c2ba5eaa0e2558a6fa05a216a03c-800x.jpg)






