- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Альдегиды и кетоны
Содержание
- 1. Презентация по химии на тему Альдегиды и кетоны
- 2. ОПРЕДЕЛЕНИЕ АЛЬДЕГИДЫ СnH2n+1OН или СnH2nO это органические
- 3. ОПРЕДЕЛЕНИЕКЕТОНЫ – органические вещества, в молекулах которых
- 4. Строение группы С=ОСвойства альдегидов и кетонов определяются
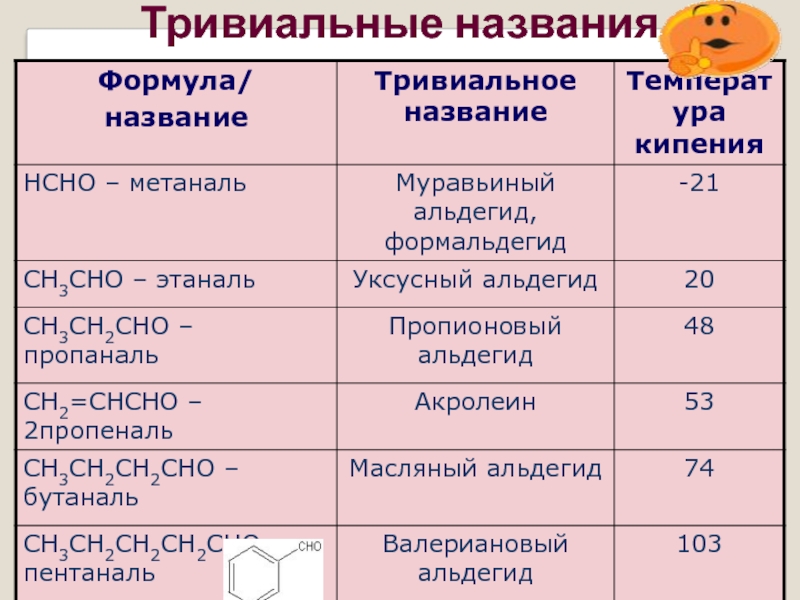
- 5. Тривиальные названия
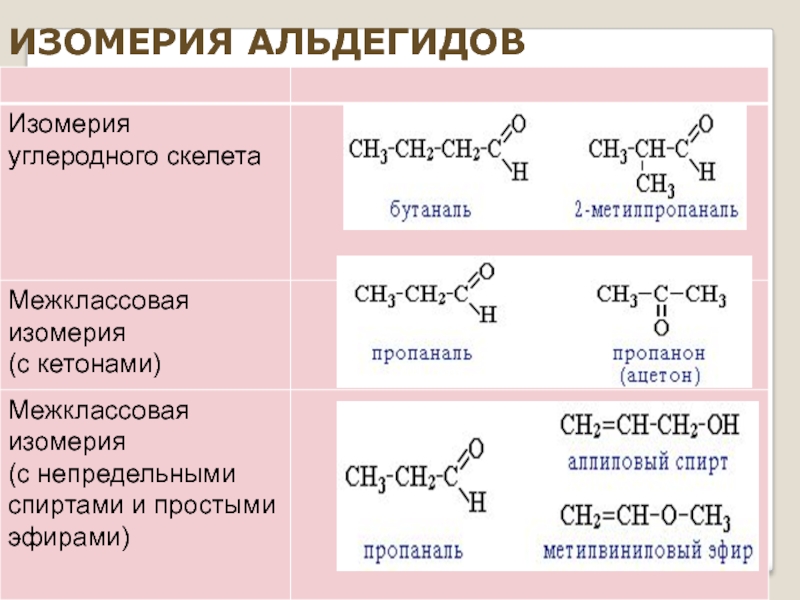
- 6. ИЗОМЕРИЯ АЛЬДЕГИДОВ
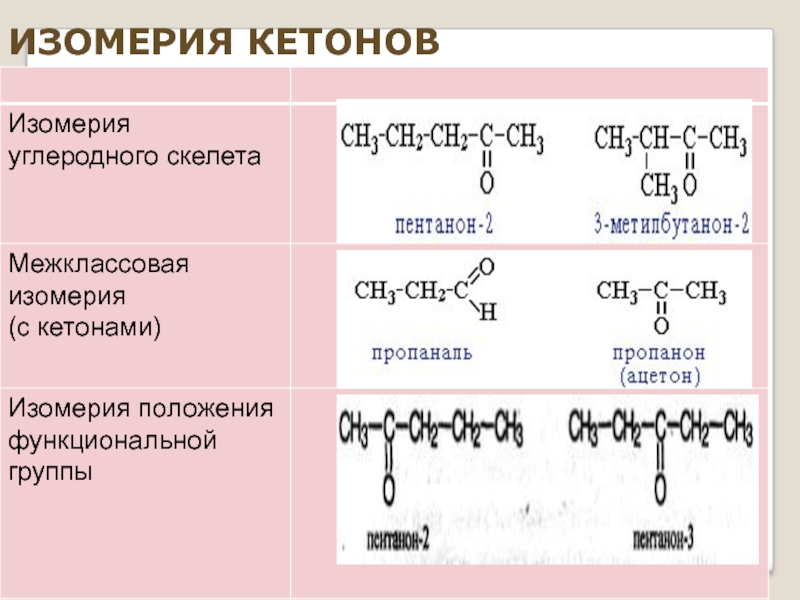
- 7. ИЗОМЕРИЯ КЕТОНОВ
- 8. Изомерия и номенклатура
- 9. С1 – газ
- 10. Физические свойства кетоновКетоны — летучие жидкости. Кетоны
- 11. Отличительной чертой многих альдегидов является
- 12. Булочки ванильные, корицы аромат,Амаретто, шоколадАльдегидов вкус таят.В
- 13. В плодах ванили
- 14. Запах цитрусовых обусловлен данным диеновым
- 15. Коричный альдегид Коричный альдегид содержится
- 16. Бензальдегид Бензальдегид – жидкость с
- 17. ФенилэтанальФенилэтаналь по сравнению с бензальдегидом лучше соответствует
- 18. n-Гидроксифенилбутанон-2 Этот кетон обуславливает в основном
- 19. ХИМИЧЕСКИЕ СВОЙСТВАРЕАКЦИЯ ВОССТАНОВЛЕНИЯ ОСН3
- 20. ХИМИЧЕСКИЕ СВОЙСТВАРеакции нуклеофильного присоединения
- 21. ХИМИЧЕСКИЕ СВОЙСТВАПрисоединение гидросульфитов
- 22. R – C = O + [O]
- 23. Кетоны окисляются в более жёстких условиях с
- 24. ХИМИЧЕСКИЕ СВОЙСТВАРЕАКЦИИ ОКИСЛЕНИЯ Реакция серебряного зеркала- качественная
- 25. Реакция с гидроксидом меди качественная реакция
- 26. Атом водорода, соединённый с углеродом, ближайшим к
- 27. Реакции замещения по связи С=О 1). С
- 28. СПОСОБЫ ПОЛУЧЕНИЯГИДРАТАЦИЯ АЛКИНОВ (Реакция Кучерова) HgSO4,H2SO4,t
- 29. СПОСОБЫ ПОЛУЧЕНИЯДЕГИДРИРОВАНИЕ СПИРТОВ
- 30. СПОСОБЫ ПОЛУЧЕНИЯОКИСЛЕНИЕ СПИРТОВ
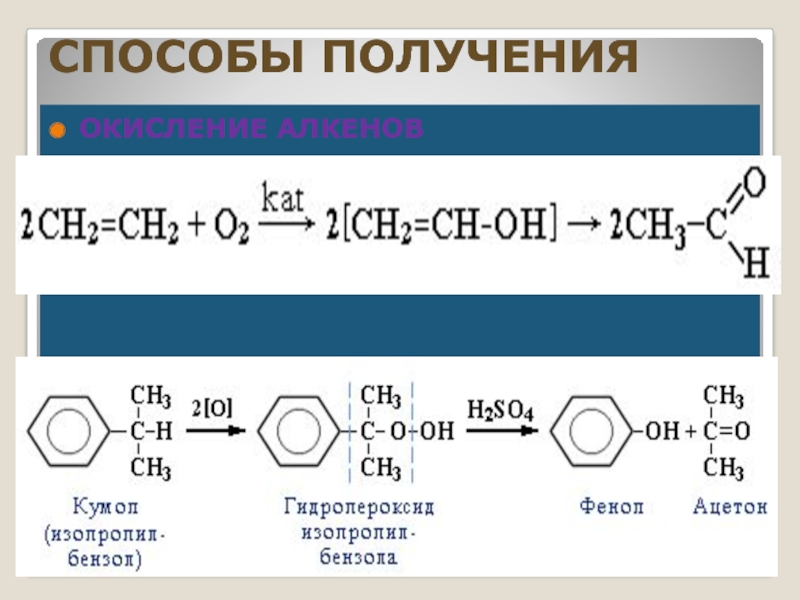
- 31. СПОСОБЫ ПОЛУЧЕНИЯОКИСЛЕНИЕ АЛКЕНОВКУМОЛЬНЫЙ СПОСОБ
- 32. Слайд 32
- 33. Слайд 33
- 34. ПРИМЕНЕНИЕ АЛЬДЕГИДОВПАРФЮМЕРИЯАльдегид анисовый, обепин – жидкость с
- 35. ПРИМЕНЕНИЕ АЛЬДЕГИДОВПОЛИМЕРНЫЕ МАТЕРИАЛЫФенолформальдегидные смолы
- 36. ПРИМЕНЕНИЕ АЛЬДЕГИДОВПРОИЗВОДСТВО ВЕЩЕСТВУксусная кислотаЭтилацетатФормалин
- 37. Контрольные вопросыНайдите формулу альдегида: 2. Исключите лишнее
- 38. 6. Укажите формулу 2,3-диметилпентаналя:7. Общая формула гомологического
- 39. 9. Гидратацией какого алкина можно получить альдегид?
- 40. Ответы 1)б
- 41. СПАСИБО ЗА ВНИМАНИЕ!
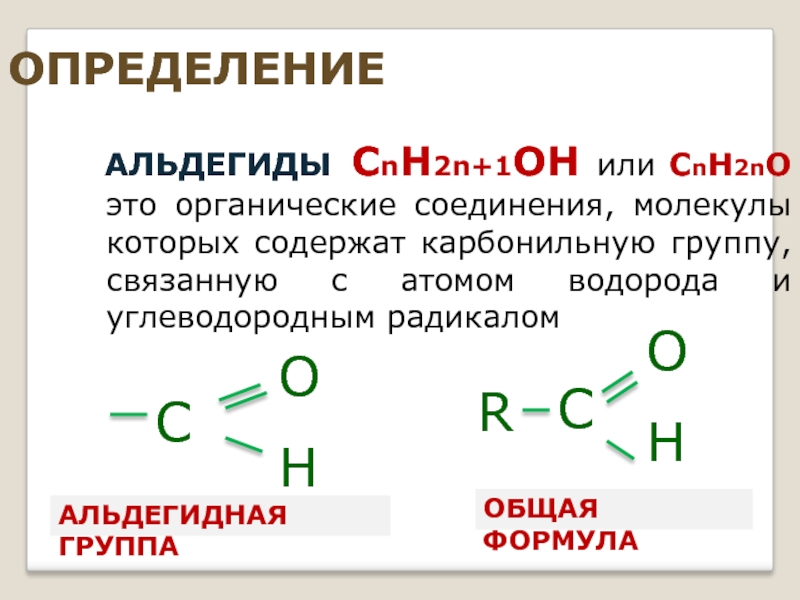
Слайд 2ОПРЕДЕЛЕНИЕ
АЛЬДЕГИДЫ СnH2n+1OН или СnH2nO это органические соединения, молекулы которых содержат
ОБЩАЯ ФОРМУЛА
АЛЬДЕГИДНАЯ ГРУППА
Слайд 3ОПРЕДЕЛЕНИЕ
КЕТОНЫ – органические вещества, в молекулах которых карбонильная группа связана с
С = О - кетогруппа
R1 – C – R2
||
O
Общая формула
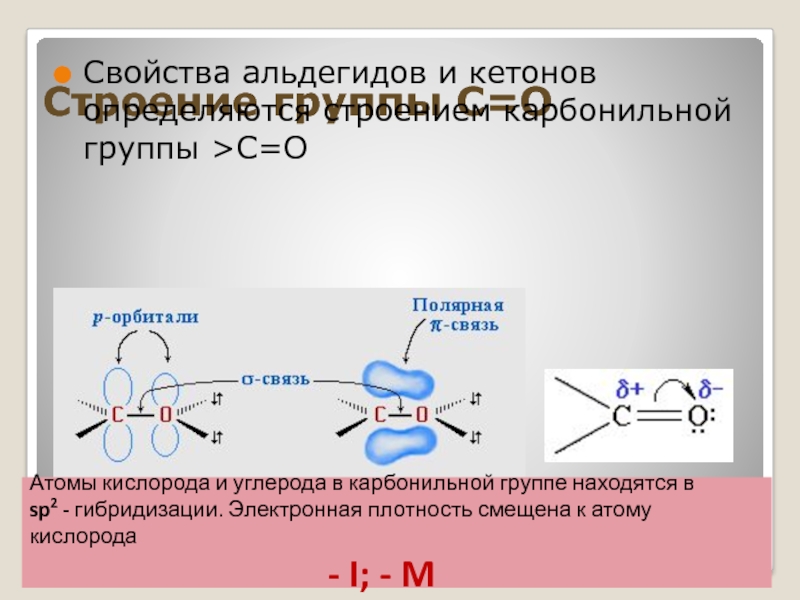
Слайд 4Строение группы С=О
Свойства альдегидов и кетонов определяются строением карбонильной группы >C=O
Атомы
sp2 - гибридизации. Электронная плотность смещена к атому кислорода
- I; - M
Слайд 8
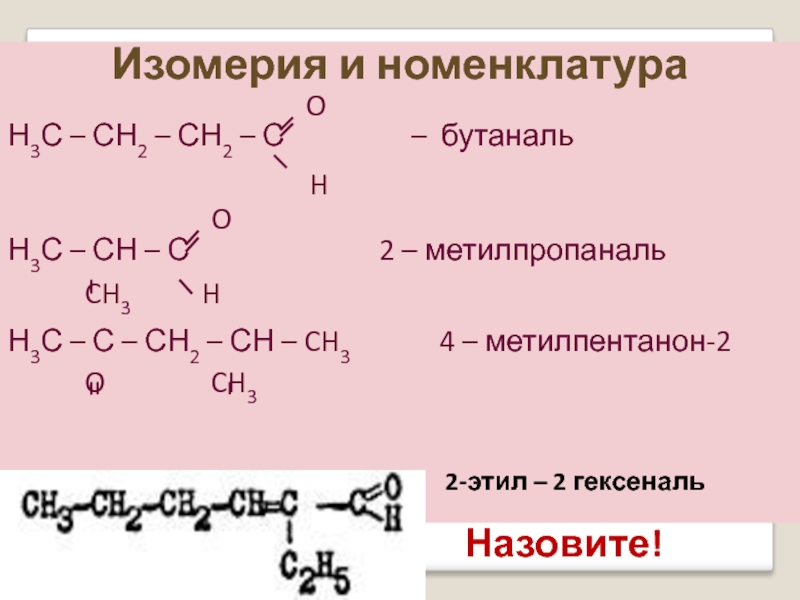
Изомерия и номенклатура
Н3С – СН2 – СН2 – С – бутаналь
H
O
Н3С – СН – С 2 – метилпропаналь
CH3 H
Н3С – С – СН2 – СН – CH3 4 – метилпентанон-2
O CH3
2-этил – 2 гексеналь
Назовите!
Слайд 9С1 – газ с резким запахом
С2 –
С4 – С6 – жидкости с неприятным запахом
>С6 – высшие (особенно непредельные или ароматические) – твердые, нерастворимые в воде с цветочным запахом
НСОН - формальдегид – газ с резким удушливым запахом, хорошо растворимый в воде, t кип. - 19,3С, ядовит. 40% раствор формальдегида называется формалином
СН3СОН – уксусный альдегид – жидкость с запахом зелёного яблока, растворимая в воде t кип. 21С
у этих альдегидов температуры кипения ниже, чем у соответствующих спиртов
Физические свойства альдегидов
Слайд 10Физические свойства кетонов
Кетоны — летучие жидкости. Кетоны обладают приятным запахом. Высшие
Пропонон ( диметилкетон) или ацетон
СН3 -С=О-СН3 – бесцветная жидкость с
резким запахом, tкип. 56,24С, хорошо
растворим в воде
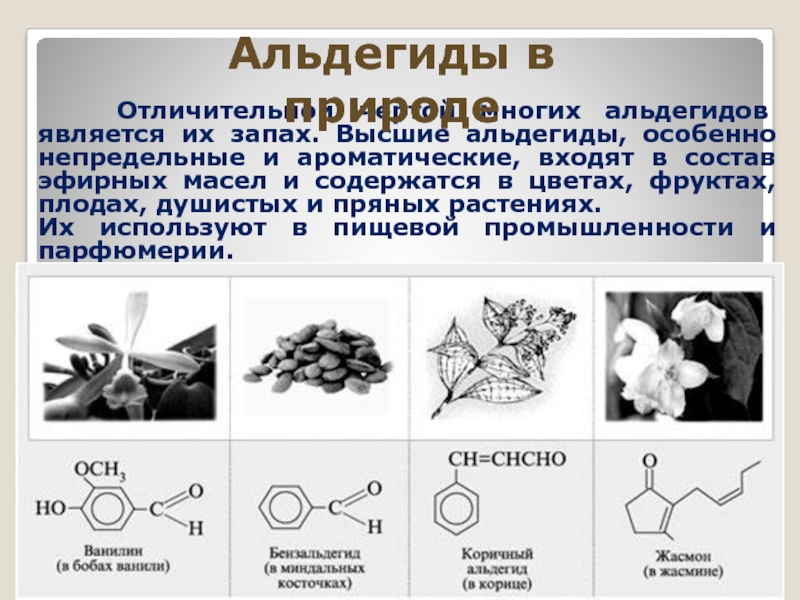
Слайд 11 Отличительной чертой многих альдегидов является их запах. Высшие альдегиды,
Их используют в пищевой промышленности и парфюмерии.
Альдегиды в природе
Слайд 12Булочки ванильные, корицы аромат,
Амаретто, шоколад
Альдегидов вкус таят.
В землянике и кокосе,
И в
И в духах, и в еде
Альдегидов след везде.
Что за запах, что за прелесть,
И откуда эта свежесть?!
Это высший альдегид
Аромат вам свой дарит!
Альдегиды в природе
Слайд 13 В плодах ванили содержится ароматический альдегид, который
Ванилин применяется в парфюмерии, кондитерской промышленности, для маскирования запахов некоторых продуктов
Ванилин
Альдегиды в природе
Слайд 14 Запах цитрусовых обусловлен данным диеновым альдегидом. Его применяют в
Цитраль
Альдегиды в природе
Слайд 15Коричный альдегид
Коричный альдегид содержится в масле корицы, его
Применяется в кулинарии в виде палочек или порошка
Альдегиды в природе
Слайд 16Бензальдегид
Бензальдегид – жидкость с запахом горького миндаля.
Встречается
Альдегиды в природе
Слайд 17Фенилэтаналь
Фенилэтаналь по сравнению с бензальдегидом лучше соответствует рецептору цветочного запаха.
Альдегиды в природе
Слайд 18n-Гидроксифенилбутанон-2
Этот кетон обуславливает в основном запах спелых ягод малины.
Его включают в состав синтетических душистых композиций
Кетоны в природе
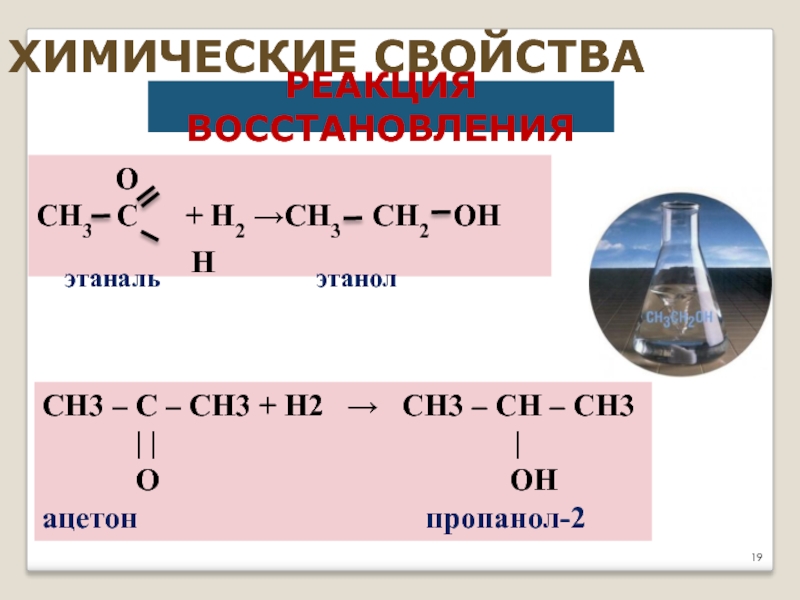
Слайд 19ХИМИЧЕСКИЕ СВОЙСТВА
РЕАКЦИЯ ВОССТАНОВЛЕНИЯ
О
СН3 С
этаналь Н этанол
CH3 – C – CH3 + H2 → CH3 – CH – CH3
| | |
O OH
ацетон пропанол-2
Слайд 20ХИМИЧЕСКИЕ СВОЙСТВА
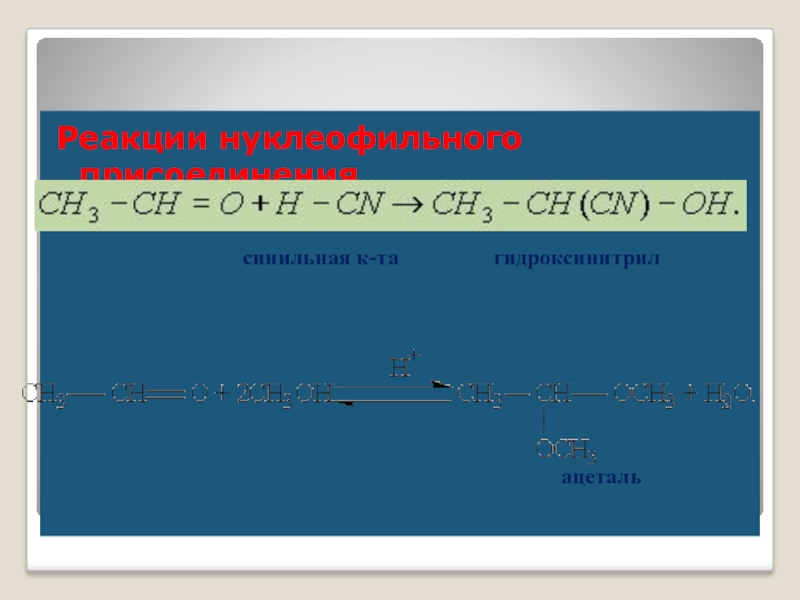
Реакции нуклеофильного присоединения
ацеталь
Слайд 21ХИМИЧЕСКИЕ СВОЙСТВА
Присоединение гидросульфитов
Гидросульфитные производные альдегидов
OH O
СН3 – С – SO3Na + HCl →CH3–C + NaCl + SO2↑ + H2O
H H
Реактив Гриньяра
Используя эту реакцию, из формальдегида получают первичный спирт, из любого другого альдегида – вторичный спирт, а из кетона третичный спирт
Слайд 22R – C = O + [O]
H OH
альдегид карбоновая кислота
О
Н-С + К2Сr2O7 + H2SO4→CO2 + Cr2(SO4)3 + K2SO4 + H2O
Н
НСООН - метановая (муравьиная) кислота
СН3СООН - этановая (уксусная) кислота
ХИМИЧЕСКИЕ СВОЙСТВА
РЕАКЦИИ ОКИСЛЕНИЯ
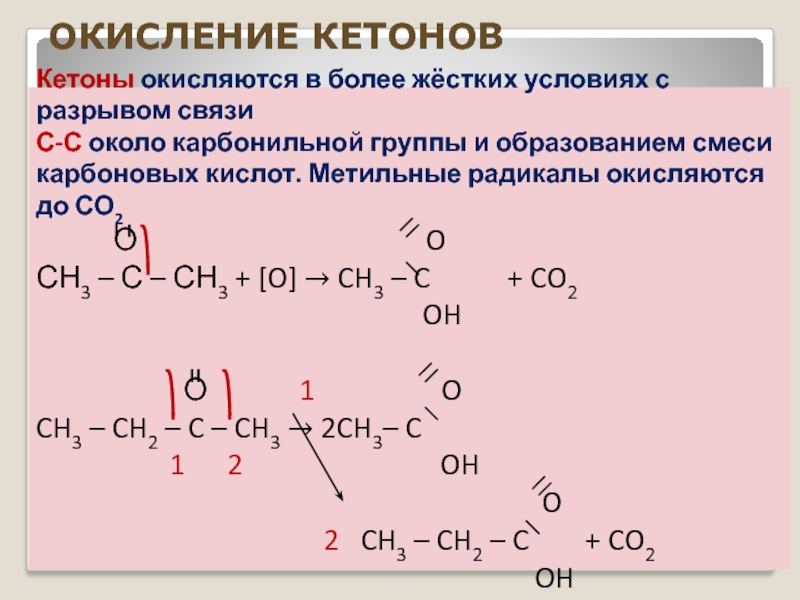
Слайд 23Кетоны окисляются в более жёстких условиях с разрывом связи
С-С около
карбоновых кислот. Метильные радикалы окисляются до СО2
О O
СН3 – С – СН3 + [O] → CH3 – C + CO2
OH
О 1 O
CH3 – CH2 – C – CH3 → 2CH3– C
1 2 OH
O
2 CH3 – CH2 – C + CO2
OH
ОКИСЛЕНИЕ КЕТОНОВ
Слайд 24ХИМИЧЕСКИЕ СВОЙСТВА
РЕАКЦИИ ОКИСЛЕНИЯ
Реакция серебряного зеркала- качественная реакция
СН3 С + 2[Ag(NH3)2]OH → СН3 С + Ag + 4NH3 + 2H2O
Н OН
О О
СН3 С + 2[Ag(NH3)2]OH → СН3 С + 2Ag + 3NH3 + 2H2O
Н ONH4
Слайд 25Реакция с гидроксидом меди качественная реакция
О
СН3 С + 2Cu(OH)2 → СН3 С + 2H2O + Cu2O этаналь Н этановая кислота OН гидроксид
меди (I)
(кирпично-красный)
РЕАКЦИИ ОКИСЛЕНИЯ
ХИМИЧЕСКИЕ СВОЙСТВА
Слайд 26
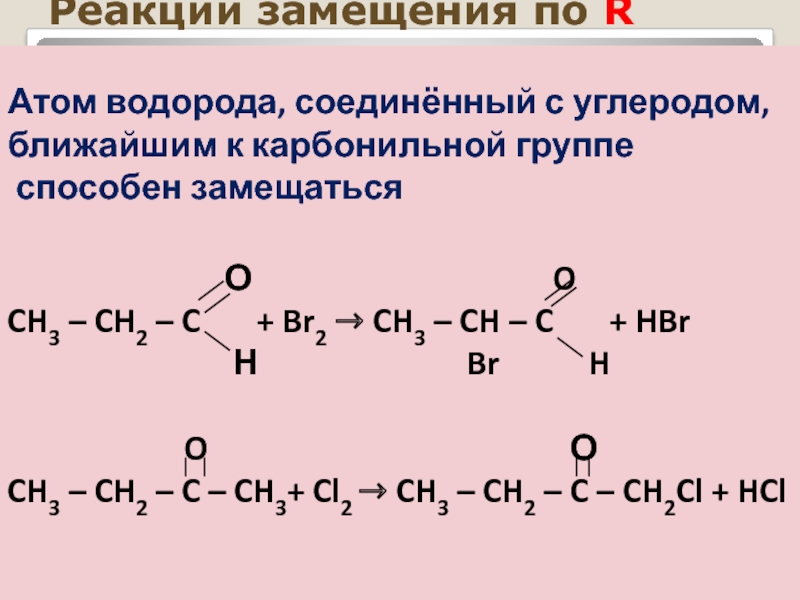
Атом водорода, соединённый с углеродом, ближайшим к карбонильной группе
способен замещаться
CH3 – CH2 – C + Br2 → CH3 – CH – C + HBr
Н Br H
O О
CH3 – CH2 – C – CH3+ Cl2 → CH3 – CH2 – C – CH2Cl + HCl
Реакции замещения по R
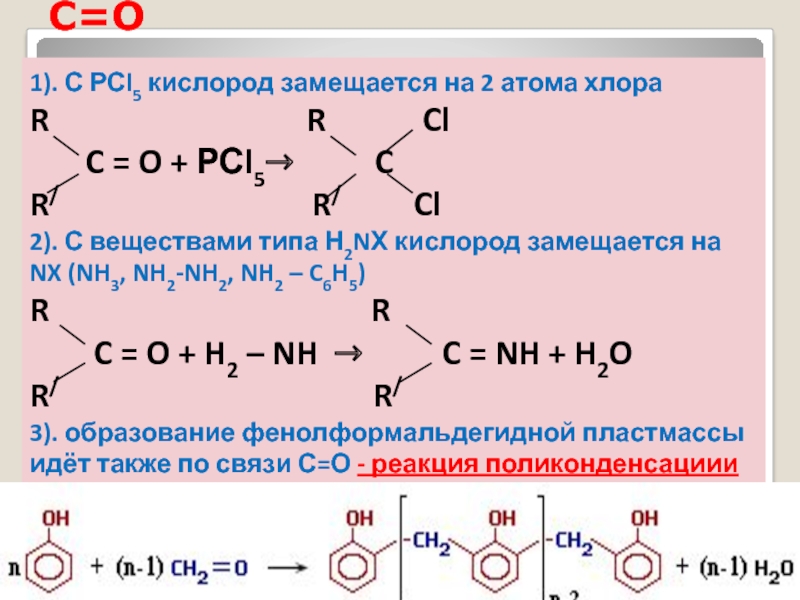
Слайд 27Реакции замещения по связи С=О
1). С РСl5 кислород замещается на 2
R R Cl
C = O + РСl5→ C
R/ R/ Cl
2). С веществами типа Н2NХ кислород замещается на NX (NH3, NH2-NH2, NH2 – C6H5)
R R
C = O + H2 – NH → C = NH + H2O
R/ R/
3). образование фенолформальдегидной пластмассы идёт также по связи С=О - реакция поликонденсациии
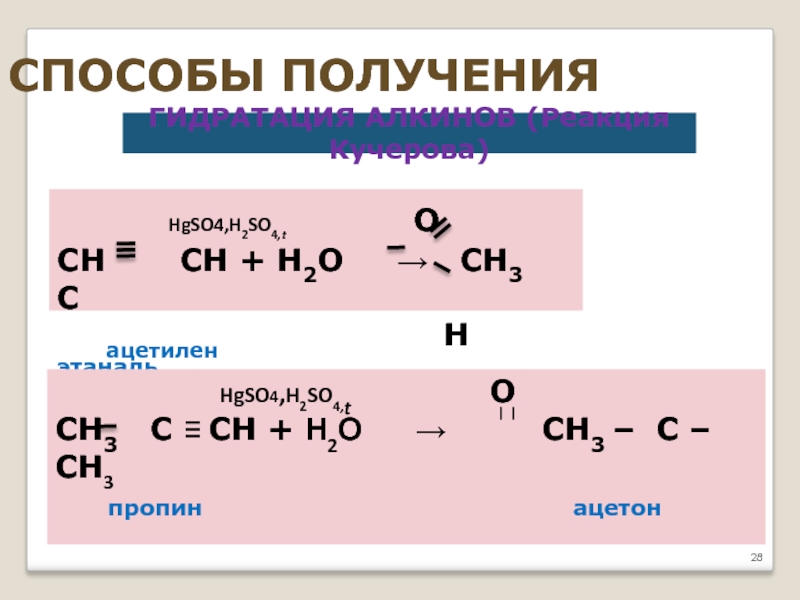
Слайд 28СПОСОБЫ ПОЛУЧЕНИЯ
ГИДРАТАЦИЯ АЛКИНОВ (Реакция Кучерова)
HgSO4,H2SO4,t
СН СН + Н2О → СН3 С
ацетилен Н этаналь
HgSO4,H2SO4,t O
СН3 С ≡ СН + Н2О → СН3 – С – СН3
пропин ацетон
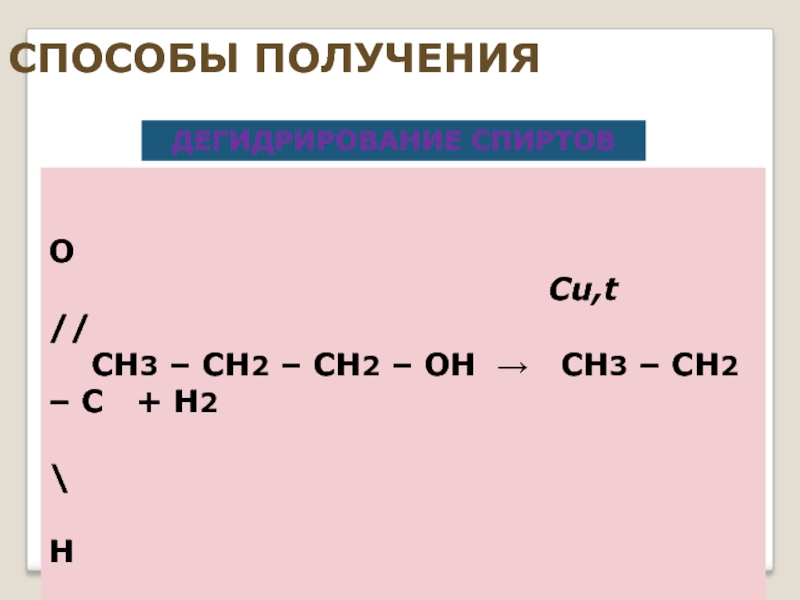
Слайд 29СПОСОБЫ ПОЛУЧЕНИЯ
ДЕГИДРИРОВАНИЕ СПИРТОВ
Cu,t //
CH3 – CH2 – CH2 – OH → СH3 – CH2 – C + H2
\
H
Cu,t
СH3 – CH – CH3 → CH3 – C – CH3 + H2
| | |
OH O
пропанон - 2 (ацетон)
Слайд 32 O
СН3
H
Cl
1,1- дихлорэтан этаналь
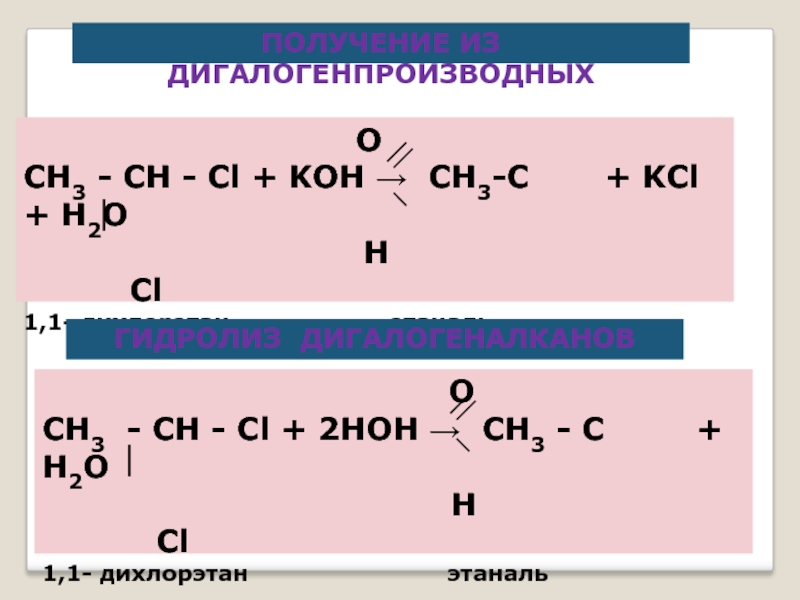
ПОЛУЧЕНИЕ ИЗ ДИГАЛОГЕНПРОИЗВОДНЫХ
O
СН3 - СН - Сl + 2НOH → СН3 - С + H2O
H
Cl
1,1- дихлорэтан этаналь
ГИДРОЛИЗ ДИГАЛОГЕНАЛКАНОВ
Слайд 33
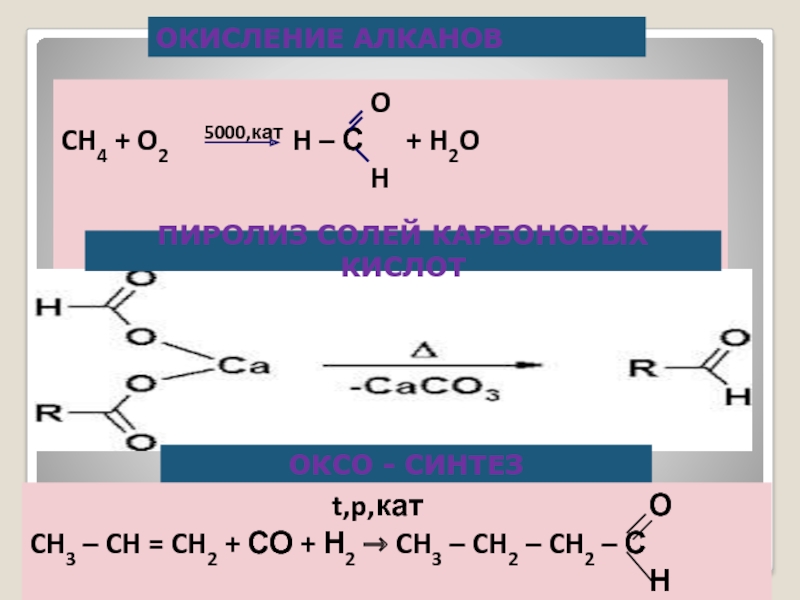
CH4 + O2 5000,кат H – С + H2O
H
ОКИСЛЕНИЕ АЛКАНОВ
ПИРОЛИЗ СОЛЕЙ КАРБОНОВЫХ КИСЛОТ
ОКСО - СИНТЕЗ
t,p,кат О
CH3 – CH = CH2 + СО + Н2 → CH3 – CH2 – CH2 – С
Н
Слайд 34ПРИМЕНЕНИЕ АЛЬДЕГИДОВ
ПАРФЮМЕРИЯ
Альдегид анисовый, обепин – жидкость с приятным запахом мимозы
Альдегид дециловый,
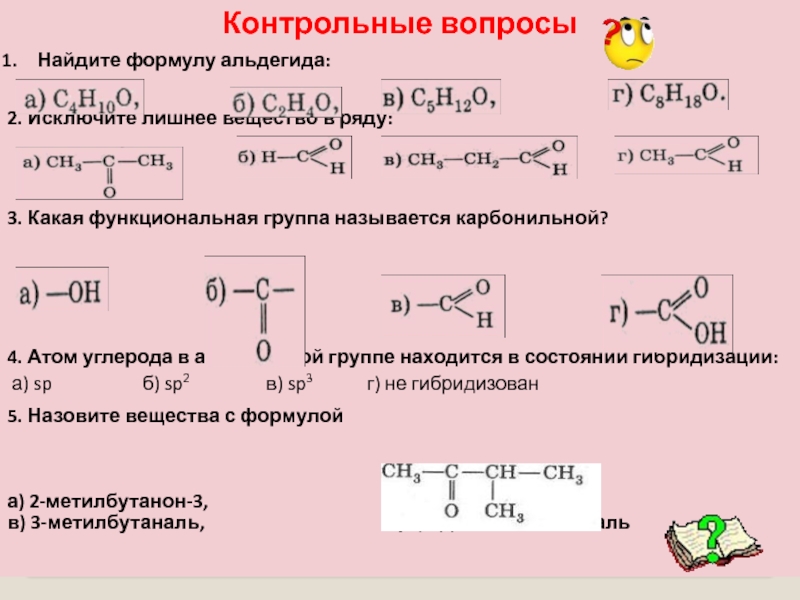
Слайд 37Контрольные вопросы
Найдите формулу альдегида:
2. Исключите лишнее вещество в ряду:
3. Какая
4. Атом углерода в альдегидной группе находится в состоянии гибридизации:
а) sp б) sp2 в) sp3 г) не гибридизован
5. Назовите вещества с формулой
а) 2-метилбутанон-3, б) 3-метилбутанон-2,
в) 3-метилбутаналь, г) 1,2-диметилпентаналь
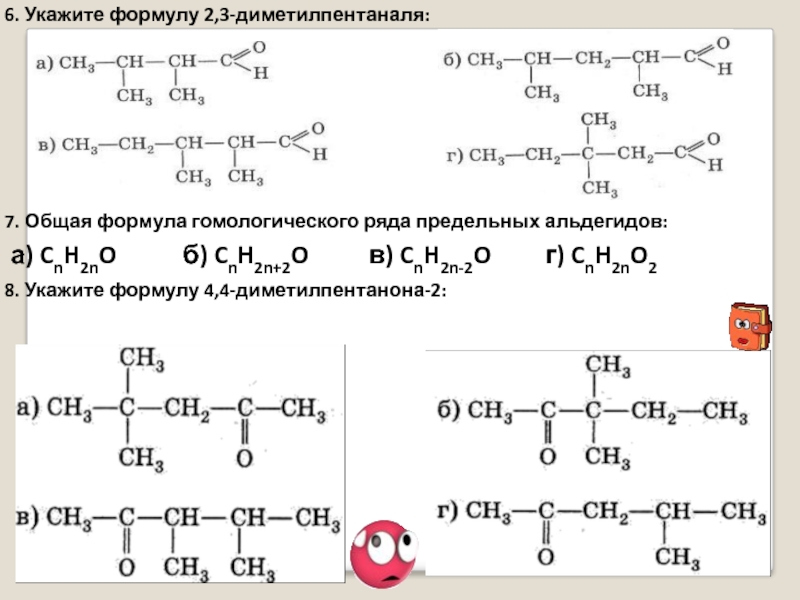
Слайд 386. Укажите формулу 2,3-диметилпентаналя:
7. Общая формула гомологического ряда предельных альдегидов:
а)
8. Укажите формулу 4,4-диметилпентанона-2:
Слайд 399. Гидратацией какого алкина можно получить альдегид? Напишите уравнение реакции, укажите
а) бутанол-2 б) 3-метилбутанол-2
в) 2-метилбутанол-2 г) 2-метилбутанол-1
10. Нагреваем соли ацетата кальция можно получить:
а) метаналь б) этаналь в) пропаналь г) пропанон
11. Какие признаки верно отражают физические свойства метаналя: 1) бесцветная жидкость, 2) газообразное вещество, 3) имеется характерный запах, 4) плохо растворим в воде, 5) молекула полярная.
а) 1, 3, 4 б) 2, 3, 5 в) 3, 4, 5 г) 2, 4, 5
12. Какая из реакций носит имя М. Г. Кучерова.
а) гидратация ацетилена б) тримеризация ацетилена
в) гидрирование ацетилена г) бромирование ацетилена












![Презентация по химии на тему Альдегиды и кетоны R – C = O + [O] → R – C = O + [O] →](/img/tmb/1/61596/8ab318b2a23ef0b5080ca4552bc28297-800x.jpg)