- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Электролитическая диссоциация
Содержание
- 1. Презентация по химии Электролитическая диссоциация
- 2. Электролитическая диссоциация
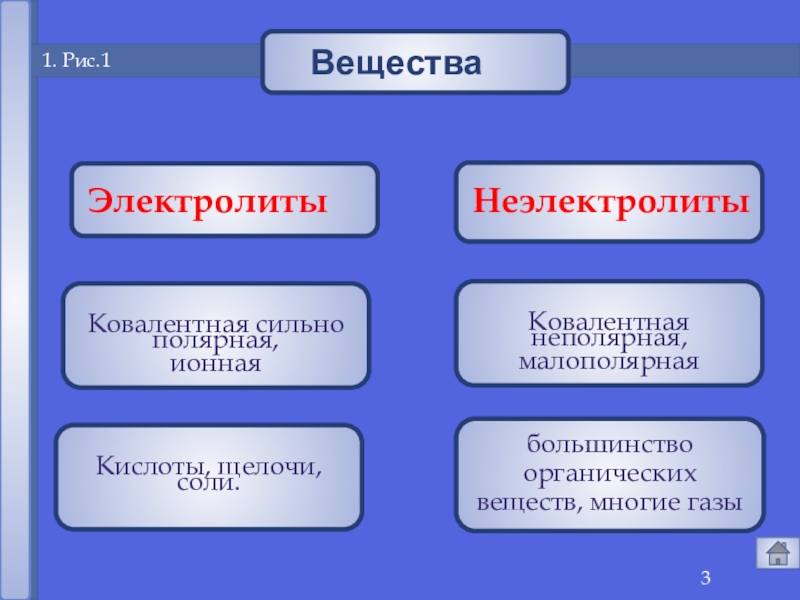
- 3. 1 1. Рис.1ЭлектролитыНеэлектролиты
- 4. «Капля воды и камень точит» 1.
- 5. 1. Электролиты и неэлектролитыэто вещества, растворы и расплавы которыепроводят электрический ток.Электролиты -
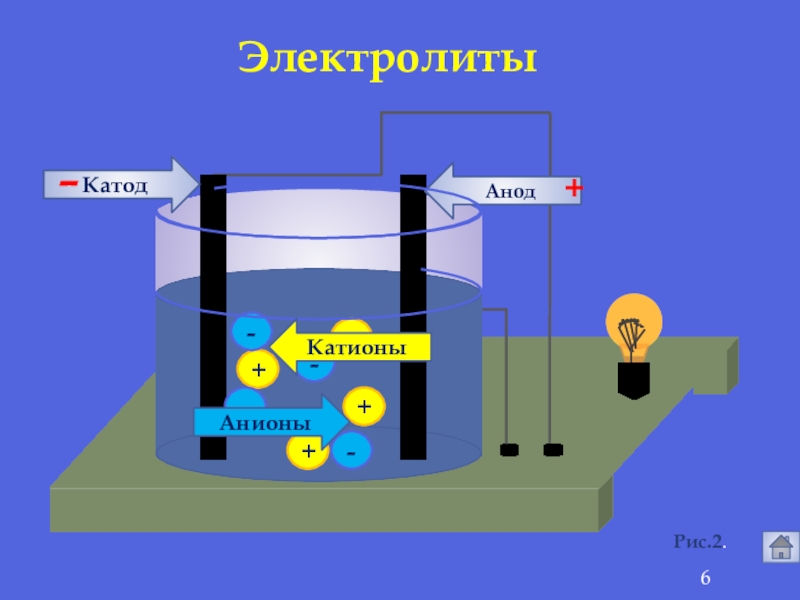
- 6. ++++----АнионыКатионыАнодКатод-+Электролиты Рис.2.
- 7. 1. Электролиты и неэлектролитыэто вещества, растворы
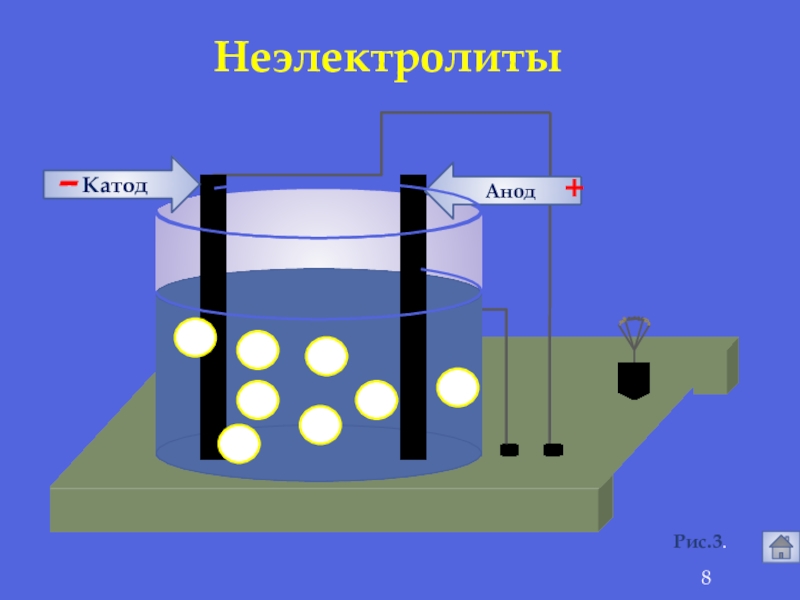
- 8. АнодКатод-+Рис.3.Неэлектролиты
- 9. «Честь науке- ей дано уменье, выводить нас
- 10. «Честь науке- ей дано уменье, выводить нас
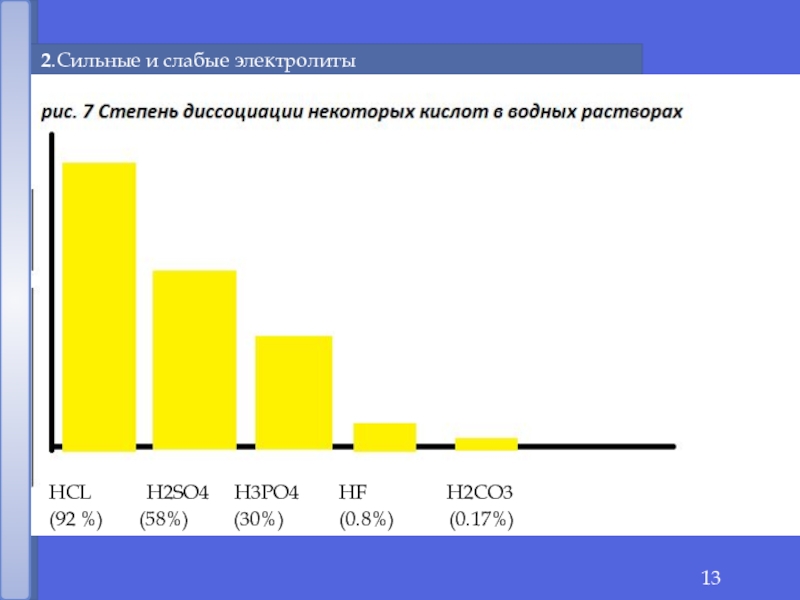
- 11. 2.Сильные и слабые электролитыHCl+++Сильные и слабыеРис.6.
- 12. отношение числа диссоциированных молекул к общему числу
- 13. 2.Сильные и слабые электролиты%НСL
- 14. Слайд 14
- 15. Слайд 15
- 16. Слайд 16
- 17. 6. О значении электролитов для
- 18. 6. Рис.8. Характерные симптомы дефицита химических элементов в организме человека подробнее
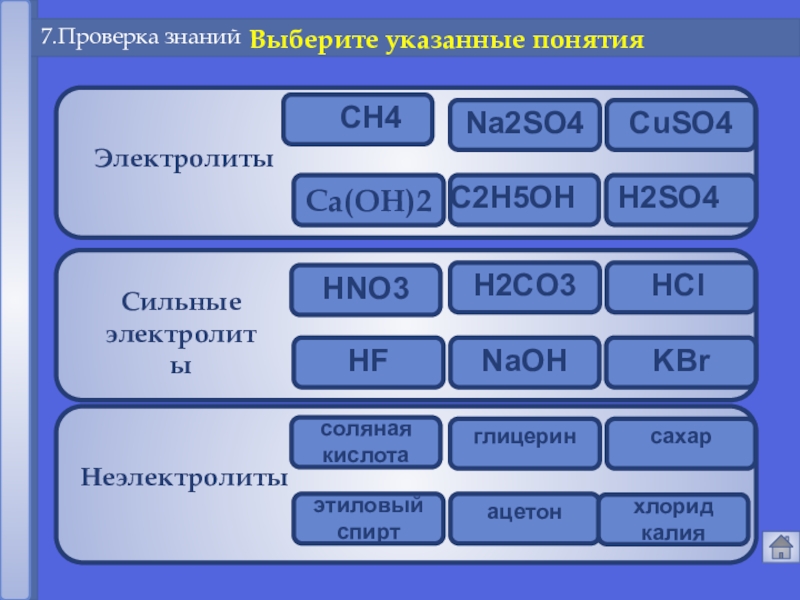
- 19. Сильные электролитыCa(OH)2ЭлектролитыНеэлектролиты 7.Проверка знаний Выберите указанные понятия
- 20. Электролитическая диссоциация 7. Проверка знанийЭлектролитическая диссоциация в
- 21. Литература Баженов А.А. Мастер-класс «Создание презентаций к
Слайд 4
«Капля воды и камень точит»
1. Электролиты и неэлектролиты
Вода –
хороший растворитель,
т.к. молекулы воды полярны.
слабый амфотерный электролит.
ион
гидроксония
Вода –
Слайд 5
1. Электролиты и неэлектролиты
это вещества, растворы и расплавы которые
проводят
Электролиты -
Слайд 7
1. Электролиты и неэлектролиты
это вещества, растворы или расплавы которые не
проводят
Неэлектролиты -
Органические вещества:
сахар, ацетон,бензин, керосин, глицерин, этиловый спирт, бензол и др.
Газы: кислород, водород, азот идр.
Слайд 9
«Честь науке- ей дано уменье, выводить нас из заблужденья». М.Светлов
процесс распада молекул электролита на ионы в растворе или расплаве.
С.Аррениус
Электролитическая диссоциация -
Теория электролитической диссоциации. 1887 г.
Слайд 10
«Честь науке- ей дано уменье, выводить нас из заблужденья».
Кратко об
Аррениусе Сванте
Августе
Шведский ученый, академик.
В 1887 году сформулировал основные положения теории электролитической диссоциации.
В 1903 г. награжден Нобелевской премией.
Проводил исследования во многих других областях науки.
С.Аррениус
(1859 – 1927)
Слайд 12
отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе.
Степень электролитической
диссоциации (α) -
α =
n
N
Слайд 14
Кислоты -
Диссоциация кислот
Н2 CO3 2 + CO3
Н
5. Диссоциация кислот, оснований, солей
Слайд 15
Основания -
Диссоциация оснований
OН
Мe(OH)n Me +
Слайд 16
это сложные вещества,
которые в водных растворах диссоциируют на катионы металла и анионы кислотного остатка.
Соли -
Диссоциация солей
Al(NO3)3 → + 3
Na
Слайд 17
6. О значении электролитов для живых организмов
Электролитическая диссоциация
Электролиты – составная часть жидкостей и плотных тканей живых организмов.
Ионы Na+,K+,Ca2+,Mg2+,H+; имеют большое значение для физиологических и биохимических процессов:
ионы H+; OH- играют большую роль в работе ферментов, обмене веществ, переваривании пищи и др.
при нарушении водно-солевого обмена в медицине применяется физиологический раствор – 0,85% раствор NaCl;
ионы I - влияют на работу щитовидной железы.
НCO3-
Слайд 18
6. Рис.8. Характерные симптомы дефицита химических элементов в организме человека
подробнее
Слайд 19
Сильные электролиты
Ca(OH)2
Электролиты
Неэлектролиты
7.Проверка знаний
Выберите указанные понятия
Слайд 20
Электролитическая диссоциация
7. Проверка знаний
Электролитическая диссоциация
в растворах – это процесс
Электролитическая диссоциация электролитов в растворах протекает под действием __________ .
Слабым электролитом является _______ .
Электролитами не являются ________ .
Под каким действием протекает электролитическая диссоциация
Слайд 21
Литература
Баженов А.А. Мастер-класс «Создание презентаций к урокам химии»..
http://www.it-ru/communities.aspx?cat_no=75761&tmpl=com
Рудзитис Г.Е.,
http://www.alhimik.ru/kunst/man's_elem.html
Благодарю за внимание!