Работу выполнила учитель географии и биологии
МБОУ «СОШ» пст. Якуньёль
Козлова С.А.
29.09.2016г
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 8 класс шпаргалка для учащихся
Содержание
- 1. Презентация по химии 8 класс шпаргалка для учащихся
- 2. Основные термины:Химическими реакциями называются явления, в процессе
- 3. Химические элементы редко встречаются в природе в
- 4. Классификация и физические свойства простых веществ.Простые вещества
- 5. Сравнение понятий «химический элемент» и «простое вещество»Признаки
- 6. Li36,9410,98ЛитийПорядковый номер Относительная атомная масса Электроотрицательность по Полингу Символ элемента Название элемента
- 7. Простые веществаВещества, которые состоят из атомов одного
- 8. Качественный состав- атомы каких элементов входят в
- 9. Сложные веществаООННОСН2ОСО2состоят из атомов разных химических элементовиндексы11Химическая
- 10. Н - один атом водорода2Н -
- 11. BaOCO₂Al₂O₃FeCl₃Na₂CO₃Заполните таблицу:1 атом бария1 атом кислорода1 атом
- 12. 3BaO2CO₂5Al₂O₃4FeCl₃Na₂CO₃325412 атома натрия1 атом углерода3 атома кислорода3
- 13. Масса молекулярнаяПонятие относительное.Смысл её физическийСовсем не удивительный.Массу
- 14. Mr(Na₂O) = 2 · Ar(Na) + Ar(O)
- 15. Структурная формулаМолекулярная формула171412162427283132401111111777712121212121414141414161616161616161616242424242727272727272828282828313131313132323232324040404040ответ5656Fe3(PO4)256161616Ортофосфат железа (ii)
- 16. Mr(Fe3(PO4)2)= 56·3+(31+16·4) ·2 =358или так Mr(Fe3(PO4)2)= 56·3+31·2+16·8 =358
- 17. Относительная молекулярная массаМr(Н2О) = 2∙Ar(H) + A
- 18. Закон постоянства состава
- 19. Слайд 19
- 20. Задачи о веществеРасчёт массовой доли ω (
- 21. Нахождение молекулярной формулы веществаПо известному содержанию составляющих
- 22. Слайд 22
Слайд 1Химия для начинающих или что ты должен знать в 1 полугодии
Слайд 2Основные термины:
Химическими реакциями называются явления, в процессе которых происходит образование новых
Агрегатное состояние- три состояния веществ( жидкое, твёрдое и газообразное).
Атом – наименьшая (неделимая химическим путем) часть элемента, сохраняющая все свойства.
Составная часть вещества, содержащая одинаковые атомы, называется химическим элементом- иначе, совокупность атомов определённого вида.
Простое вещество – состоит из атомов одного химического элемента.
Сложное вещество – состоит из атомов разных химических элементов
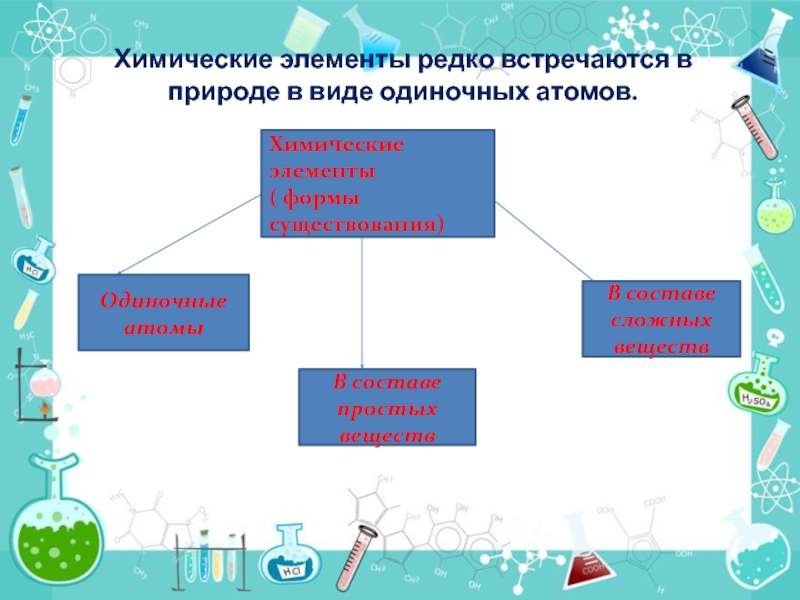
Слайд 3Химические элементы редко встречаются в природе в виде одиночных атомов.
Одиночные атомы
В составе простых
веществ
В составе сложных веществ
Химические элементы
( формы существования)
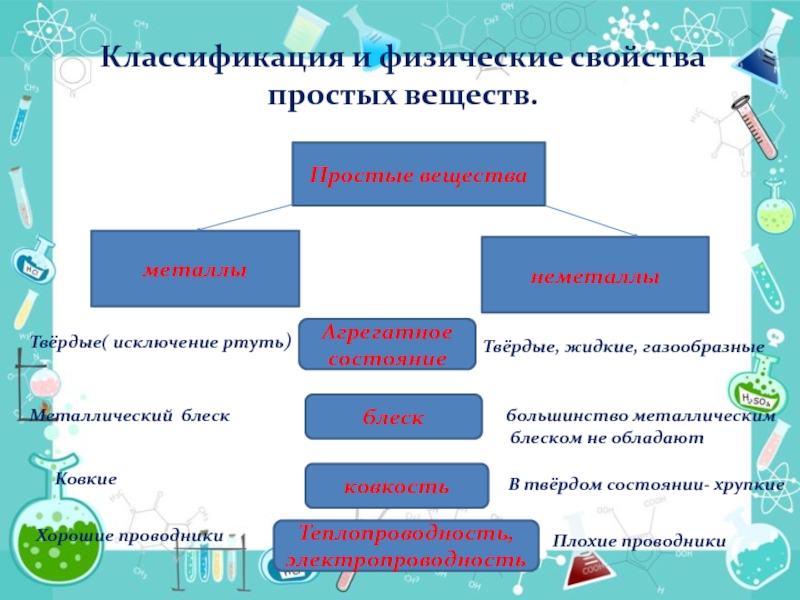
Слайд 4Классификация и физические свойства простых веществ.
Простые вещества
металлы
неметаллы
Агрегатное состояние
блеск
ковкость
Теплопроводность, электропроводность
Твёрдые( исключение ртуть)
Твёрдые, жидкие, газообразные
Металлический блеск
большинство металлическим
блеском не обладают
Ковкие
В твёрдом состоянии- хрупкие
Хорошие проводники
Плохие проводники
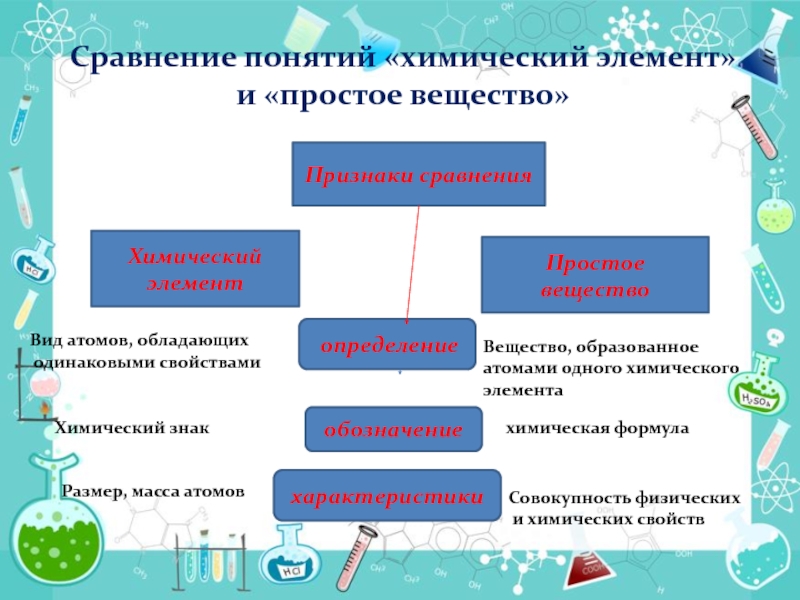
Слайд 5Сравнение понятий «химический элемент» и «простое вещество»
Признаки сравнения
Химический элемент
Простое вещество
определение
обозначение
характеристики
Вид атомов, обладающих
одинаковыми свойствами
Вещество, образованное атомами одного химического
элемента
Химический знак
химическая формула
Размер, масса атомов
Совокупность физических
и химических свойств
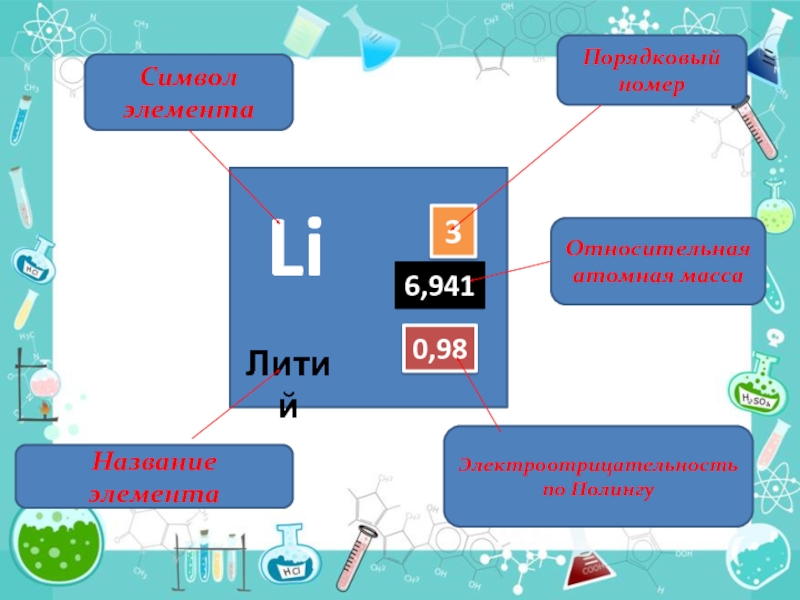
Слайд 6Li
3
6,941
0,98
Литий
Порядковый номер
Относительная атомная масса
Электроотрицательность по Полингу
Символ элемента
Название
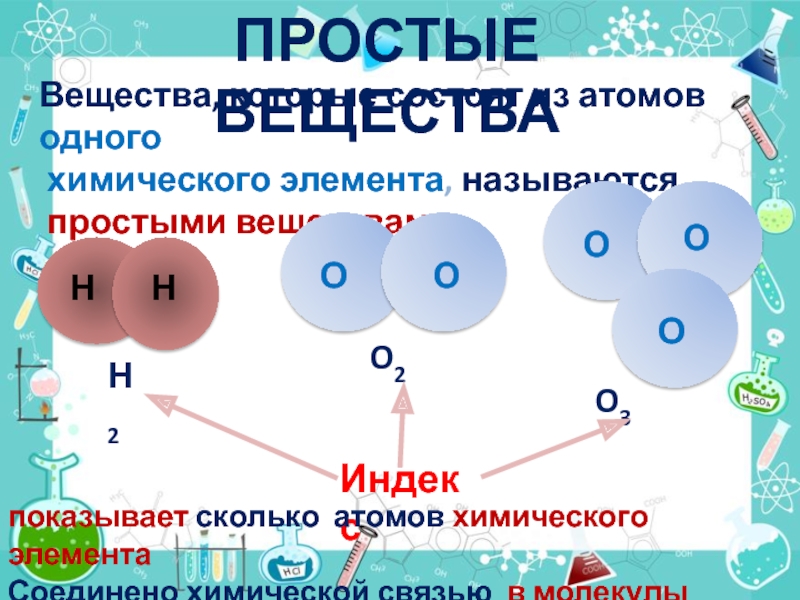
Слайд 7Простые вещества
Вещества, которые состоят из атомов одного
химического элемента, называются
простыми
Н
Н
Н2
О
О
О
O2
O3
О
О
Индекс
показывает сколько атомов химического элемента
Соединено химической связью в молекулы
Слайд 8Качественный состав- атомы каких элементов входят в состав молекулы
Вывод - простое
Количественный состав – сколько
атомов каждого элемента входят в состав молекулы
Для нахождения относительной молекулярной массы
Слайд 9Сложные вещества
О
О
Н
Н
О
С
Н2О
СО2
состоят из атомов разных химических элементов
индексы
1
1
Химическая формула показывает, атомы каких
соединены между собой
Слайд 10 Н - один атом водорода
2Н - два атома водорода
5О -
коэффициент
1
Н2О - одна молекула воды
2Н2О - две молекулы воды
5О2 - пять молекул кислорода
коэффициент
1
Что означает запись?
4Н2О - четыре молекулы воды; в состав каждой
входит два атома водорода и один атом кислорода
5N2 - пять молекул азота; в состав каждой входит
два атома азота
Слайд 11BaO
CO₂
Al₂O₃
FeCl₃
Na₂CO₃
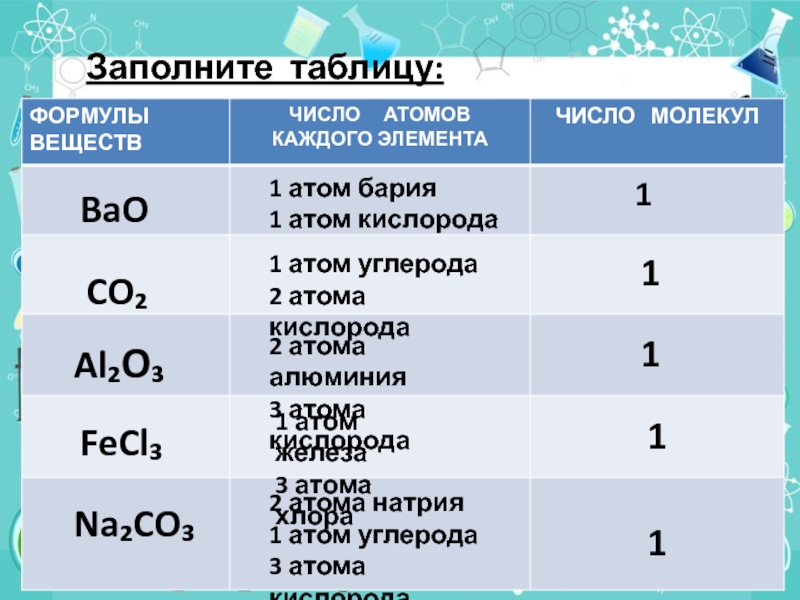
Заполните таблицу:
1 атом бария
1 атом кислорода
1 атом углерода
2 атома кислорода
2 атома
3 атома кислорода
1 атом железа
3 атома хлора
2 атома натрия
1 атом углерода
3 атома кислорода
1
1
1
1
1
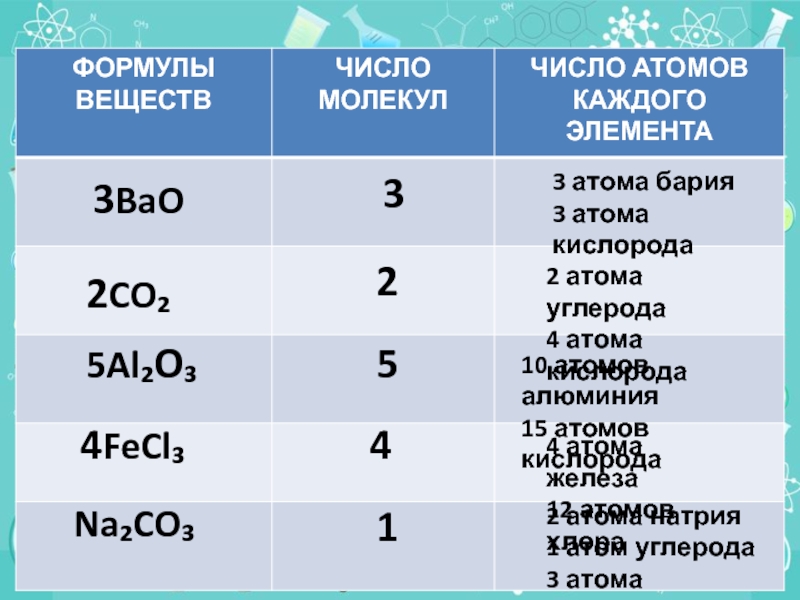
Слайд 123BaO
2CO₂
5Al₂O₃
4FeCl₃
Na₂CO₃
3
2
5
4
1
2 атома натрия
1 атом углерода
3 атома кислорода
3 атома бария
3 атома кислорода
2
4 атома кислорода
10 атомов алюминия
15 атомов кислорода
4 атома железа
12 атомов хлора
Слайд 13Масса молекулярная
Понятие относительное.
Смысл её физический
Совсем не удивительный.
Массу чтоб молекулы быстренько сравнить,
m (в-ва)
Mr (в-ва)= ------------------
1/12 m (C)
Ты молекулярную
Массу рассчитай:
Атомные массы
Вместе все слагай
И на число атомов
При этом умножай.
Mr
Слайд 14Mr(Na₂O) = 2 · Ar(Na) + Ar(O) = 2 · 23
Mr(H₂SO₄) = 2 · 1 + 32 + 4 · 16 = 98
?
?
?
РАСЧИТАЙТЕ ОТНОСИТЕЛЬНЫЕ
МОЛЕКУЛЯРНЫЕ МАССЫ :
Mr( H₂O) = ?
Mr( NaCl) = ?
Mr(H₂O) = 2 · 1 + 16 = 18
Mr(NaCl) = 23 + 35,5 = 58,5
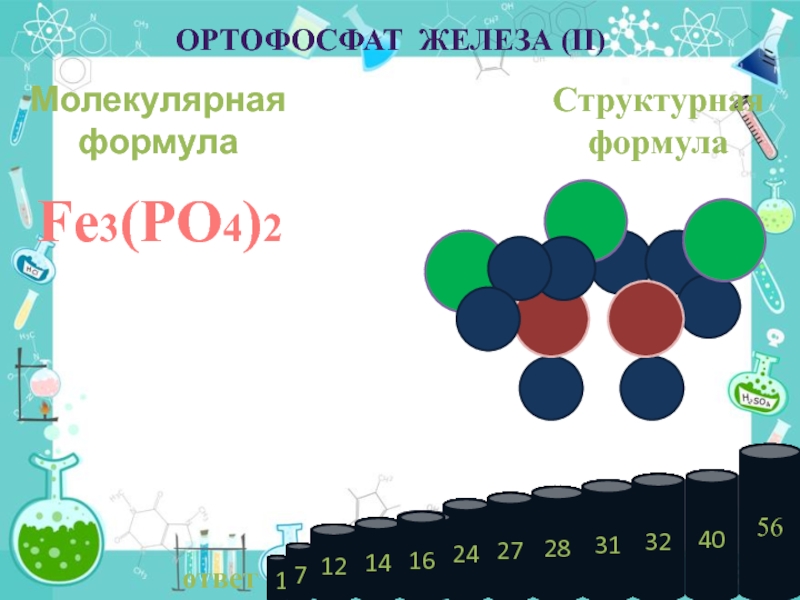
Слайд 15Структурная
формула
Молекулярная
формула
1
7
14
12
16
24
27
28
31
32
40
1
1
1
1
1
1
1
7
7
7
7
12
12
12
12
12
14
14
14
14
14
16
16
16
16
16
16
16
16
16
24
24
24
24
27
27
27
27
27
27
28
28
28
28
28
31
31
31
31
31
32
32
32
32
32
40
40
40
40
40
ответ
56
56
Fe3(PO4)2
56
16
16
16
Ортофосфат железа (ii)
Слайд 17Относительная молекулярная масса
Мr(Н2О) = 2∙Ar(H) + A r(O) = 2∙1 +
Мr(Н2SО4) = 2∙1 + 32 + 16∙4 = 98
Мr(Al2О3) = 2∙27 + 3∙16 = 102
Мr(CO2) = 12 + 16∙2 = 44
Мr(N2O) = 2∙14 + 16 = 44
Слайд 18Закон постоянства состава
Был открыт французским
всякое чистое вещество (химическое соединение), каким бы путем оно ни было получено, имеет строго определенный и постоянный состав (качественный и количественный).
Слайд 19
Из каких атомов
состоит это вещество?
Найдите атомные
массы серы и железа.
FeS
На основе закона
постоянства состава
можно производить
различные расчеты
Слайд 20Задачи о веществе
Расчёт массовой доли ω ( омега) химического элемента по
Задача. Рассчитать массовые доли элементов в сульфате меди по формуле CuSO4
Решение. Дано: CuSO4 Найти: ωCu - ?; ωS - ?; ωO - ?.
Подсчитываем относительную молекулярную массу сульфата меди.
MrCuSO4 = 64•1+32•1+16•4 = 160
2. Приняв массу всей молекулы за 100% и составив пропорции, рассчитываем массовые доли всех элементов вещества:
Массовые доли меди, серы и кислорода обозначим соответственно через x, y, и z.
160:100% = 64:х% 160:100% = 32:y% 160:100% = 64:z%
x= 100%•64 = 40% y= 100%•32 = 20% z= 100%•64 = 40%
160 160 160
Ответ: ωCu = 40%; ωS= 20%; ωO = 40%
Слайд 21Нахождение молекулярной
формулы вещества
По известному содержанию составляющих его элементов
В задачах
Рассмотрим пример: Задача. Органическое вещество содержит углерод 84,21% и водород 15,79%. Плотность паров по воздуху составляет 3,93. Определите формулу вещества.
Дано: ωC = 84, 21%; ωH = 15,79%; Dвозд = 3,93; Найти: Cx Hy.
Решение: Что такое массовая доля? Это – доля от целой массы. В нашем случае – это
ωC = X · ArC : Mr(CxHy); ωH = Y · ArH : Mr(CxHy)
Выразим из этих уравнений X и Y и возьмём их соотношение:
x = ωC · M(CxHy) : ArC y = ωH · M(CxHy) : ArH
X : Y = ωC · ωH = 84,21 · 15,79 = 7,0175 : 15,79 = 1 : 2,25 = 4 : 9 Простейшая формула: C4H9
ArC · ArH 12 · 1
Поскольку вещества с такой формулой не существует, обратимся к данной в условии относительной плотности по воздуху:
Dвозд = M(CxHy) : Mвозд M(CxHy) = Dвозд · Mвозд = 3,93 · 29г/моль = 114г/моль
M(C4H9) = 57, что в 2 раза меньше M(CxHy)/ Значит истиная формула искомого вещества содержит атомов углерода и атомов водорода в 2 раза больше чем простейшая
C4H9 · 2 = C8H18 Это – октан.
Ответ: Формула вещества C8H18