- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку серная кислота
Содержание
- 1. Презентация к уроку серная кислота
- 2. Цели урока:1.Знать физические, химические свойства и области
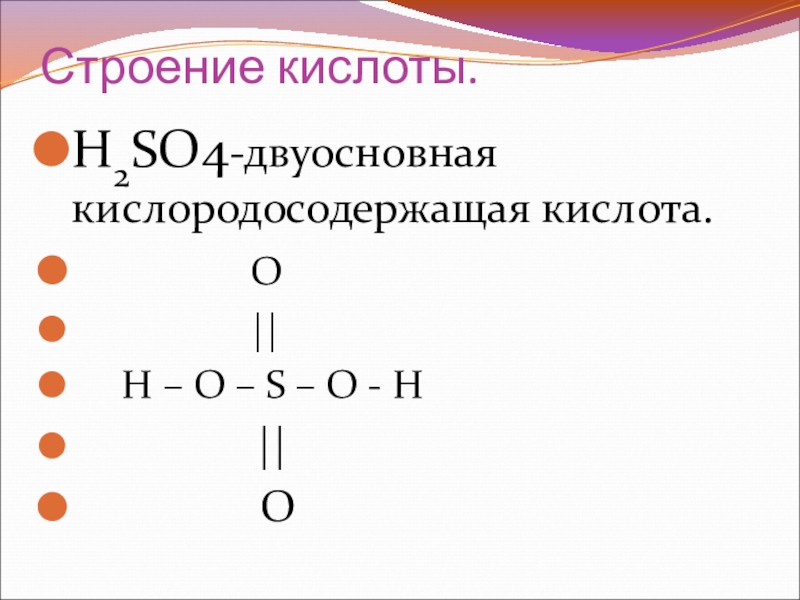
- 3. Строение кислоты. Н2SO4-двуосновная кислородосодержащая кислота.
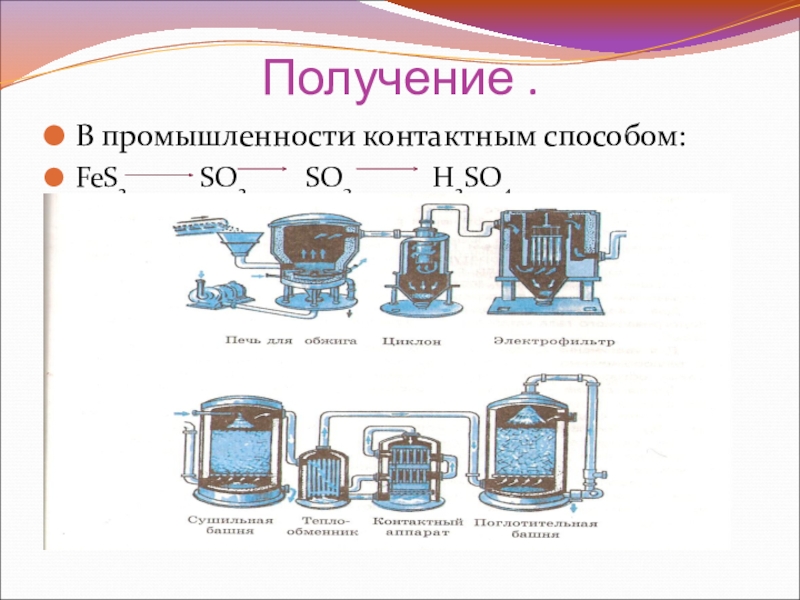
- 4. Получение .В промышленности контактным способом:FeS2
- 5. Физические свойства.1.Бесцветная маслянистая жидкость.2.Жадно поглощает воду.3.Обугливает органические вещества. 4. При растворении образует гидраты.
- 6. Слайд 6
- 7. Разбавление серной кислоты.
- 8. Химические свойства.1.Диссоциация на ионы.2.Взаимодействие с основными оксидами.3.Нейтрализация
- 9. Слайд 9
- 10. Слайд 10
- 11. Качественная реакция на кислоту .Проделать опыт на определение катиона и аниона.
- 12. Соли серной кислоты.СаSO4 - сульфаты.Са(НSO4)2 - гидросульфаты.
- 13. Применение солейСоли серной кислоты. В строительстве и
Цели урока:1.Знать физические, химические свойства и области применения серной кислоты.2.Уметь составлять уравнения отражающие химические свойства кислоты, объяснять особенности кислоты.3.Воспитание соблюдения техники безопасности при работе с кислотой.
Слайд 2Цели урока:
1.Знать физические, химические свойства и области применения серной кислоты.
2.Уметь составлять
уравнения отражающие химические свойства кислоты, объяснять особенности кислоты.
3.Воспитание соблюдения техники безопасности при работе с кислотой.
3.Воспитание соблюдения техники безопасности при работе с кислотой.
Слайд 5Физические свойства.
1.Бесцветная маслянистая жидкость.
2.Жадно поглощает воду.
3.Обугливает органические вещества.
4. При растворении
образует гидраты.
Слайд 8Химические свойства.
1.Диссоциация на ионы.
2.Взаимодействие с основными оксидами.
3.Нейтрализация основаниями.
4. .Взаимодействие с солями
более слабых кислот.
5. .Взаимодействие H2SO4 ( разб) с активными металлами.
6. Взаимодействие H2SO4 ( концен ) с медью, серебром, ртутью.
5. .Взаимодействие H2SO4 ( разб) с активными металлами.
6. Взаимодействие H2SO4 ( концен ) с медью, серебром, ртутью.
Слайд 13Применение солей
Соли серной кислоты. В строительстве и в медицине широко используют
полуводный гипс, получаемый при обжиге горной породы (дигидрат сульфата кальция). Будучи смешан с водой, он быстро застывает, образуя дигидрат сульфата кальция, то есть гипс.
Декагидрат сульфата натрия используют в качестве сырья для получения соды.