- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку по химии на тему Окислительно-восстановительные реакции (9 класс)
Содержание
- 1. Презентация к уроку по химии на тему Окислительно-восстановительные реакции (9 класс)
- 2. Загадка 1Два антипода пáрою ходят – Первый
- 3. Слайд 3
- 4. Слайд 4
- 5. Изменение восстановительных свойств в Периодической таблице В
- 6. Задание1.Дайте определения понятиям «окислитель» и «восстановитель».2. Какой
- 7. Ответ 1Атомы, ионы или молекулы, принимающие электроны,
- 8. Ответ 2Атомы, ионы или молекулы, отдающие электроны,
- 9. Ответ 3Если элемент находится в промежуточной степени
- 10. Задание 2Из перечня, приведенного ниже, выпишите отдельно
- 11. Ответ 2Окислители: КМnO4, К2Cr2О7, НNO3,
- 12. Практическая работа (задание 3)Используя имеющиеся реактивы
- 13. Вопрос Какой из этих процессов окислительно – восстановительный?
- 14. ОтветСаО + Н2О = Са(ОН)2, реакция
- 15. Слайд 15
- 16. 4. Литературный вопрос«По берегам ледяных и шумливых
- 17. Вопросы и задания Что произошло с пиритом? Запишите уравнение реакции.
- 18. ОтветПирит окислился:4FeS2 + 11O2 = 2Fe2O3 + 8SO2↑http://freethoughtblogs.com/entequilaesverdad/files/2012/10/DSC05330-884x1024.jpg
- 19. 5. Литературно-практический вопрос«Пожар пылал несколько часов подряд.
- 20. Вопросы и заданияКакие процессы произошли в пещере?
- 21. Ответ СаСО3 = CаО + СО2↑,СаО +
- 22. 6. Практическая работаВ начале XIX в. Б.Куртуа
- 23. Вопросы и заданияКак называется это вещество? Используя
- 24. ОтветВещество – это йод.Варианты реакций, в результате
- 25. 7.Литературный вопрос…Трясся Крым двадцать восьмого годаИ вставало
- 26. Вопросы и задания Запишите уравнения происходящих реакций.
- 27. Ответ2Н2S+ O2 = 2S↓ + H2O,2H2S +
- 28. 8.Вопрос по технике безопасности Можно ли горящий
- 29. Ответ. Горящий магний нельзя гасить ни водой,
- 30. 9.Вопрос на сообразительностьНа поверхности одной из планет
- 31. Вопросы и задания Как называется это
- 32. Ответ Планета − Земля; вещество −
- 33. 10. Литературный вопросНа рукомойнике моемПозеленела медь.И так играет луч на нем,Что весело глядеть.А.Ахматова
- 34. Вопрос и задание Какие превращения претерпела медь? Запишите уравнения реакции.
- 35. Ответ Медь окислилась2Сu + O2 + CO2
- 36. 11. Экологический вопросПри извержении вулкана в атмосферу
- 37. Вопросы и задания Какая реакция лежит в
- 38. 2Н2S + SO2 = 3S↓ + 2H2O
- 39. Слайд 39
- 40. Тестовое заданиеI вариантЗадание № 1.К окислительно-восстановительным реакциям
- 41. Тестовое заданиеI вариантЗадание № 2.В каком соединении
- 42. Тестовое заданиеI вариантЗадание № 3.Схема Na0
- 43. Тестовое заданиеI вариантЗадание № 4.Восстановительные свойства простых
- 44. Ответы на тестовое заданиеI вариант1 - В2
- 45. Слайд 45
- 46. Спасибо за работу на уроке!
Слайд 1МБОУ «Средняя школа №2» города Велижа
ОКИСЛИТЕЛЬНО-
ВОССТАНОВИТЕЛЬНЫЕ
РЕАКЦИИ
(презентация к обобщающему уроку в
Подготовила: Нахаева М.И.,
учитель химии
Велиж
2016
Слайд 2Загадка 1
Два антипода пáрою ходят –
Первый теряет, второй находит,
Ролью меняясь
Кто ж из них первый и кто же второй?
Слайд 5Изменение восстановительных свойств в Периодической таблице
В периоде восстановительные свойства уменьшаются,
В группе восстановительные свойства увеличиваются, окислительные - уменьшаются
Слайд 6Задание
1.Дайте определения понятиям «окислитель» и «восстановитель».
2. Какой процесс называется окислением, какой
3. В каких случаях элемент проявляет только восстановительные, в каких – только окислительные свойства?
Слайд 7Ответ 1
Атомы, ионы или молекулы, принимающие электроны, называются окислителями.
Соединения, содержащие элемент
Слайд 8Ответ 2
Атомы, ионы или молекулы, отдающие электроны, называются восстановителями.
Соединения, содержащие элемент
Слайд 9Ответ 3
Если элемент находится в промежуточной степени окисления, то его атомы
Слайд 10Задание 2
Из перечня, приведенного ниже, выпишите отдельно вещества, проявляющие
только окислительные
H2S, Al, FeCl2, NH3, KMnO4, K2Cr2O7, NO2, HNO3, Na2SO3, H2SO4, H2SO3, Cr2O3
Слайд 11Ответ 2
Окислители:
КМnO4, К2Cr2О7,
НNO3, H2SO4.
Восстановители:
Н2S, Аl, NH3.
И те, и
Слайд 12Практическая работа (задание 3)
Используя имеющиеся реактивы
(растворы солей йодида калия, дихромата
Слайд 14Ответ
СаО + Н2О = Са(ОН)2,
реакция соединения;
СuSО4 + 2NаОН =
=
реакция обмена;
Zn + 2НСl = ZnСl2 + Н2↑, реакция замещения, окислительно- восстановительная.
Фото из Шаттерстока
Слайд 164. Литературный вопрос
«По берегам ледяных и шумливых рек песок блестел крупинками
К.Паустовский. «Блистающие облака»
Слайд 18Ответ
Пирит окислился:
4FeS2 + 11O2 = 2Fe2O3 + 8SO2↑
http://freethoughtblogs.com/entequilaesverdad/files/2012/10/DSC05330-884x1024.jpg
Слайд 195. Литературно-практический вопрос
«Пожар пылал несколько часов подряд. Пещера превратилась в настоящую
Л.Буссенар. «Похитители бриллиантов»
Слайд 20Вопросы и задания
Какие процессы произошли в пещере?
Есть ли среди них
Какие реакции называются окислительно-восстановительными?
Какая из описанных реакций протекает с выделением теплоты? Как она называется?
Запишите уравнения реакций.
Осуществите практически последнюю из описанных реакций.
Слайд 21Ответ
СаСО3 = CаО + СО2↑,
СаО + Н2О = Са(ОН)2↓ + Q,
Окислительно-восстановительных реакций нет.
Реакции, в результате которых изменяются степени окисления элементов, называются окислительно- восстановительными.
Фото из Шаттерстока
Слайд 226. Практическая работа
В начале XIX в. Б.Куртуа получил новое простое вещество.
Слайд 23Вопросы и задания
Как называется это вещество?
Используя имеющиеся реактивы, получите это
Запишите уравнения реакций.
Расставьте коэффициенты методом электронного баланса.
Слайд 24Ответ
Вещество – это йод.
Варианты реакций, в результате которых из имеющихся на
а) 6KI + К2Сr 2О7 + 7Н2SО4 = 3I2 + 4К2SО4 + Сr2(SО4)3 + 7Н2О;
б) 2СuSО4 + 4КI = 2СuI + I2 + 2К2SО4.
http://www.libex.ru/dimg/342a5.jpg
Слайд 257.Литературный вопрос
…Трясся Крым двадцать восьмого года
И вставало море на дыбы,
Испуская к
Огненные серые столбы.
Все прошло. Опять гуляет пена,
Но с тех пор все выше, все плотней
Сумрачная серная гиена
Подползает к днищам кораблей…
Ю.Кузнецов. «Тайна Черного моря»
Слайд 26Вопросы и задания
Запишите уравнения происходящих реакций.
Разберите их с
Укажите окислитель и восстановитель.
Слайд 27Ответ
2Н2S+ O2 = 2S↓ + H2O,
2H2S + 3O2 = 2SO2↑ +
H2S – восстановитель, О2 – окислитель.
http://koktebel.ecrimea.ru/pictures/storm/storm15.jpg
…И вставало море на дыбы…
Слайд 288.Вопрос по технике безопасности
Можно ли горящий магний погасить водой или
Запишите уравнения происходящих реакций. Являются ли они окислительно-восстановительными?
Слайд 29Ответ.
Горящий магний нельзя гасить ни водой, ни песком, т.к. он с
Mg + 2H2O = Mg(OH)2 + H2↑,
2Mg + SiO2 = 2MgO + Si.
Это окислительно-восстановительные реакции, т.к. степени окисления элементов изменяются.
Горящий магний
http://www.angelo.edu/faculty/kboudrea/demos/burning_magnesium/BurningMg08.jpg
Слайд 309.Вопрос на сообразительность
На поверхности одной из планет Солнечной системы встречается вещество,
Слайд 31Вопросы и задания
Как называется это планета?
Что это за
Запишите уравнения реакций. Какие из них окислительно -восстановительные?
Слайд 32Ответ
Планета − Земля;
вещество − вода.
2Н2О + 2F2 = 4HF +
2H2O = 2H2 + O2,
2H2 + O2 = 2H2O,
3O2 = 2O3.
Первые три реакции −
окислительно-восстановительные.
Планета Земля
http://grandwallpapers.net/photo/svetyashayasya-zemlya-1600x1200.jpg
Слайд 3310. Литературный вопрос
На рукомойнике моем
Позеленела медь.
И так играет луч на нем,
Что
А.Ахматова
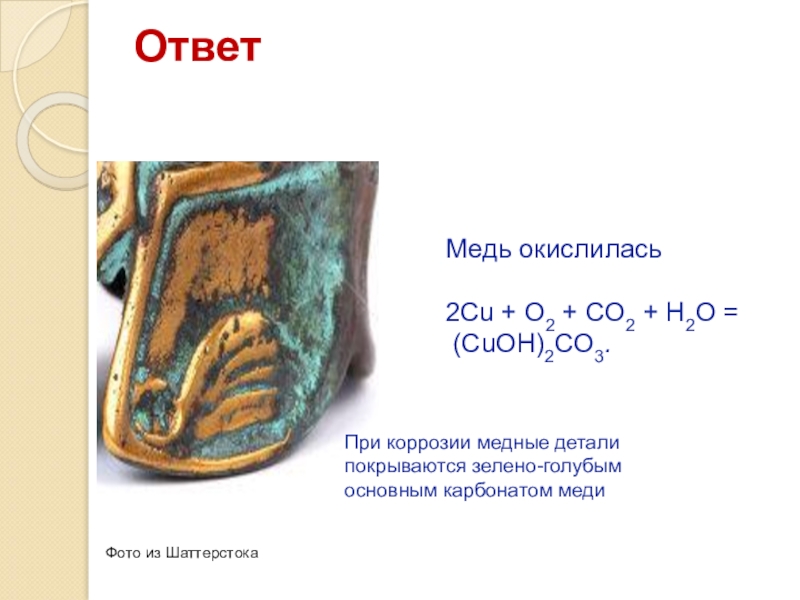
Слайд 35Ответ
Медь окислилась
2Сu + O2 + CO2 + H2O =
(CuOH)2CO3.
При
Фото из Шаттерстока
Слайд 3611. Экологический вопрос
При извержении вулкана в атмосферу выбрасываются соединения серы: диоксид
Слайд 37Вопросы и задания
Какая реакция лежит в основе образования этого вещества?
Запишите уравнение этой реакции.
Какое экологическое значение имеет эта реакция?
Слайд 382Н2S + SO2 = 3S↓ + 2H2O С ПОМОЩЬЮ ЭТОЙ РЕАКЦИИ МОЖНО
Ответ
http://aksakal.info/uploads/posts/2012-06/1340676467_4.jpg
Слайд 40Тестовое задание
I вариант
Задание № 1.
К окислительно-
восстановительным
реакциям не относится
реакция, представленная
А) N2 + 3Н2 = 2NН3
Б) Mg + 2HCl = MgCl2 +
+ H2↑
В)MgCO3 = MgO + CO2 ↑
Г) 2CuO = 2Cu + O2↑
II вариант
Задание № 1.
К окислительно-
восстановительным
реакциям относится
реакция, представленная
схемой:
А) H2O + CaO = Ca(OH)2
Б) H2O + N2O5 = 2HNO3
В) Na2CO3 + 2HCl = 2NaCl + H2O + CO2
Г) CuO + H2 = Cu + H2O
Слайд 41Тестовое задание
I вариант
Задание № 2.
В каком соединении
степени окисления
элементов равны
А) NF3 Б) Cl2O3
В) NH3 Г) AlCl3
II вариант
Задание № 2.
В каком соединении
степени окисления
элементов равны +3 и -2
А) NF3 Б) Cl2O3
В) NH3 Г) AlCl3
Слайд 42Тестовое задание
I вариант
Задание № 3.
Схема Na0 → Na+1
отражает
А) Окисления
Б) Восстановления
В) Нейтрализации
Г) Диссоциации
II вариант
Задание № 3.
Схема Сl0 → Сl-1
отражает процесс:
А) Окисления
Б) Восстановления
В) Нейтрализации
Г) Диссоциации
Слайд 43Тестовое задание
I вариант
Задание № 4.
Восстановительные свойства
простых веществ,
образованных элементами
второго
увеличением заряда ядра:
А) Уменьшаются
Б) Усиливаются
В) Изменяются периодически
Г) Не изменяются
II вариант
Задание № 4.
Окислительные свойства
простых веществ,
образованных элементами
седьмой группы, главной
подгруппы с увеличением
заряда ядра:
А) Уменьшаются
Б) Усиливаются
В) Изменяются периодически
Г) Не изменяются