- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к урокам азот и фосфор
Содержание
- 1. Презентация к урокам азот и фосфор
- 2. азотАзо́т — элемент 15-й группы (по устаревшей классификации — главной подгруппы
- 3. Простое вещество азот — достаточно инертный при нормальных условиях
- 4. открытия Кавендиш выделил азот, но не
- 5. НазваниеНазвание «азо́т» предложил в 1787 году Антуан Лавуазье,
- 6. Азот в природеПриродный азот состоит из двух стабильных изотопов 14N — 99,635 % и 15N — 0,365 %.
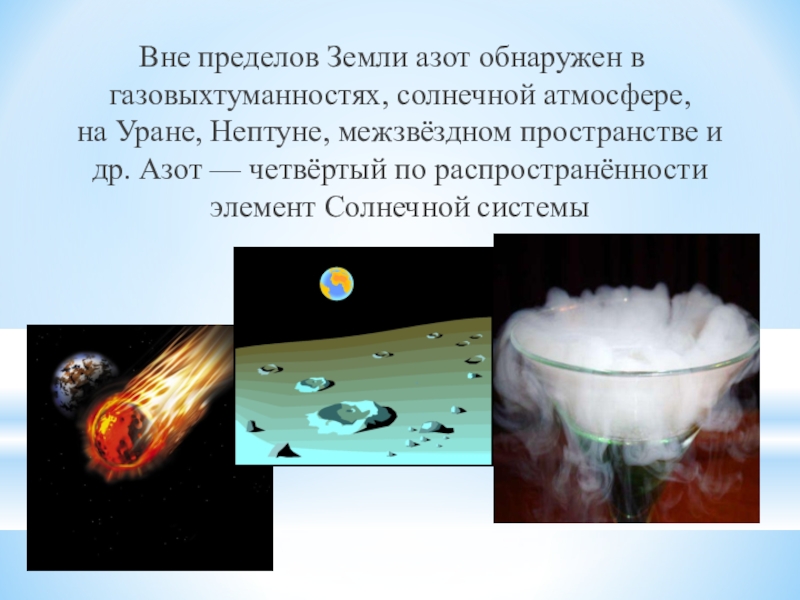
- 7. Вне пределов Земли азот обнаружен в газовыхтуманностях, солнечной атмосфере,
- 8. Азот в свободном состоянии существует в форме
- 9. При нормальных условиях азот это бесцветный газ,
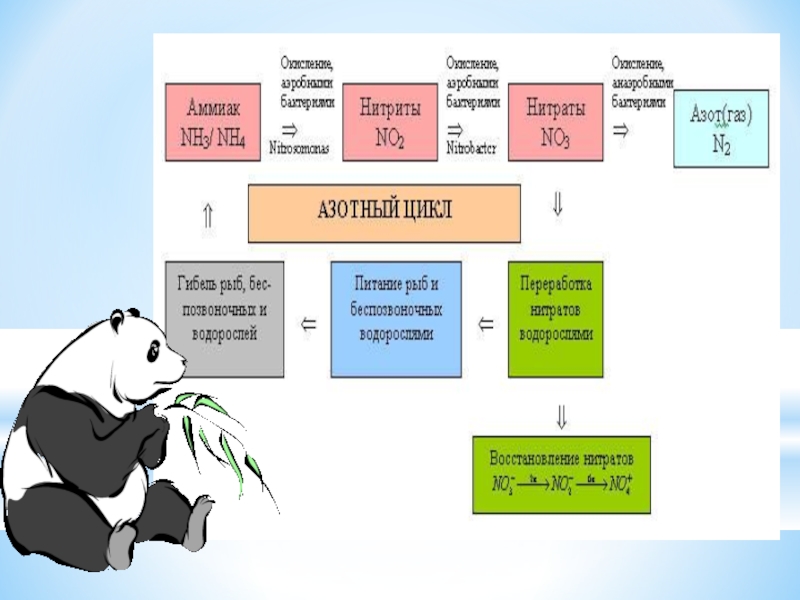
- 10. Биологическая роль
- 11. ФосфорФо́сфор - химический элемент 15-й группы (по устаревшей классификации — главной
- 12. СодержаниеСодержится во всех частях зелёных растений, ещё
- 13. Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать философский камень, а получил светящееся вещество.
- 14. Белый, желтый,красный, черный,металлический
- 15. Физ. свойства в зависимости от вида фосфора
- 16. 1) Фосфор
- 17. Фосфор используют как отраву для грызунов и
- 18. Спасибо за внимание!
азотАзо́т — элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 7. Обозначается символом N (лат. Nitrogenium)
Слайд 2азот
Азо́т — элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) второго периода периодической
системы химических элементов Д. И. Менделеева, с атомным номером 7. Обозначается символом N (лат. Nitrogenium)
Слайд 3
Простое вещество азот — достаточно инертный при нормальных условиях двухатомный газ без цвета, вкуса
и запаха, из которого на три четверти состоит земная атмосфера.
Слайд 4 открытия
Кавендиш выделил азот, но не сумел понять, что это
новое вещество.
Даниэль Резерфорд опубликовал магистерскую диссертацию, где указал основные свойства азота и стал его официальным первооткрывателем.
Слайд 5Название
Название «азо́т» предложил в 1787 году Антуан Лавуазье, который в то время
в составе группы других французских учёных разрабатывал принципы химической номенклатуры.
Слайд 6Азот в природе
Природный азот состоит из двух стабильных изотопов 14N — 99,635 % и 15N —
0,365 %.
Слайд 7
Вне пределов Земли азот обнаружен в газовыхтуманностях, солнечной атмосфере, на Уране, Нептуне, межзвёздном пространстве и
др. Азот — четвёртый по распространённости элемент Солнечной системы
Слайд 8
Азот в свободном состоянии существует в форме двухатомных молекул N2
Между атомами
азота 3-ая связь N≡N (длина связи N≡N = 0,1095 нм).
Молекула азота крайне прочна
Молекула азота неполярна и слабо поляризуется, силы взаимодействия между молекулами очень слабые, поэтому в обычных условиях азот газообразен.
В высоких слоях атмосферы происходит фотохимическая диссоциация молекул N2.
Молекула азота крайне прочна
Молекула азота неполярна и слабо поляризуется, силы взаимодействия между молекулами очень слабые, поэтому в обычных условиях азот газообразен.
В высоких слоях атмосферы происходит фотохимическая диссоциация молекул N2.
Слайд 9
При нормальных условиях азот это бесцветный газ, не имеет запаха, мало
растворим в воде,(плотность 1,2506 кг/м³ (при н.у.).
В жидком состоянии (темп. кипения −195,8 °C) — бесцветная, подвижная, как вода, жидкость.
В жидком состоянии (темп. кипения −195,8 °C) — бесцветная, подвижная, как вода, жидкость.
Слайд 11 Фосфор
Фо́сфор - химический элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) третьего
периода периодической системы Д. И. Менделеева; имеет атомный номер 15.
В земной коре его содержание составляет 0,08—0,09 % её массы. Концентрация в морской воде 0,07 мг/л.
В земной коре его содержание составляет 0,08—0,09 % её массы. Концентрация в морской воде 0,07 мг/л.
Слайд 12Содержание
Содержится во всех частях зелёных растений, ещё больше его в плодах
и семенах, в животных тканях, входит в состав белков и других важнейших органических соединений (АТФ,ДНК)
Слайд 13
Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать философский камень,
а получил светящееся вещество.
Слайд 15
Физ. свойства в зависимости от вида фосфора различны. От белого к
желтому,черному, красному и металлическому они меняются и характеризуются в каждом виде отдельно.
Слайд 16
1) Фосфор легко окисляется кислородом
2) Взаимодействует
с металлами — окислитель,
3) Взаимодействует с неметаллами — восстановитель
4)В холодных концентрированных растворах щелочей также медленно протекает реакция диспропорционирования:
5)Сильные окислители превращают фосфор в фосфорную кислоту
3) Взаимодействует с неметаллами — восстановитель
4)В холодных концентрированных растворах щелочей также медленно протекает реакция диспропорционирования:
5)Сильные окислители превращают фосфор в фосфорную кислоту
Слайд 17
Фосфор используют как отраву для грызунов и в фармацевтических препаратах. Красный
фосфор применяют в больших количествах при производстве спичек. Фосфаты, в качестве удобрений в с/х. Также широко применение в промышленности и медицине.