Понятие о ряде активности металлов.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Физические и химические свойства кислот
Содержание
- 1. Презентация Физические и химические свойства кислот
- 2. Цель: Познакомить с физическими и химическими свойствами
- 3. Слайд 3
- 4. Шарада – Мы первым подзовем
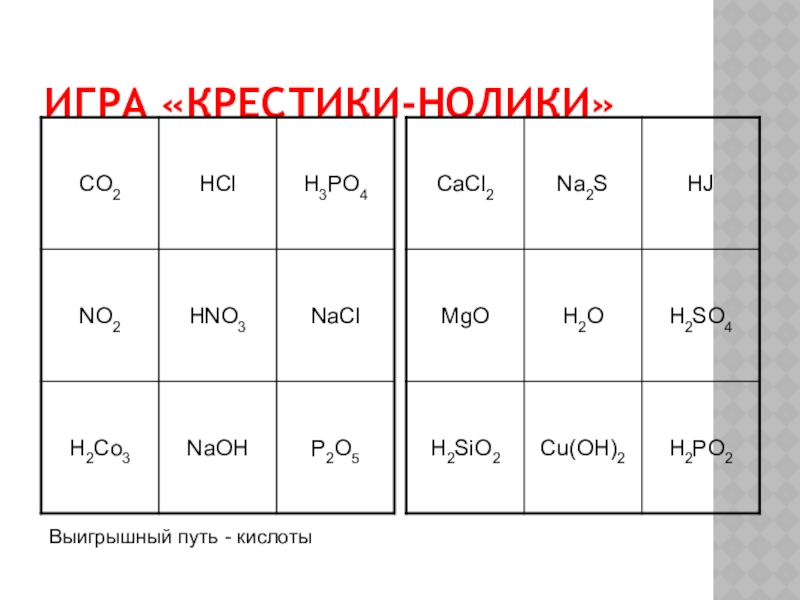
- 5. игра «Крестики-нолики»Выигрышный путь - кислоты
- 6. беговая дорожка HClH2CO3H3PO4HJH2SH2SO4HBrHNO3H3PO4HClH2SO3H3PO4HFH2CO3H2S
- 7. Нитратная кислота описывается в трудах арабского
- 8. Ж., з., ρ = 1,51 г/см3, tпл
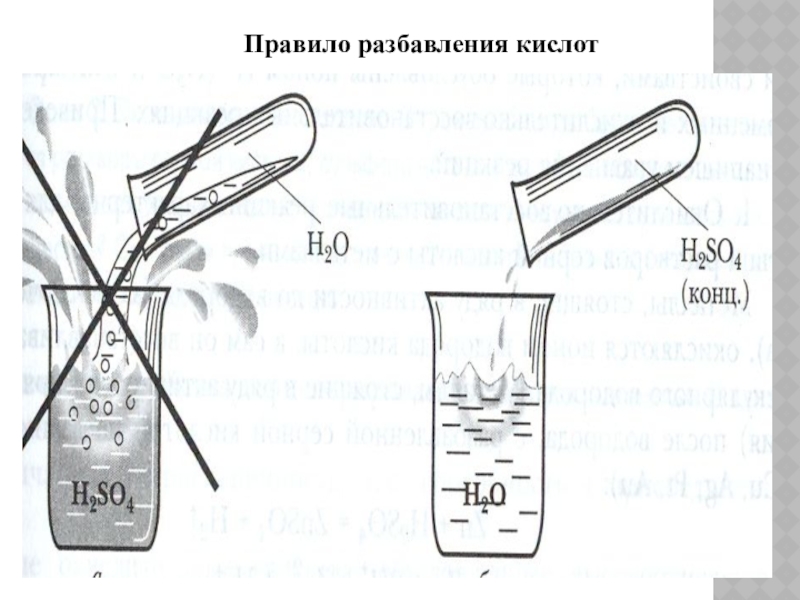
- 9. Правило разбавления кислот
- 10. Слайд 10
- 11. Это вам не волшебство, В том загадки
- 12. Н.Н.Бекетове
- 13. Интересная история из жизни ученого :
- 14. Слайд 14
- 15. Кислота, чтоб вы знали, Обожает металлы. Но
- 16. Расшифруйте запись Б + D = MgSO4 + A
- 17. Слайд 17
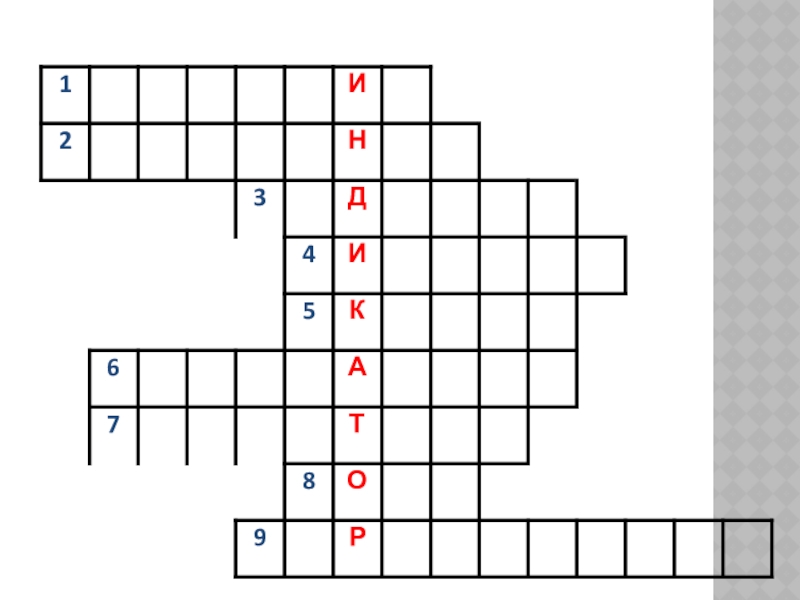
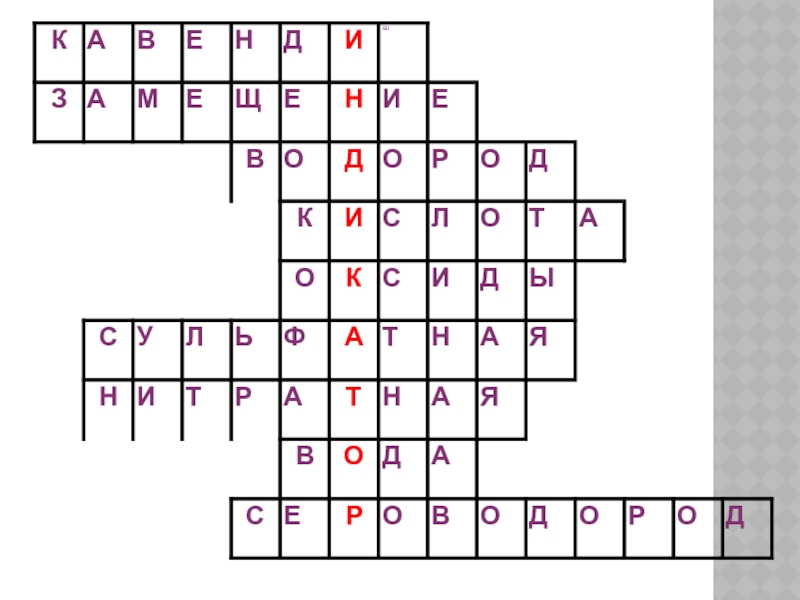
- 18. 1.УЧЕНЫЙ, ОТКРЫВШИЙ ВОДОРОД2. ТИП РЕАКЦИИ ВЗАИМОДЕЙТВИЯ КИСЛОТ
- 19. Слайд 19
- 20. Человек рождается на свет, Чтоб творить, дерзать,
Цель: Познакомить с физическими и химическими свойствами кислот. Развивать навыки составления уравнений химических реакций. Развивать умения школьников наблюдать, анализировать, делать выводы.
Слайд 1Тема: Физические и химические свойства кислот: действие индикатора, взаимодействие с металлами.
Слайд 2Цель: Познакомить с физическими и химическими свойствами кислот. Развивать навыки составления
уравнений химических реакций. Развивать умения школьников наблюдать, анализировать, делать выводы.
Слайд 4 Шарада – Мы первым подзовем кота. Вторым измерим толщу
вод,
Союз на третье нам пойдет.
А целым станет… ( кислота)
Слайд 7Нитратная кислота описывается в трудах арабского врача и алхимика Джабира
ибн Хаяна (815). Сульфатная стала известна после 11 ст. В работах Альберта Великого (1280) есть воспоминания о получении сульфатной кислоты. В России « купоросное масло»(сульфатную), «Крепкую водку» (нитратную). «царскую водку» ( смесь нитратной и хлоридной) в небольшом количеству получали в аптеках .Аптеки были основаны в 1581 г во времена Ивана Грозного.
Слайд 8Ж., з., ρ = 1,51 г/см3, tпл = - 420С, tкип
= 860С
НNO3 (конц., дымящая)
ω = 1, желтая
НNO3 (разб., недымящая)
ω = 0,6 бесцветная
НNO3 (конц., дымящая)
ω = 1, желтая
НNO3 (разб., недымящая)
ω = 0,6 бесцветная
Физические свойства
Правила обращения с концентрированной азотной кислотой
«Дымит», так как пары ее образуют с влагой воздуха мелкие капельки тумана
HNO3 ---------->
Работать в резиновых перчатках!
Берегись ожога!
При попадании кислоты на кожу место поражения быстро промыть большим количеством воды!
свет
!
4NO2 ↑+ O2 ↑ + 2H2O
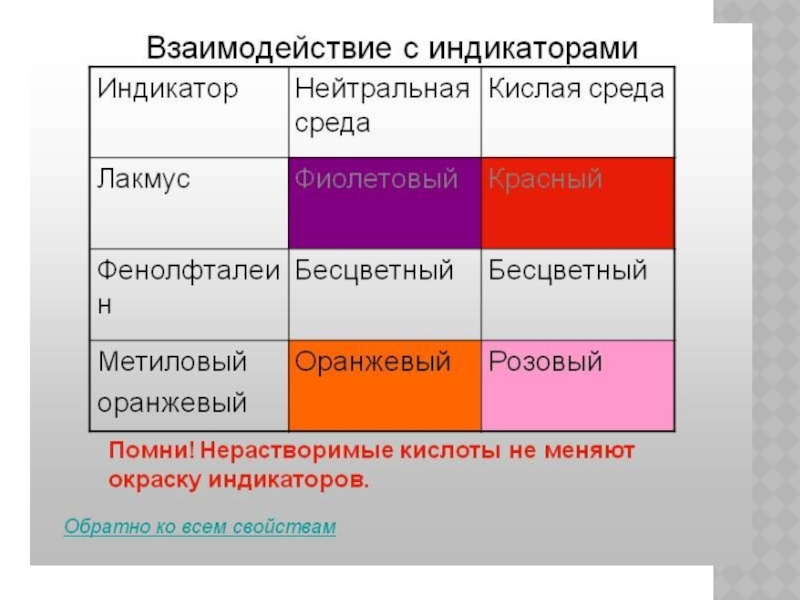
Слайд 11Это вам не волшебство, В том загадки нет. Индикатор – вещество, Что меняет цвет. У
метилоранжа флаг трехцветный:
Коль нейтральная среда,
Он оранжевый всегда;
Если встретит кислоту,
То краснеет на ходу;
Ну, а если гидроксид -
То желтеет в тот же миг.
Слайд 13Интересная история из жизни ученого : Профессор химии Н.Н.Бекетов
работал, когда в кабинет вбежал взволнованный слуга
-Николай Николаевич! В Вашей библиотеке воры!
Бекетов поднял голову и спросил: Да? И что они там читают.
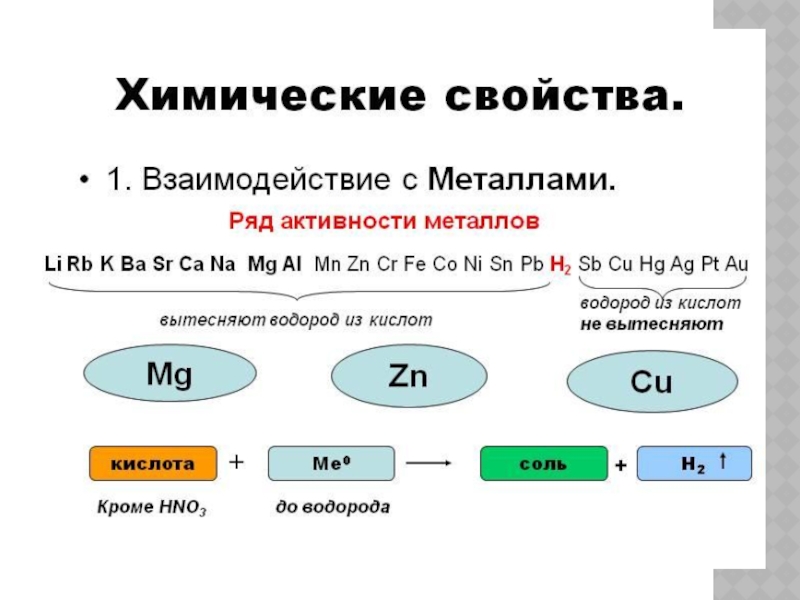
Слайд 15Кислота, чтоб вы знали, Обожает металлы. Но не все, а только те, Что доступны
кислоте.
Сам Бекетов, говорят,
Разместил металлы в ряд.
Водород стоит меж ними,
Чуть подальше середины.
С металлом, что до водорода,
И реагируют кислоты.
Итог известен наперед:
Соль да чистый водород.
Идет реакция сия
По типу замещения.
Слайд 181.УЧЕНЫЙ, ОТКРЫВШИЙ ВОДОРОД
2. ТИП РЕАКЦИИ ВЗАИМОДЕЙТВИЯ КИСЛОТ С МЕТАЛЛАМИ
3. ЛЕГКИЙ ГАЗ
4.
ВЕЩЕСТВО ПОД ДЕЙСТВИЕМ, КОТОРОГО МЕТИЛ-ОРАНЖ МЕНЯЕТ ЦВЕТ НА КРАСНЫЙ
5. СЛОЖНОЕ ВЕЩЕСТВО, СОСТОЯЩЕЕ ИЗ ДВУХ ЭЛЕМЕНТОВ, ОДИН ИЗ КОТОРЫХ – ОКСИГЕН.
6. СИЛЬНАЯ КИСЛОТА
7. КИСЛОТА, КОТОРАЯ ВХОДИТ В СОСТАВ « ЦАРСКОЙ ВОДКИ»
8. ВЕЩЕСТВО, КОТОРОЕ МОЖЕТ НАХОДИТЬСЯ В ТРЕХ АГРЕГАТНЫХ СОСТОЯНИЯХ
9. СОЕДИНЕНИЕ С ГИДРОГЕНОМ, ИМЕЮЩЕЕ НЕПРИЯТНЫЙ ЗАПАХ
5. СЛОЖНОЕ ВЕЩЕСТВО, СОСТОЯЩЕЕ ИЗ ДВУХ ЭЛЕМЕНТОВ, ОДИН ИЗ КОТОРЫХ – ОКСИГЕН.
6. СИЛЬНАЯ КИСЛОТА
7. КИСЛОТА, КОТОРАЯ ВХОДИТ В СОСТАВ « ЦАРСКОЙ ВОДКИ»
8. ВЕЩЕСТВО, КОТОРОЕ МОЖЕТ НАХОДИТЬСЯ В ТРЕХ АГРЕГАТНЫХ СОСТОЯНИЯХ
9. СОЕДИНЕНИЕ С ГИДРОГЕНОМ, ИМЕЮЩЕЕ НЕПРИЯТНЫЙ ЗАПАХ
Слайд 20Человек рождается на свет, Чтоб творить, дерзать, а не иначе, Чтоб оставить в
жизни добрый след
И решить все сложные задачи.
Человек рождается на свет…
Для чего? Ищите свой ответ.