- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад для учащихся 8 классов на тему Основания
Содержание
- 1. Презентация для учащихся 8 классов на тему Основания
- 2. Химические свойства Гидроксид – ионы (ОН-), образующиеся
- 3. Химические свойства оснований (щелочей и нерастворимых оснований)
- 4. Химические свойства щелочей 3. Взаимодействие с оксидами:Са(OН)2
- 5. Химические свойства щелочей4. Взаимодействие с растворами солей:
- 6. Химические свойства нерастворимых оснований
- 7. Способы получения растворимых оснований (щелочей) 1. Взаимодействие
- 8. Способы получения нерастворимых основанийВзаимодействие раствора щелочи с
Слайд 2Химические свойства
Гидроксид – ионы (ОН-), образующиеся при диссоциации оснований, обуславливают
1. Действие на индикаторы
Слайд 3Химические свойства оснований
(щелочей и нерастворимых оснований)
2NaOH + H2SO4 →
основание + кислота = соль + вода
Реакция нейтрализации – реакция между кислотой и основанием
2. Взаимодействие с кислотами
Cu(OH)2 + H2SO4=CuSO4 + 2H 2O
нерастворимое + кислота = соль + вода
основание
Слайд 4Химические свойства щелочей
3. Взаимодействие с оксидами:
Са(OН)2 + SO3 = СаSO4
2КOН + ZnO = К2ZnO2 + H2O
кислотными
амфотерными
Слайд 5Химические свойства щелочей
4. Взаимодействие с растворами солей:
2NaОН + CuSO4 → Cu(OH)2 + Na2SO4
Слайд 6Химические свойства нерастворимых оснований
Сu(OН)2 ---> СuO + H2O
Разложение при нагревании
Слайд 7Способы получения растворимых оснований (щелочей)
1. Взаимодействие щелочных и щелочно-земельных металлов с
2Na + 2H2O = 2NaOH + H2
2. Взаимодействие оксидов щелочных и щелочно-земельных металлов с водой
СаO + H2O = Са(OН)2
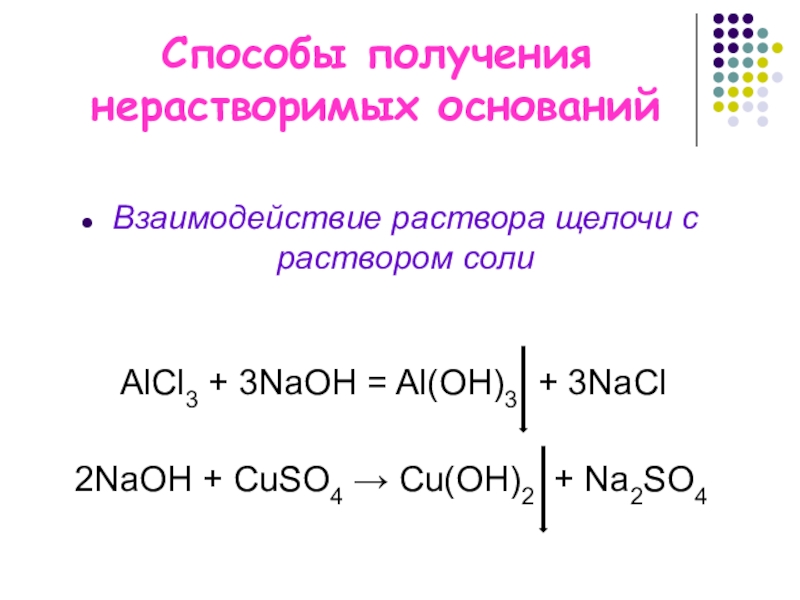
Слайд 8Способы получения нерастворимых оснований
Взаимодействие раствора щелочи с раствором соли
АlCl3 + 3NaOH
2NaОН + CuSO4 → Cu(OH)2 + Na2SO4