- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Презентации на тему: Растворы №1 и №2; и Великие химики - Великой страны
Содержание
- 1. Презентации на тему: Растворы №1 и №2; и Великие химики - Великой страны
- 2. Цели урока:Углубление знаний учащихся о растворах, растворимости,
- 3. Задачи:А) обучающие:Вооружить учащихся конкретными знаниями 2) Актуализировать
- 4. Характеристика урока:Тип урока:Изучение новогоматериала Методы урока:
- 5. Формы урока:Урок с элементами исследования и решения проблемных задач способствует применению индивидуальной, парной, фронтальной формы работы.
- 6. Сегодня о растворах мы поговорим, И
- 7. Процесс растворения складывается из: -Разрушения структуры растворяемого
- 8. Слайд 8
- 9. В ходе эволюции вода создала окружающую нас природу, живой мир, да и самого человека.
- 10. Слайд 10
- 11. Итак, ответьте на вопросы:Есть ли абсолютно нерастворимые
- 12. Ответы:Растворение- это измельчение (диспергирование) вещества до структурных
- 13. Ответы:Прозрачные , непрозрачныеОсаждаются, не осаждаютсяРасслаиваются, не расслаиваютсяВидны
- 14. Проблемная задачаПомоги друзьям!Однажды Незнайка и Знайка пошли
- 15. Правильные ответы ребят:Растворить смесь в воде.Тщательно перемешать.Профильтровать.Выпарить соль.Ребята! Назовите виды растворов, которые вы знаете.
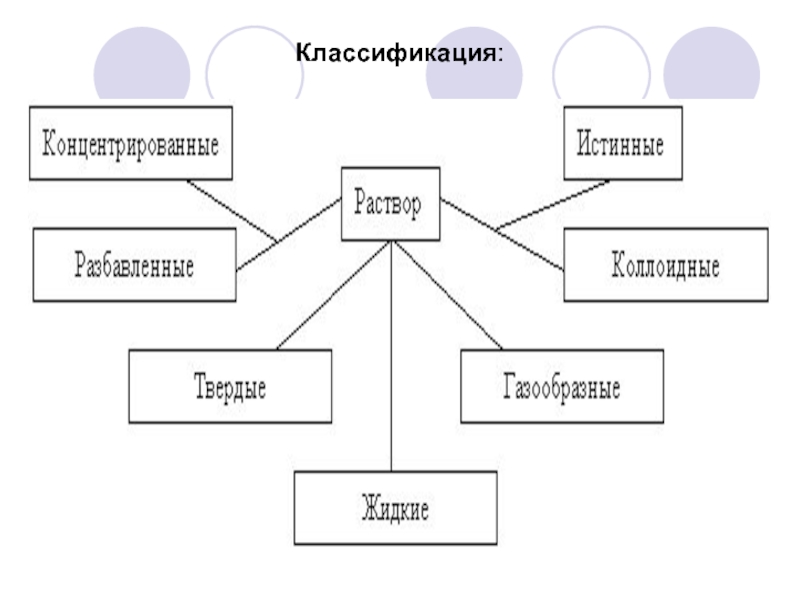
- 16. Классификация:
- 17. Голодный « динозаврик»- это
- 18. Проблемная задача
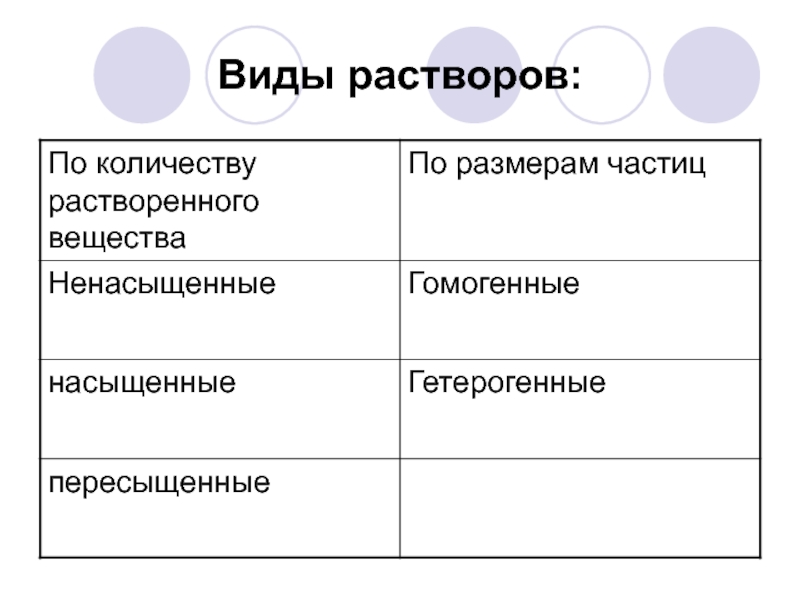
- 19. Виды растворов:
- 20. В зависимости от структурных единиц различают растворы:Молекулярные
- 21. Слайд 21
- 22. Тест о растворахНасыщенный раствор одновременно:А) может быть
- 23. 4. При растворении твердых веществ в воде
- 24. 9. Укажите признаки, которые свидетельствуют о химической
- 25. Формулы для выражения состава раствора1 W=
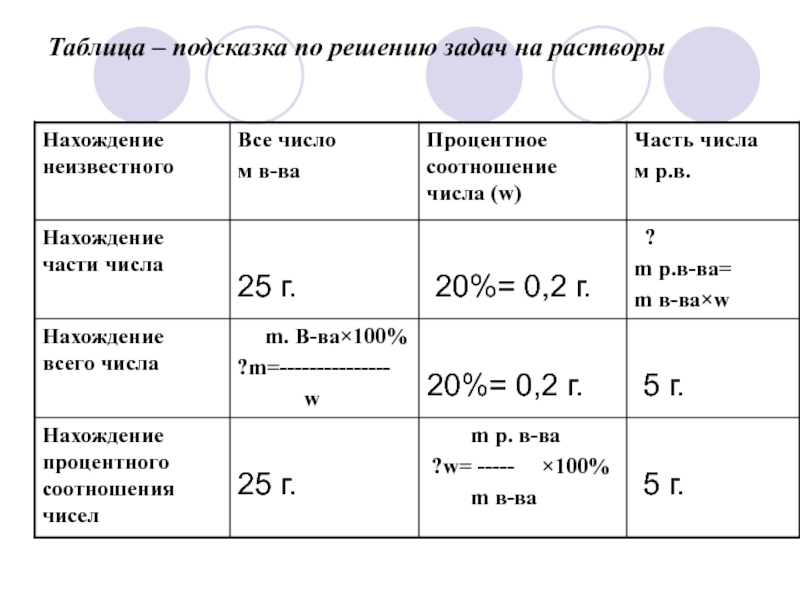
- 26. Таблица – подсказка по решению задач на растворы
- 27. Занимательная задача
- 28. Закрепление Сколько г медного купороса и
- 29. Применение
- 30. Итог урокаСегодня на уроке?Теперь я знаю?Мне на уроке?
- 31. Дом. задание * 8, стр. 70-71, упр. № 4Практическая работа по желаниюСпасибо за работу!
Слайд 1Тема урока:
Растворы, растворимость.
«Незнающие пусть
Учитель: Прутко В.В.
Слайд 2Цели урока:
Углубление знаний учащихся о растворах, растворимости, способах выражения растворимости
Закрепить на
Слайд 3Задачи:
А) обучающие:
Вооружить учащихся конкретными знаниями
2) Актуализировать навыки решения расчетных задач
Б)
Развивать логическое мышление, сообразительность, умение находить решение в нетипичных ситуациях
Активизация познавательной деятельности через решение проблемных ситуаций
Развивать умения анализировать, делать выводы
В) воспитательные
Показать материальное единство мира
Формировать навыки исследовательской деятельности
Воспитывать четкость, наблюдательность и организованность в работе
Слайд 4Характеристика урока:
Тип урока:
Изучение нового
материала
Методы урока:
Исследовательский,
репродуктивный,
Объяснительно- иллюстративный
Слайд 5Формы урока:
Урок с элементами исследования и решения проблемных задач способствует применению
Слайд 6 Сегодня о растворах мы поговорим,
И рассмотрим их значенье на
На растворимость поглядим,
Разных веществ в воде.
Узнаем много способов мы разных,
Выраженье растворимости, друзья.
Для растворения ведь очень важно:
Температура, природа вещества и растворителя.
Ребята! Как вы думаете, из чего складывается процесс растворения?
Слайд 7Процесс растворения складывается из:
-Разрушения структуры растворяемого вещества под воздействием растворителя.
-Взаимодействия
-Равномерного распределения частиц растворенного вещества с молекулами растворителя.
А, какое вещество является универсальным растворителем?
Слайд 10
Мир загадок:
1.Как только попаду я в воду,
То не видать меня вам сроду?
2.В воду – родится,
А воды – боится?
3.Только в воду окунется
Невидимкой обернется?
Химический анекдот:
На уроке химии: Скажи –ка, Володя, какие вещества не растворяются в воде?
Володя, не раздумывая сказал: Рыбы.
Это интересно:
Красивые облака – это тоже вода. Кажется, что они невесомы, но 1 км их весит около 2000 тонн.
Слайд 11Итак, ответьте на вопросы:
Есть ли абсолютно нерастворимые вещества?
Что
Что такое растворимое вещество?
Что такое растворение веществ?
Что такое раствор?
Слайд 12Ответы:
Растворение- это измельчение (диспергирование) вещества до структурных частиц (атомов, молекул, ионов)
Растворитель –это жидкость в которой растворяемое вещество растворяется, образуя раствор.
Растворимое вещество- это вещество, которое растворяется в растворителе, образуя раствор.
Раствор – это гомогенная система, состоящая из растворителя, растворенных веществ и продуктов их взаимодействия.
А что вы можете сказать о растворах?
Слайд 13Ответы:
Прозрачные , непрозрачные
Осаждаются, не осаждаются
Расслаиваются, не расслаиваются
Видны невооруженным глазом, не видны.
Вопрос:
Опыт: Взаимодействие воды с Na и Fe.
Слайд 14Проблемная задача
Помоги друзьям!
Однажды Незнайка и Знайка пошли с друзьями в поход.
- Ничего страшного! – воскликнул Знайка. – Беда легко поправима! Нам для этого нужно взять только …?
Что сказал Знайка? Каков план действий?
Слайд 15Правильные ответы ребят:
Растворить смесь в воде.
Тщательно перемешать.
Профильтровать.
Выпарить соль.
Ребята! Назовите виды растворов,
Слайд 17 Голодный « динозаврик»- это Сытый « динозаврик»- ненасыщенный раствор,
Слайд 18 Проблемная задача «Алмазные веточки»
Готовим насыщенный раствор
Почему??
Ответ: В растворе соли больше, чем надо. Вот соль и обрадовалась, когда появилась веточка, и излишки соли отдала ей.
Слайд 20В зависимости от структурных единиц различают растворы:
Молекулярные – водные растворы неэлектролитов
Ионные
Молекулярно- ионные – водные растворы слабых электролитов.
Закрепление в виде теста: ( перед проведением проверочной работы проводится физ. минутка)
Слайд 21 Физ.
Вы глаза свои закройте, про себя тихонько спойте:
1,2,3,4,5 – будем тихо отдыхать
6,7,8 – мы усталость свою сбросим.
На 9 – лени пальцем погрозим,
На 10 - дружно говорим,
Быть лентяем не хотим!
Слайд 22Тест о растворах
Насыщенный раствор одновременно:
А) может быть разбавленным
Б) не может быть
В) не может быть концентрированным
2. Что не представляет собой раствор?
А) дистиллированная вода
Б)хлорная вода
В)аммиачная вода
Г)известковая
3. Раствор, в котором при данной температуре вещество больше не растворяется
А) пересыщенный б) насыщенный в)ненасыщенный
Слайд 23
4. При растворении твердых веществ в воде энергия:
А) всегда поглощается
В) может выделяться или поглощаться
Г) не выделяется и не поглощается
5. Укажите компоненты сахара в воде:
А) вода б) катион глюкозы и анион фруктозы
В) сахароза г) фруктоза и глюкоза
6. Растворимость веществ в воде зависит от:
А) их природы б) для газов от давления
В) от природы растворителя г) от температуры
7. Ненасыщенный раствор можно сделать насыщенным:
А) добавив в раствор воды б) упарив раствор
В) дополнительно растворив соответствующую порцию соли
8. В какой воде лучше растворяется поваренная соль:
А) в холодной б) в горячей
Слайд 24
9. Укажите признаки, которые свидетельствуют о химической стороне процесса растворения:
А) выделение
В) диффузия частиц растворимого вещества
Г) изменение окраски раствора
10. Процесс , при котором молекулы воды окружают молекулы растворенного вещества называется:
А) сольватация б) гидратация в) синерезис
Слайд 25Формулы для выражения состава раствора
1 W= (m р. в-ва /m
2 W = (V р.в/ V р-ра) . 100% - объемная доля р.в. (для газовых смесей)
3 См = (n р.в/ V р-ра) . 100% - молярная концентрация
4 m = (m р.в./ m р-ля) .100% - моляльная концентрация
Слайд 28Закрепление
Сколько г медного купороса и воды нужно взять для получения 200г
Сколько г меда, в котором было 50% глюкозы, съел Чебурашка, если клетки его организма получили 120 г. воды?
Сколько г гидроксида натрия потребуется для получения 500 мл 0,2 М раствора?