- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Первоначальные сведения о строении атома урок химии 8 класс
Содержание
- 1. Первоначальные сведения о строении атома урок химии 8 класс
- 2. Атом – наименьшая частица химического элемента, являющаяся носителем его свойств
- 3. Основные сведения о строении атомаМБОУ СОШ №12 им. ак.В.И. Кудиноваг.ВоткинскУдмуртская РеспубликаУчитель химии : Григоровская Л.НВоткинск -2018
- 4. ЗАДАЧИ: - ОЗНАКОМИТЬСЯ С ТЕОРИЯМИ СТРОЕНИЯ
- 5. Атом греч. atomos«неделимый»
- 6. Эрнест Резерфорд В 1911 г. предложил уточнённую «планетарную» модель строения атома.
- 7. Эрнест Резефорд В 1913 г. доказал, что
- 8. Слайд 8
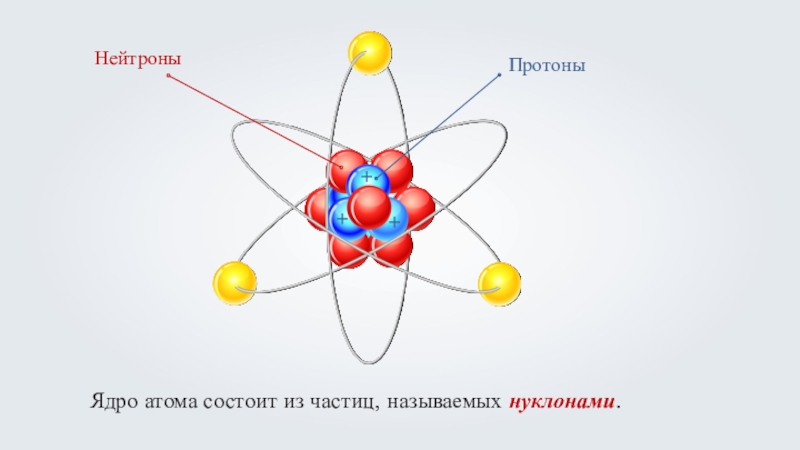
- 9. Ядро атома состоит из частиц, называемых нуклонами. +++
- 10. Протоныp+
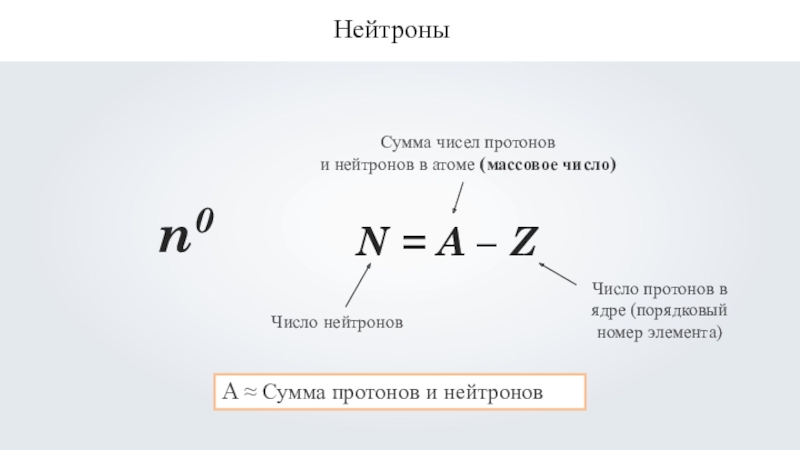
- 11. Нейтроныn0N = A – Z A ≈ Сумма протонов и нейтронов
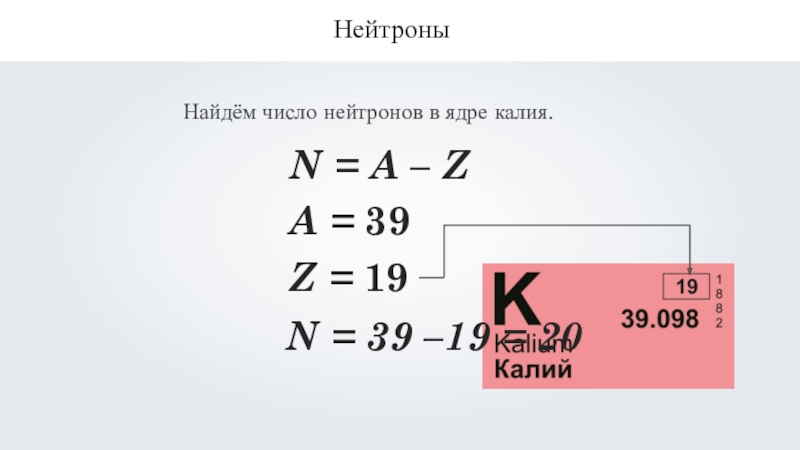
- 12. НейтроныНайдём число нейтронов в ядре калия. N
- 13. НейтроныНайдём число нейтронов в ядре аргона. N
- 14. Электроные- Число электронов равно числу протонов.
- 15. Найдем из периодической системы число электронов и протонов брома.ЭлектроныЧисло электронов = 35Z = 35
- 16. Атом – сложная нейтральная частица химического элемента,
- 17. Слайд 17
Атом – наименьшая частица химического элемента, являющаяся носителем его свойств
Слайд 3Основные сведения о строении атома
МБОУ СОШ №12
им. ак.В.И. Кудинова
г.Воткинск
Удмуртская Республика
Учитель
химии : Григоровская Л.Н
Воткинск -2018
Слайд 4ЗАДАЧИ: - ОЗНАКОМИТЬСЯ С ТЕОРИЯМИ СТРОЕНИЯ АТОМА - УЗНАТЬ ВИДЫ КАКИХ ЧАСТИЦ ВХОДЯТ
В СОСТАВ АТОМА
- НАУЧИТЬ ОПРЕДЕЛЯТЬ КОЛИЧЕСТВО
ЧАСТИЦ, ВХОДЯЩИХ В СОСТАВ АТОМА
- ДАТЬ ПОЛНОЕ ПОНЯТИЕ АТОМА
Цель урока: Изучение строения атома
Слайд 7Эрнест Резефорд
В 1913 г. доказал, что порядковый (атомный) номер химического
элемента численно равен заряду ядра его атома.
Химический элемент – это вид атомов с одинаковым зарядом ядра
Слайд 15Найдем из периодической системы число электронов и протонов брома.
Электроны
Число электронов =
35
Z = 35
Слайд 16
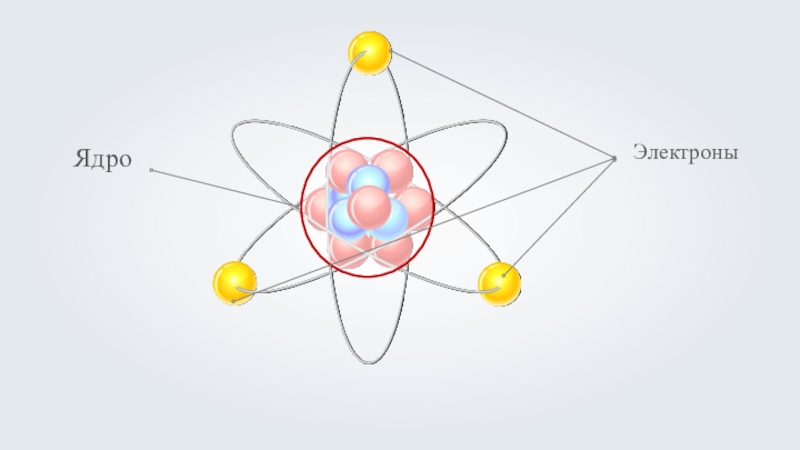
Атом – сложная нейтральная частица химического элемента, состоящая из положительно заряженного
ядра, вокруг которого движутся отрицательно заряженные электроны. Адро атома состоит из протонов и нейтронов