- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Оксиды
Содержание
- 1. Оксиды
- 2. Оксиды - этосложные вещества,состоящие из двух элементов,
- 3. Способы получения оксидов.Взаимодействие простых веществ с кислородом:
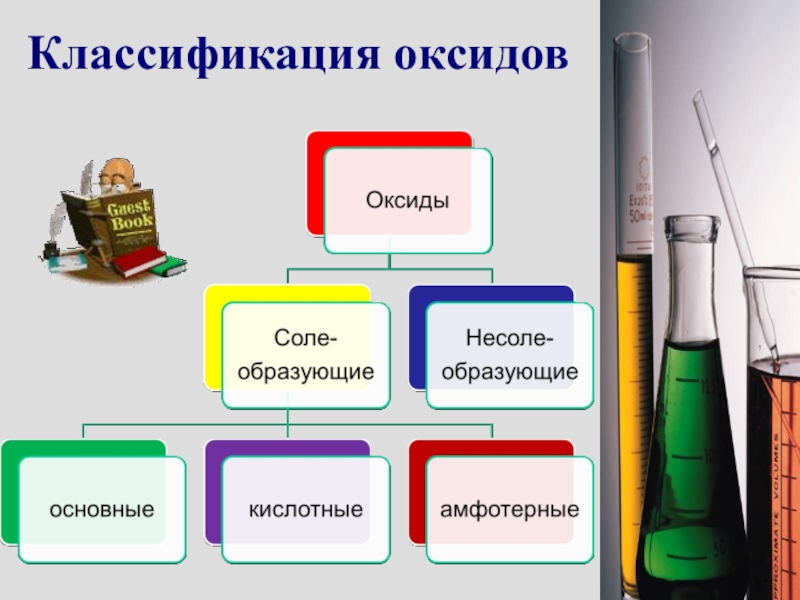
- 4. Классификация оксидов
- 5. НесолеобразующиеоксидыЭто оксиды, которые не взаимодействуют ни с
- 6. Основные оксидыЭто оксиды, которым в качестве гидроксидов
- 7. Химические свойстваосновных оксидов.Взаимодействие с кислотами: основный оксид
- 8. Кислотные оксидыЭто оксиды, которым в качестве гидроксидов
- 9. Химические свойствакислотных оксидов.Со щелочами: кислотный оксид+ щёлочь→соль
- 10. АМФОТЕРНЫЕ ОКСИДЫ. Это оксиды, которым соответствуют гидроксиды,
- 11. Химические свойстваамфотерных оксидов. Как основные оксиды. С
- 12. Вывод. С повышением валентности атомов элемента, образующего
- 13. Задания. Определите характер данных оксидов
Оксиды - этосложные вещества,состоящие из двух элементов, один из которых кислород.Например: CaO, SO2, Al2O3, CO.
Слайд 2Оксиды - это
сложные вещества,
состоящие из двух
элементов, один из
которых кислород.
Например:
CaO, SO2,
Al2O3, CO.
Al2O3, CO.
Слайд 3Способы получения оксидов.
Взаимодействие простых веществ с кислородом:
2Mg + O2 = 2Mg O
2. Горение на воздухе сложных веществ:
CH4 + 2O2 = CO2 + 2H2O
3. Разложение нерастворимых оснований:
Mg(OH)2 = MgO + H2O
4. Разложение некоторых кислот:
H2SiO3 = SiO2 + H2O
5. Разложение некоторых солей:
CaCO3 = CaO + CO2
2. Горение на воздухе сложных веществ:
CH4 + 2O2 = CO2 + 2H2O
3. Разложение нерастворимых оснований:
Mg(OH)2 = MgO + H2O
4. Разложение некоторых кислот:
H2SiO3 = SiO2 + H2O
5. Разложение некоторых солей:
CaCO3 = CaO + CO2
Слайд 5Несолеобразующие
оксиды
Это оксиды, которые не взаимодействуют ни с кислотами, ни с основаниями
и не образуют солей. Оксиды образованы атомами неметаллов:
CO, NO, N2O, SiO.
CO, NO, N2O, SiO.
Солеобразующие
оксиды
Это оксиды, которые взаимодействуют с кислотами или со щелочами с образованием солей и воды: N2O5, CO2, CaO, Na2O.
Слайд 6Основные оксиды
Это оксиды, которым в качестве гидроксидов
соответствуют основания.
Например: CuO →
Cu(OH)2
Основные оксиды образуют только металлы с валентностью I и II.
Например: Na2O, K2O, CaO, MgO, CuO, CrO.
Исключение BeO, ZnO, SnO, PbO.
Основные оксиды образуют только металлы с валентностью I и II.
Например: Na2O, K2O, CaO, MgO, CuO, CrO.
Исключение BeO, ZnO, SnO, PbO.
Слайд 7Химические свойства
основных оксидов.
Взаимодействие с кислотами:
основный оксид + кислота→соль +вода
MgO + 2HCl → MgCl2 + H2O
2. взаимодействие с кислотными оксидами,:
основный оксид + кислотный оксид →соль
CaO + N2O5 → Ca(NO3)2
3. С водой (если соответствующее основание растворимо):
основный оксид +вода → щёлочь
Na2O + H2O → 2NaOH
2. взаимодействие с кислотными оксидами,:
основный оксид + кислотный оксид →соль
CaO + N2O5 → Ca(NO3)2
3. С водой (если соответствующее основание растворимо):
основный оксид +вода → щёлочь
Na2O + H2O → 2NaOH
Слайд 8Кислотные оксиды
Это оксиды, которым в качестве гидроксидов соответствуют кислоты.
Например:
SO3 → H2SO4
Кислотные оксиды образуют все неметаллы в любой валентности, исключая несолеобразующие оксиды, и металлы с валентностью V и выше.
Например: CO2, N2O5, SiO2,
Mn2O7, CrO3.
Кислотные оксиды образуют все неметаллы в любой валентности, исключая несолеобразующие оксиды, и металлы с валентностью V и выше.
Например: CO2, N2O5, SiO2,
Mn2O7, CrO3.
Слайд 9Химические свойства
кислотных оксидов.
Со щелочами:
кислотный оксид+ щёлочь→соль + вода
CO2 + 2KOH → K2CO3 + H2O
2. С основными оксидами:
кислотный оксид + основный→соль
CO2 + MgO → MgCO3
3. С водой (исклSiO2):
кислотный оксид+вода→кислота
SO3 + H2O → H2SO4
CrO3 + H2O → H2CrO4
2. С основными оксидами:
кислотный оксид + основный→соль
CO2 + MgO → MgCO3
3. С водой (исклSiO2):
кислотный оксид+вода→кислота
SO3 + H2O → H2SO4
CrO3 + H2O → H2CrO4
Слайд 10АМФОТЕРНЫЕ
ОКСИДЫ.
Это оксиды, которым соответствуют гидроксиды, проявляющие свойства как оснований,
так и кислот.
Например:
BeO → Be(OH)2 → H2BeO2
ZnO → Zn(OH)2 → H2ZnO2
Амфотерные оксиды образуют только металлы с валентностью III и IV.
Например: Cr2O3, Fe2O3, Al2O3.
Оксиды BeO, ZnO , SnO, PbO также являются амфотерными.
Например:
BeO → Be(OH)2 → H2BeO2
ZnO → Zn(OH)2 → H2ZnO2
Амфотерные оксиды образуют только металлы с валентностью III и IV.
Например: Cr2O3, Fe2O3, Al2O3.
Оксиды BeO, ZnO , SnO, PbO также являются амфотерными.
Слайд 11Химические свойства
амфотерных оксидов.
Как основные оксиды.
С кислотами:
ZnO + 2HCl → ZnCl2 + H2O
2. С кислотными оксидами, образуя соли:
ZnO + SiO2 → ZnSiO3
Как кислотные оксиды.
Со щелочами, образуя соль и воду:
ZnO + 2KOH → K2ZnO2 + H2O
2. С основными оксидами, образуя соли:
ZnO + CaO → CaZnO2
С водой амфотерные оксиды не взаимодействуют.
2. С кислотными оксидами, образуя соли:
ZnO + SiO2 → ZnSiO3
Как кислотные оксиды.
Со щелочами, образуя соль и воду:
ZnO + 2KOH → K2ZnO2 + H2O
2. С основными оксидами, образуя соли:
ZnO + CaO → CaZnO2
С водой амфотерные оксиды не взаимодействуют.
Слайд 12Вывод.
С повышением валентности атомов элемента, образующего оксиды, увеличиваются кислотные свойства
его оксидов и гидроксидов.
Неметаллы образуют кислотные оксиды ( исключение - несолеобразующие оксиды).
Металлы
Неметаллы образуют кислотные оксиды ( исключение - несолеобразующие оксиды).
Металлы
Слайд 13Задания.
Определите характер данных оксидов
CO2, ZnO, Na2O,
SO2, CaO, NO и напишите соответствующие им гидроксиды.
2. Из предложенного ряда K2O, SO3, NaOH, HCl, ZnO, CaSO4, H2O выпишите вещества, реагирующие с оксидом кальция. Напишите уравнения соответствующих реакций .
3. Найдите массу оксида магния, образовавшегося при горении 0,3 моль магния.
2. Из предложенного ряда K2O, SO3, NaOH, HCl, ZnO, CaSO4, H2O выпишите вещества, реагирующие с оксидом кальция. Напишите уравнения соответствующих реакций .
3. Найдите массу оксида магния, образовавшегося при горении 0,3 моль магния.