- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Метан - как газообразное вещество.
Содержание
- 1. Метан - как газообразное вещество.
- 2. ГАЗ Газ (газообразное состояние) (от нидерл. gas) — агрегатное
- 3. Газообразное состояние вещества в условиях, когда возможно
- 4. Газообразное состояние — самое распространённое состояние вещества Вселенной
- 5. Идеальный газ — математическая модель газа, в
- 6. Реальный газ — газ, который не описывается уравнением
- 7. Мета́н — простейший углеводород, бесцветный газ без запаха,
- 8. Метан — первый член гомологического ряда насыщенных углеводородов,
- 9. ИСТОЧНИКИ Основной компонент природных (77—99 %), попутных нефтяных
- 10. Классификация по происхождению:абиогенный — образован как результат химических
- 11. ПОЛУЧЕНИЕ В лаборатории получают нагреванием натронной извести
- 12. ХИМИЧЕСКИЕ СВОЙСТВАГорит в воздухе голубоватым пламенем, при
- 13. ПРИМЕНЕНИЕ Топливо.Продукты хлорирования используются в огнетушителях, как
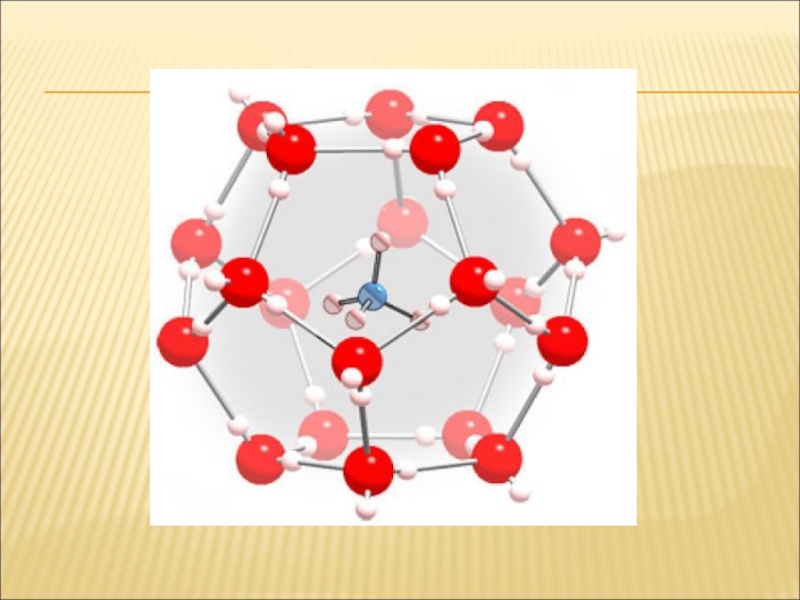
- 14. СОЕДИНЕНИЯ ВКЛЮЧЕНИЯ Метан образует соединения включения — газовые гидраты, широко распространенные в природе.
- 15. Газовые гидраты могут иметь практическое применение в
- 16. Слайд 16
Слайд 2ГАЗ
Газ (газообразное состояние) (от нидерл. gas) — агрегатное состояние вещества, характеризующееся очень слабыми
Слайд 3
Газообразное состояние вещества в условиях, когда возможно существование устойчивой жидкой или
Подобно жидкостям, газы обладают текучестью и сопротивляются деформации. В отличие от жидкостей, газы не имеют фиксированного объёма и не образуют свободной поверхности, а стремятся заполнить весь доступный объём (например, сосуда).
Слайд 4
Газообразное состояние — самое распространённое состояние вещества Вселенной (межзвёздное вещество, туманности, звёзды,
Слайд 5
Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной
Слайд 6
Реальный газ — газ, который не описывается уравнением состояния идеального газа Клапейрона —
Зависимости между его параметрами показывают, что молекулы в реальном газе взаимодействуют между собой и занимают определенный объем. Состояние реального газа часто на практике описывается обобщенным уравнением Менделеева — Клапейрона:
Слайд 7
Мета́н — простейший углеводород, бесцветный газ без запаха, химическая формула — CH4. Малорастворим
Слайд 8
Метан — первый член гомологического ряда насыщенных углеводородов, наиболее устойчив к химическим
Слайд 9ИСТОЧНИКИ
Основной компонент природных (77—99 %), попутных нефтяных (31—90 %), рудничного и болотного газов
Древесный дебрис - источник метана
Слайд 10
Классификация по происхождению:
абиогенный — образован как результат химических реакций неорганических соединений;
биогенный — образован
бактериальный (микробный) — образован в результате жизнедеятельности бактерий;
термогенный — образован в ходе термохимических процессов.
На Марсе обнаружен минерал серпентин – возможно, именно он, а не прячущиеся где-то живые организмы, является источником метана в атмосфере планеты
Слайд 11ПОЛУЧЕНИЕ
В лаборатории получают нагреванием натронной извести (смесь гидроксидов натрия и кальция)
2NaOH+CH3COOH→(t)Na2CO3+CH4↑+H2O Для этой реакции важно отсутствие воды, поэтому и используется гидроксид натрия, так как он менее гигроскопичен.
Возможно получение метана сплавлением ацетата натрия с гидроксидом натрия:
CH3COONa + NaOH → CH4↑ + Na2CO3
Ученые предлагают использовать гидраты — твердые соединения метана с водой, которые образуются при низкой температуре и высоком давлении. Гидрат состоит из сформированных молекулами воды «клеток», внутри которых заключены молекулы метана. Удобным местом для формирования подобных соединений является дно океана, где существуют подходящие условия.
Слайд 12ХИМИЧЕСКИЕ СВОЙСТВА
Горит в воздухе голубоватым пламенем, при этом выделяется энергия около
Вступает с галогенами в реакции замещения (например, CH4 + 3Cl2= CHCl3+ 3HCl), которые проходят по свободно радикальному механизму:
CH4 + ½Cl2 = CH3Cl (хлорметан)
CH3Cl + ½Cl2 = CH2Cl2 (дихлорметан)
CH2Cl2 + ½Cl2 = CHCl3 (трихлорметан)
CHCl3 + ½Cl2 = CCl4 (тетрахлорметан)
Выше 1400° С разлагается по реакции: 2CH4 = C2H2 + 3H2
Окисляется до муравьиной кислоты при 150—200 °C и давлении 30—90 атм по цепному радикальному механизму:
CH4 + 3[O] = HCOOH + H2O
Слайд 13ПРИМЕНЕНИЕ
Топливо.
Продукты хлорирования используются в огнетушителях, как снотворное, или растворитель.
Производство продукта дегидрирования-ацетилена.
Продукт
Метанол запретили применять в автохимии.