- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Химия пәнінен олимпиада есептерін шығару
Содержание
№1 Бензиннің (оның құрамы шамамен С-86%, H-14%) 1 кг толық жану үшін теориялық оттектің мөлшерін есептеңіздер? Оттектің ауадағы массалық үлесі 23%, ал оның салыстырмалы молекулалық массасы 29.
Слайд 2
№1 Бензиннің
(оның құрамы шамамен С-86%, H-14%) 1 кг толық жану үшін теориялық оттектің мөлшерін есептеңіздер? Оттектің ауадағы массалық үлесі 23%, ал оның салыстырмалы молекулалық массасы 29.
Слайд 3 Берілгені
Шешуі
m(бензин)=1кг m(C)=m(бензин)*W(C)=1000*0,86=860г.
W(C)=86% m(Н)=m(бензин)*W(Н)=1000*0,14=140г.
W(H)= 14% 860г хг
W(O)=23% С + О2 = СО2
т/к m(оттек)-? 12г/моль 32г/моль
х=2293г
140г х г
2Н2 + О2 = 2Н2О
т/к m(ауа)-? 2 г/моль 32 г/моль
х=1120г
оттектің жалпы массасы: 2293г+1120г=3413г
Егер ауадығы оттектің массалық үлесі 23%болса, онда 100г ауада 23г оттектің бар болғаны, олай болса ауаның
100грамында 23г оттек бар, ал х г ауада 3413г оттек бар деп,
Х=100*3413 = 14840 г = 14,8 кг
23
Жауабы: m(оттек) =14,8 кг
m(бензин)=1кг m(C)=m(бензин)*W(C)=1000*0,86=860г.
W(C)=86% m(Н)=m(бензин)*W(Н)=1000*0,14=140г.
W(H)= 14% 860г хг
W(O)=23% С + О2 = СО2
т/к m(оттек)-? 12г/моль 32г/моль
х=2293г
140г х г
2Н2 + О2 = 2Н2О
т/к m(ауа)-? 2 г/моль 32 г/моль
х=1120г
оттектің жалпы массасы: 2293г+1120г=3413г
Егер ауадығы оттектің массалық үлесі 23%болса, онда 100г ауада 23г оттектің бар болғаны, олай болса ауаның
100грамында 23г оттек бар, ал х г ауада 3413г оттек бар деп,
Х=100*3413 = 14840 г = 14,8 кг
23
Жауабы: m(оттек) =14,8 кг
Слайд 4
№2. Белісіз металл нитратының сулы ерітіндісі суытқанда
одан 0,3 моль кристаллогидрат алынған. Онда сусыз тұздың массалық үлесі 59,5%, ал кристалдық судың массасы сусыз тұздың массасының 22,8 г кем болған. Кристалогидраттың молекулалық массасын есептеңдер.
Слайд 5Берілгені:
Шешуі:
Х(NO3) n W(H2O) =100%-59,5%=40,5%
V (крис-т)= 0,3моль m X(NO3) - m(H2O) =22.8%
w(тұз)=59.5% W=59.5%-40.5%=19%
m(H2O)= m(тұз)-22.8 19% 22.8
100% x
т\к Mr (крис-т)=? X=120г.
масса кристаллогидрат: V = m M =m
M V
M =m = 120 = 400г/моль
V 0.3
Жауабы: Mr(крис-т)= 400г/моль
Х(NO3) n W(H2O) =100%-59,5%=40,5%
V (крис-т)= 0,3моль m X(NO3) - m(H2O) =22.8%
w(тұз)=59.5% W=59.5%-40.5%=19%
m(H2O)= m(тұз)-22.8 19% 22.8
100% x
т\к Mr (крис-т)=? X=120г.
масса кристаллогидрат: V = m M =m
M V
M =m = 120 = 400г/моль
V 0.3
Жауабы: Mr(крис-т)= 400г/моль
Слайд 6 №3 Массасы 100 г суды электр тогымен
айырғанда массасы бойынша қанша сутек және оттек бөлінеді?
Слайд 7 Берілгені
Шешуі
m(H2O)=100г 100г х у
Т/К m(H2), m(O2)=? 2H2O → 2H2 + O2
18г/моль 2/моль 32/моль
V = m = 100г = 5.55моль
M 18г/моль
Реакция теңдеуі бойынша бөлінген сутегінің зат мөлшері де осынша
55,5 моль m= V * M = 55,5 моль * 2 г/моль = 11,1 г
Реакция теңдеуі бойынша бөлінген оттектің зат мөлшері сутектен екі есе аз, яғни m = 5.55:2 = 2.775 моль
m= V * M = 2.775 моль* 32 г/моль = 88,8 г
Жауабы: m(H2) = 11.1 г m(O2) =88,8 г
m(H2O)=100г 100г х у
Т/К m(H2), m(O2)=? 2H2O → 2H2 + O2
18г/моль 2/моль 32/моль
V = m = 100г = 5.55моль
M 18г/моль
Реакция теңдеуі бойынша бөлінген сутегінің зат мөлшері де осынша
55,5 моль m= V * M = 55,5 моль * 2 г/моль = 11,1 г
Реакция теңдеуі бойынша бөлінген оттектің зат мөлшері сутектен екі есе аз, яғни m = 5.55:2 = 2.775 моль
m= V * M = 2.775 моль* 32 г/моль = 88,8 г
Жауабы: m(H2) = 11.1 г m(O2) =88,8 г
Слайд 8 №4. Белгілі бір температурадағы
H2 + Br2→ 2HBr
реакциясының тепе-теңдік константасы КТ.Т.=1,0. Егер реакцияға 1 моль H2 және 2 моль Br2 алынған болса, тепе-теңдік жүйедегі қоспаның құрамы қандай?
реакциясының тепе-теңдік константасы КТ.Т.=1,0. Егер реакцияға 1 моль H2 және 2 моль Br2 алынған болса, тепе-теңдік жүйедегі қоспаның құрамы қандай?
Слайд 9Берілгені
Шешуі
КТ.Т.=1,0. КТ.Т. = [HBr]2
V (H2 ) = 1 моль [H2] [Br2]
V (Br2 ) = 2 моль H2 + Br2→ 2HBr
Т/К тепе теңдік жүйедегі V (H2 ) = (1-x) моль
қоспаның құрамы V (Br2 ) = (2-х) моль
V (НBr ) = 2х моль
КТ.Т. = [2х]2 = 1
[1-х] * [2-х]
4x2 = (1-x)(2-x)= 2-2x-x+x2
3x2-3x-2=0
Х=0,45
V (H2 ) = (1-0,45)= 0,55 моль
V (Br2 ) = (2-0,45)= 1,55 моль
V (НBr ) = 2 * 0,45 = 0,90 моль
Жауабы: тепе теңдік жүйедегі қоспаның құрамы төмендегідей
V (H2 ) = (1-0,45)= 0,55 моль
V (Br2 ) = (2-0,45)= 1,55 моль
V (НBr ) = 2 * 0,45 = 0,90 моль
КТ.Т.=1,0. КТ.Т. = [HBr]2
V (H2 ) = 1 моль [H2] [Br2]
V (Br2 ) = 2 моль H2 + Br2→ 2HBr
Т/К тепе теңдік жүйедегі V (H2 ) = (1-x) моль
қоспаның құрамы V (Br2 ) = (2-х) моль
V (НBr ) = 2х моль
КТ.Т. = [2х]2 = 1
[1-х] * [2-х]
4x2 = (1-x)(2-x)= 2-2x-x+x2
3x2-3x-2=0
Х=0,45
V (H2 ) = (1-0,45)= 0,55 моль
V (Br2 ) = (2-0,45)= 1,55 моль
V (НBr ) = 2 * 0,45 = 0,90 моль
Жауабы: тепе теңдік жүйедегі қоспаның құрамы төмендегідей
V (H2 ) = (1-0,45)= 0,55 моль
V (Br2 ) = (2-0,45)= 1,55 моль
V (НBr ) = 2 * 0,45 = 0,90 моль
Слайд 10 № 5 Массасы 4,8 г органикалық
затты жаққанда көлемі 3,36 л көмірқышқыл газы және көлемі 6,72 л су буы түзілді. Органикалық зат буының сутегі бойынша салыстырмалы тығыздығы 16-ға тең. Осы органикалық заттың формуласын табыңыздар.
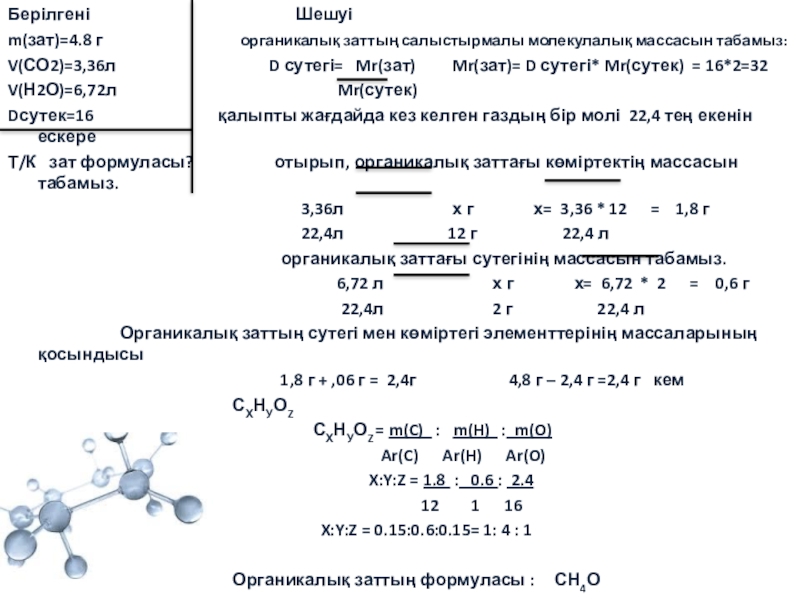
Слайд 11Берілгені
Шешуі
m(зат)=4.8 г органикалық заттың салыстырмалы молекулалық массасын табамыз:
V(СО2)=3,36л D сутегі= Mr(зат) Mr(зат)= D сутегі* Mr(сутек) = 16*2=32
V(Н2О)=6,72л Mr(сутек)
Dсутек=16 қалыпты жағдайда кез келген газдың бір молі 22,4 тең екенін ескере
Т/К зат формуласы? отырып, органикалық заттағы көміртектің массасын табамыз.
3,36л х г х= 3,36 * 12 = 1,8 г
22,4л 12 г 22,4 л
органикалық заттағы сутегінің массасын табамыз.
6,72 л х г х= 6,72 * 2 = 0,6 г
22,4л 2 г 22,4 л
Органикалық заттың сутегі мен көміртегі элементтерінің массаларының қосындысы
1,8 г + ,06 г = 2,4г 4,8 г – 2,4 г =2,4 г кем
СХНУОZ
СХНУОZ = m(C) : m(H) : m(O)
Ar(C) Ar(H) Ar(O)
X:Y:Z = 1.8 : 0.6 : 2.4
12 1 16
X:Y:Z = 0.15:0.6:0.15= 1: 4 : 1
Органикалық заттың формуласы : СН4О
m(зат)=4.8 г органикалық заттың салыстырмалы молекулалық массасын табамыз:
V(СО2)=3,36л D сутегі= Mr(зат) Mr(зат)= D сутегі* Mr(сутек) = 16*2=32
V(Н2О)=6,72л Mr(сутек)
Dсутек=16 қалыпты жағдайда кез келген газдың бір молі 22,4 тең екенін ескере
Т/К зат формуласы? отырып, органикалық заттағы көміртектің массасын табамыз.
3,36л х г х= 3,36 * 12 = 1,8 г
22,4л 12 г 22,4 л
органикалық заттағы сутегінің массасын табамыз.
6,72 л х г х= 6,72 * 2 = 0,6 г
22,4л 2 г 22,4 л
Органикалық заттың сутегі мен көміртегі элементтерінің массаларының қосындысы
1,8 г + ,06 г = 2,4г 4,8 г – 2,4 г =2,4 г кем
СХНУОZ
СХНУОZ = m(C) : m(H) : m(O)
Ar(C) Ar(H) Ar(O)
X:Y:Z = 1.8 : 0.6 : 2.4
12 1 16
X:Y:Z = 0.15:0.6:0.15= 1: 4 : 1
Органикалық заттың формуласы : СН4О