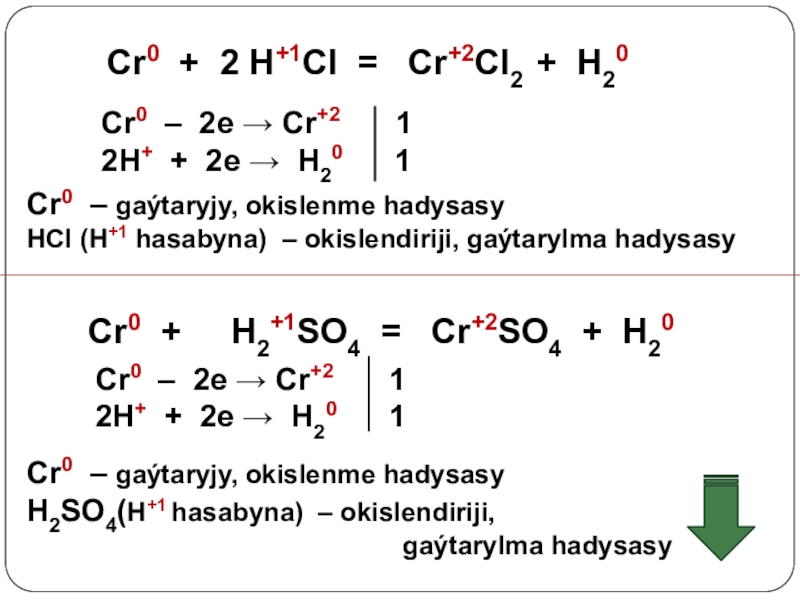- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Himiya, 11-nji synp, Prezentasiya, Hrom
Содержание
- 1. Himiya, 11-nji synp, Prezentasiya, Hrom
- 2. I. Taryhy maglumatlarII. Hrом – himiki
- 3. 1766 –nji ýylda Ýekateniburgyň töwereginde mineral tapylyp
- 4. Fransuz himigi Lui Nikolýa
- 5. Слайд 5
- 6. D. I. Mendeleýewiň HEPS – da ýerleşişi.
- 7. Tebigatda tapylyşyHrom giňden ýaýran elementlere degişli (0,02
- 8. Fiziki häsiýetleriDykyzlygy 7,19 g/sм3; t ereme 1890°С;
- 9. Alnyşy Fe(CrO2)2 hromly demir magdany kömür bilen
- 10. Arassa hrom almak üçin reaksiýa şeýle geçýär:1)
- 11. Elektroliziň kömegi bilen hromyň
- 12. Himiki häsiýetleriLi, K, Ba, Ca ,Na ,Mg,
- 13. Otag temperaturasynda oksid örtüginiň
- 14. Cr0 + O20
- 15. Cr0 + N20 =
- 16. Has gaty gyzdyrlanda hrom suwuň buglary bilen
- 17. Cr0 +
- 18. kislorodyň gatnaşmagyndahromyň (III) duzlaryny
- 19. Коsentrirlenen kükürt we azot kislotalary sowukda
- 20. Cr0 + H2S+6O4 → Cr2+3(SO4)3 + S+4O2
- 21. Hrom köp metallary olaryň duzlarynyň erginlerinden gysyp
- 22. Cr + KClO3 + KOH
- 23. Cr0 + KCl+5O3 + KOH → K2Cr+6O4
- 24. Hrom – ösümlik we
- 25. Hrom ром köp sanly legilirlenen
Слайд 2I. Taryhy maglumatlar
II. Hrом – himiki element:
1. D.I.Меndеlеýеwiň himiki elementleriň
2. Atomnyň gurluşy.
III.Hrом – sada madda
3. Tebigatda tapylyşy
1. Düzümi. Fiziki häsiýetleri.
2. Alnyşy.
3. Himiki häsiýetleri.
4. Biologiki ähmiýeti we fiziologiki täsiri.
5. Ulanylyşy.
Слайд 3
1766 –nji ýylda Ýekateniburgyň töwereginde mineral tapylyp «sibir gyzyl gurşuny» diýip
1797 – nji ýylda fransuz himigi L. N. Woklen bu mineralda täze himiki elementi açdy we 1798 – nji ýylda erkin hrom almagy başardy..
Adynyň gelip çykyşy
Elementiň ady grek. χρῶμα — reňk, boýag sözünden emele gelipdir.
Слайд 4 Fransuz himigi Lui Nikolýa Woklen Sent Andre d
Minerallaryň analizine uly goşand goşupdyr. Himikleriň mekdebini döredipdir. Ilkinjileriň hatarynda himiki analiz boýunça gollanma çap edipdir – «Analitiki himiýa giriş» (1799).
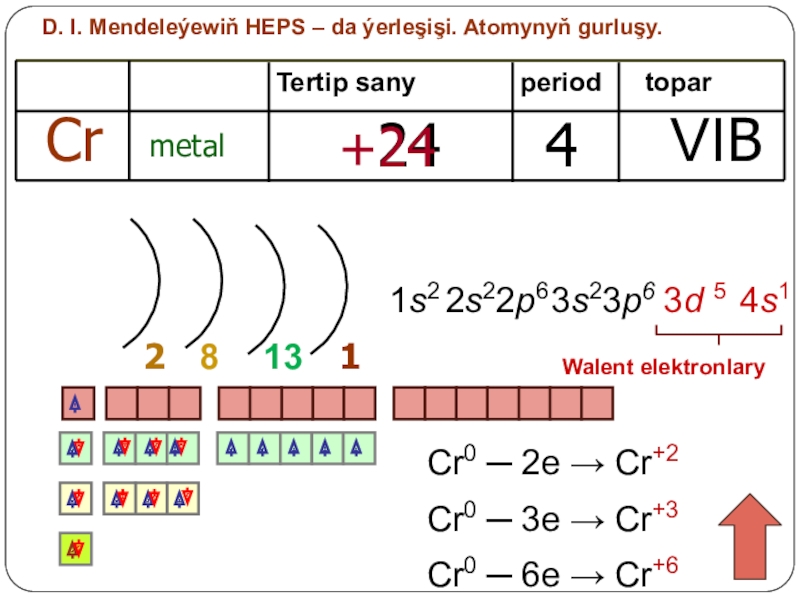
Слайд 6D. I. Mendeleýewiň HEPS – da ýerleşişi. Atomynyň gurluşy.
period
topar
Tertip sany
Cr
metal
24
4
VIB
+24
4
2
1
8
Walent elektronlary
13
1s2
2s22p6
4s1
3s23p6
3d
Cr0 ─ 2e → Cr+2
Cr0 ─ 3e → Cr+3
Cr0 ─ 6e → Cr+6
Слайд 7Tebigatda tapylyşy
Hrom giňden ýaýran elementlere degişli (0,02 mass. pňaýy, %). Hromuň esasy
FeO·Cr2O3, ikinji derejede krokoid durýar PbCrO4.
hromit
krokoit
Слайд 8Fiziki häsiýetleri
Dykyzlygy 7,19 g/sм3;
t ereme 1890°С;
t gaýnama
Erkin halda — gögümtil – ak metal.
Hrom (goşundyly) iň bir gaty metallaryň biridir.
Örän arassa hrom bilen mehaniki işlemek mümkindir.
Howada durnukly. 2000 °C – de ýaşyl hrom oksidini (III) Cr2O3. emele getirip ýanýar.
Слайд 9Alnyşy
Fe(CrO2)2 hromly demir magdany kömür bilen gyzdyrlanda hromuň we demriň
FeO· Cr2O3 + 4C → Fe + 2Cr + 4CO↑
Ferrohrom — demiriň we hromuň splawy ( 60% töweregi),
Esasy garyndylary – uglerod (5% çenli) кremniý (8% çenli), kükürt
(0,05 % çenli), fosfor (0,05 %).
Ferrohrom legilirlenen splawlary öndürmekde ulanylýar.
Слайд 10Arassa hrom almak üçin reaksiýa şeýle geçýär:
1) howada demir hromidi bilen
4Fe(CrO2)2 + 8Na2CO3 + 7O2→8Na2CrO4 + 2Fe2O3 + 8CO2↑
2) natriý hromadyny eredip demir oksidinden bölüp aýyrýarlar;
3) тergini turşadyp we kristallaşdyryp hromaty dihromata öwürýärler;
4) dihromaty kömür bilen gaýtaryp arassa hrom oksidini alýarlar:
Na2Cr2O7 + 2C → Cr2O3 + Na2CO3 + CO↑
5) alýuminotermiýa arkaly hrom metalyny alýarlar:
Cr2O3 + 2Al → Al2O3 + 2Cr + 130 ккal
Слайд 11 Elektroliziň kömegi bilen hromyň angidrid ergininden kükürt kislotasyny
1) alty walentli hromyň erginli üç walentli hroma çenli gaýtarylmagy;
2) wodorod ionlarynyň razrýadyndan gaz görnüşli wodorodyň bölünip çykmagy;
3) metal hromyň çökmegi bilen bolup alty walentli hromy saklaýan ionlaryň razrýady ;
Cr2O72− + 14Н+ + 12е− = 2Cr + 7H2O
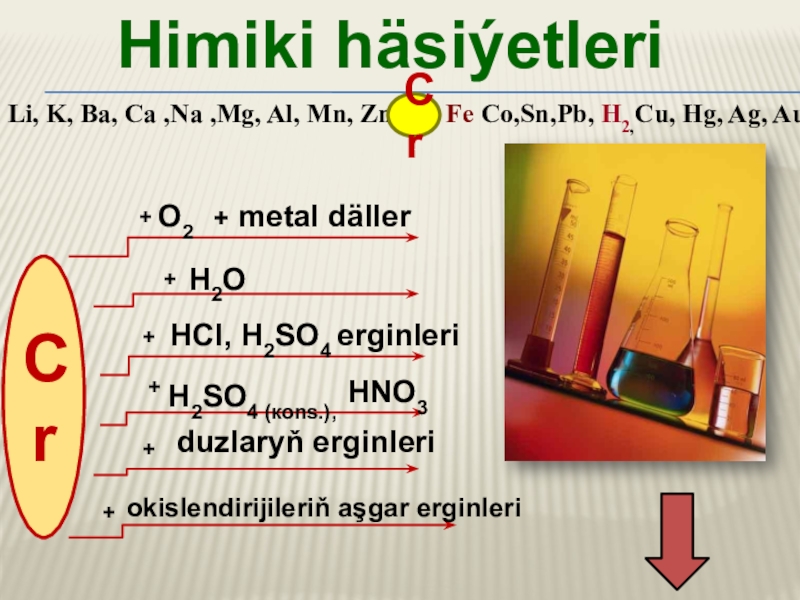
Слайд 12Himiki häsiýetleri
Li, K, Ba, Ca ,Na ,Mg, Al, Mn, Zn,
Cr
Cr
+
+
+
+
H2SO4 (коns.),
duzlaryň erginleri
+ metal däller
О2
HCl, H2SO4 erginleri
H2O
+
okislendirijileriň aşgar erginleri
+
HNO3
Слайд 13 Otag temperaturasynda oksid örtüginiň emele gelmegi netijesinde hrom
Gyzdyrlanda окsid örtügi dargaýar we ol ähli metal däller bilen reaksiýa girýär, mysal üçin:
kislorod, galogenler, аzot, kükürt bilen.
Agzalan maddalar bilen hromyň
reaksiýasynyň
deňlemesini düzüň.
Berlen reaksiýalara
okislenme – gaýtarylma
hökmünde garaň.
Слайд 14 Cr0 + O20 = Cr2+3O3–2
4
2
3
Cr0 –
O20 + 4e → 2O–2 3
Cr0 – gaýtaryjy, okislenme hadysasy
O20 – okislendiriji, gaýtarylma hadysasy
Cr0 + Br20 = Cr+3Br3–1
2
3
2
Cr0 – 3e → Cr+3 2
Br20 + 2e → 2Br–1 3
Cr0 – gaýtaryjy, okislenme hadysasy
Br20 – okislendiriji, gaýtarylma hadysasy
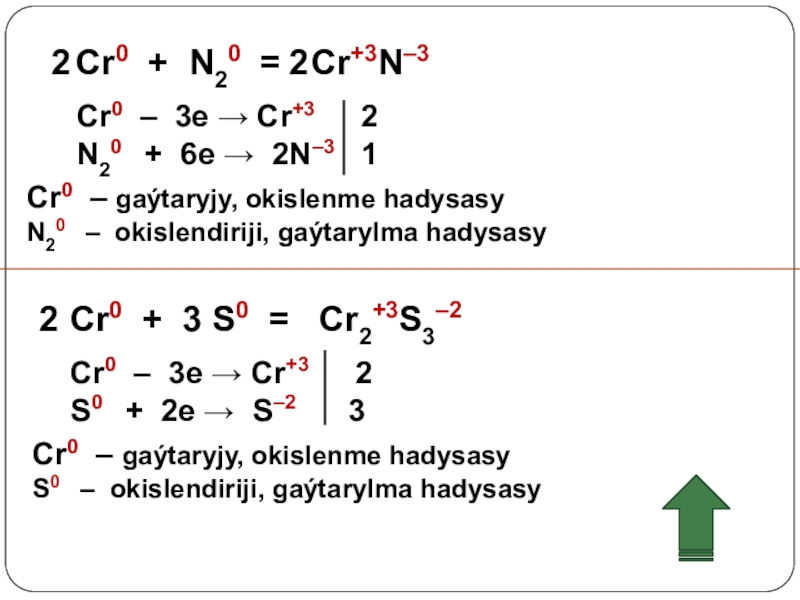
Слайд 15 Cr0 + N20 = Cr+3N–3
Cr0 – 3e
N20 + 6e → 2N–3 1
2
2
Cr0 – gaýtaryjy, okislenme hadysasy
N20 – okislendiriji, gaýtarylma hadysasy
Cr0 + S0 = Cr2+3S3–2
Cr0 – 3e → Cr+3 2
S0 + 2e → S–2 3
2
3
Cr0 – gaýtaryjy, okislenme hadysasy
S0 – okislendiriji, gaýtarylma hadysasy
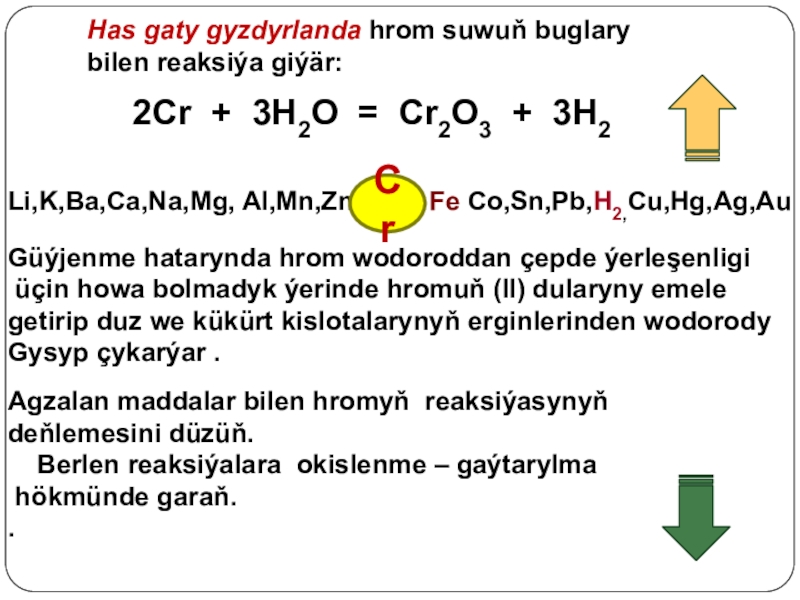
Слайд 16Has gaty gyzdyrlanda hrom suwuň buglary
bilen reaksiýa giýär:
2Cr + 3H2O
Li,K,Ba,Ca,Na,Mg, Al,Mn,Zn, Fe Co,Sn,Pb,H2,Cu,Hg,Ag,Au
Cr
Güýjenme hatarynda hrom wodoroddan çepde ýerleşenligi
üçin howa bolmadyk ýerinde hromuň (II) dularyny emele
getirip duz we kükürt kislotalarynyň erginlerinden wodorody
Gysyp çykarýar .
Agzalan maddalar bilen hromyň reaksiýasynyň
deňlemesini düzüň.
Berlen reaksiýalara okislenme – gaýtarylma
hökmünde garaň.
.
Слайд 17 Cr0 + H+1Cl = Cr+2Cl2
Cr0 – 2e → Cr+2 1
2H+ + 2e → H20 1
2
Cr0 – gaýtaryjy, okislenme hadysasy
HCl (Н+1 hasabyna) – okislendiriji, gaýtarylma hadysasy
Cr0 + H2+1SO4 = Cr+2SO4 + H20
Cr0 – 2e → Cr+2 1
2H+ + 2e → H20 1
Cr0 – gaýtaryjy, okislenme hadysasy
H2SO4(Н+1 hasabyna) – okislendiriji,
gaýtarylma hadysasy
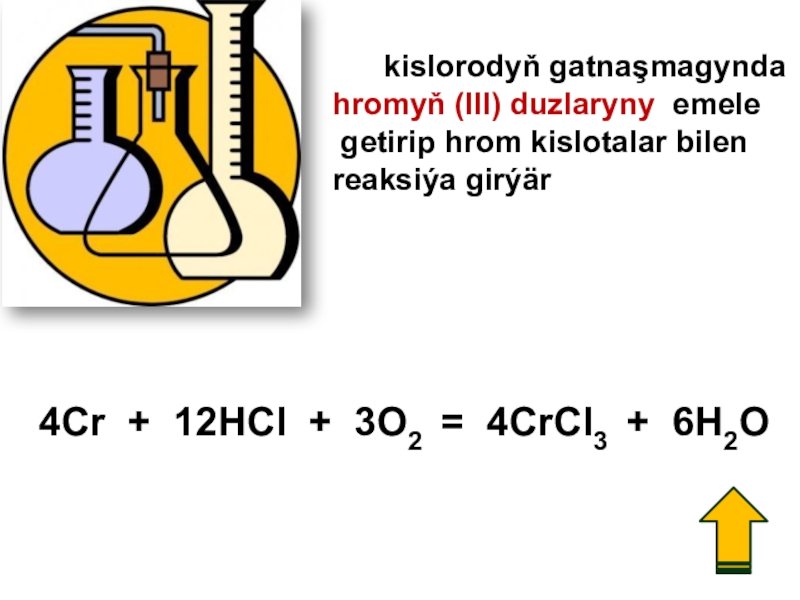
Слайд 18 kislorodyň gatnaşmagynda
hromyň (III) duzlaryny emele
getirip hrom kislotalar
reaksiýa girýär
4Cr + 12HCl + 3O2 = 4CrCl3 + 6H2O
Слайд 19 Коsentrirlenen kükürt we azot kislotalary
sowukda hromy passiwleýärler
Has gyzdyrlanda kislotalar
hrоmyň (III) duzuny emele getirip
eredýärler
Cr + H2SO4 → Cr2(SO4)3 + SO2 + H2O
Cr + HNO3 → Cr(NO3)3 + NO2 + H2O
Berlen reaksiýalara okislenme – gaýtarylma
hökmünde garaň. Koeffisientlerini goýuň.
Okislendirijini we gaýtaryjyny atlandyryň.
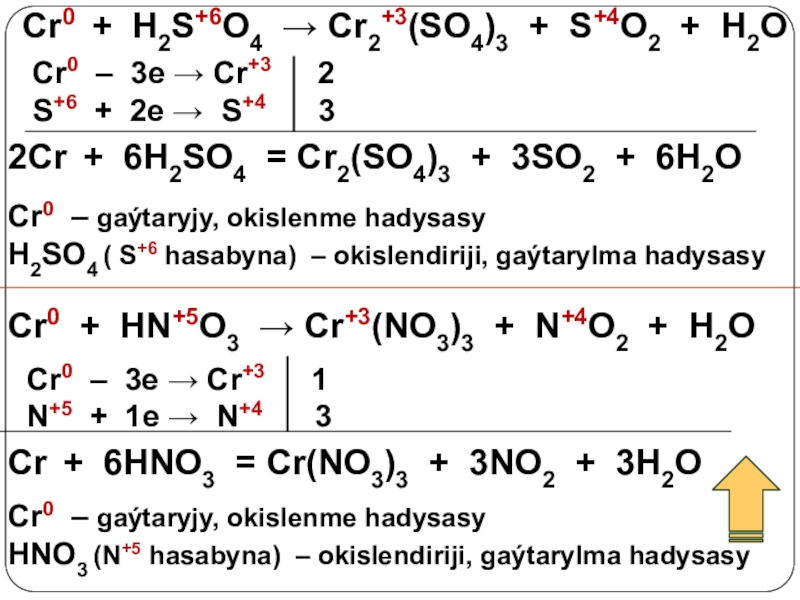
Слайд 20Cr0 + H2S+6O4 → Cr2+3(SO4)3 + S+4O2 + H2O
Cr0 + HN+5O3
Cr0 – 3e → Cr+3 2
S+6 + 2e → S+4 3
2Cr + 6H2SO4 = Cr2(SO4)3 + 3SO2 + 6H2O
Cr0 – gaýtaryjy, okislenme hadysasy
H2SO4 ( S+6 hasabyna) – okislendiriji, gaýtarylma hadysasy
Cr0 – 3e → Cr+3 1
N+5 + 1e → N+4 3
Cr + 6HNO3 = Cr(NO3)3 + 3NO2 + 3H2O
Cr0 – gaýtaryjy, okislenme hadysasy
HNO3 (N+5 hasabyna) – okislendiriji, gaýtarylma hadysasy
Слайд 21Hrom köp metallary olaryň duzlarynyň erginlerinden gysyp çykarýar, mysal üçin misi,
Cr0 + Cu+2SO4 → Cr+2SO4 + Cu0
Hom bilen misiň (II) sulfatynyň okislenme - gaýtarylma reaksiýasyny düzüň.
Cr0 – 2e → Cr+2 1
Cu+2+ 2e → Cu0 1
Cr + CuSO4 = CrSO4 + Cu
Cr0 – gaýtaryjy, okislenme hadysasy
CuSO4 (Cu+2 hasabyna) – okislendiriji,
gaýtarylma hadysasy
Слайд 22Cr + KClO3 + KOH
Berlen reaksiýalara okislenme – gaýtarylma
hökmünde garaň. Koeffisientlerini goýuň.
Okislendirijini we gaýtaryjyny atlandyryň.
Aşgarlaryň erginleri hroma täsir etmeýärler.
Hrom okislendirijileriň aşgarly erginleri bilen reagirleşýär.
Okislendiriji hökmünde natriý, kaliý nitratyny, kaliý hloratyny we beýlekiler ulanylýar.
Okislendirijileriň aşgarly erginleri bilen täsirleşende ýokary okislenme derejäni ýüze çykaryp, anion tipli duzlary emele getirýär.
splawlaşdyrma
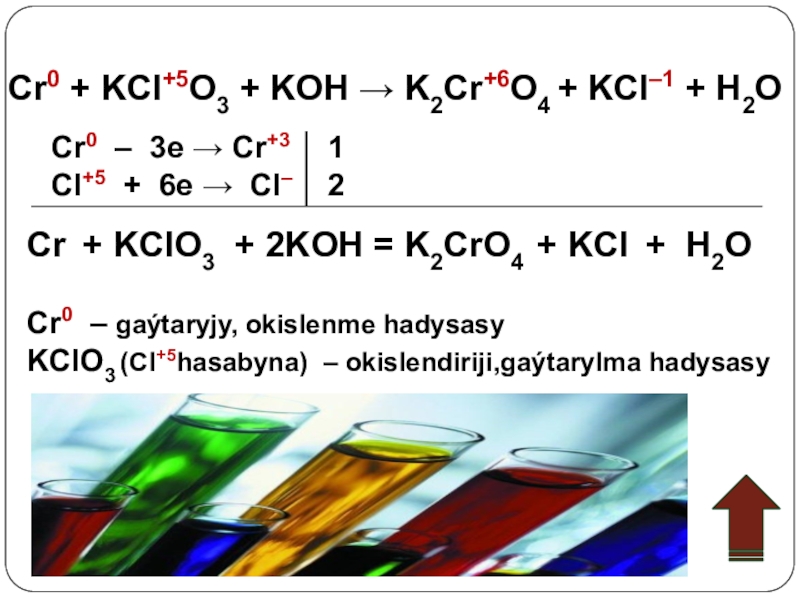
Слайд 23Cr0 + KCl+5O3 + KOH → K2Cr+6O4 + KCl–1 + H2O
Cr0
Cl+5 + 6e → Cl– 2
Cr + KClO3 + 2KOH = K2CrO4 + KCl + H2O
Cr0 – gaýtaryjy, okislenme hadysasy
KClO3 (Cl+5hasabyna) – okislendiriji,gaýtarylma hadysasy
Слайд 24 Hrom – ösümlik we haýwan organizmleriniň hökmany düzüm
Слайд 25 Hrom ром köp sanly legilirlenen poladlaryň wajyp düzüm bölegidir.
hrom-30 we hrom-90, olar awiakosmos önümçiliginde giňden ulanylýarlar.