- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Амины, когда переходила на другой учебник
Содержание
- 1. Амины, когда переходила на другой учебник
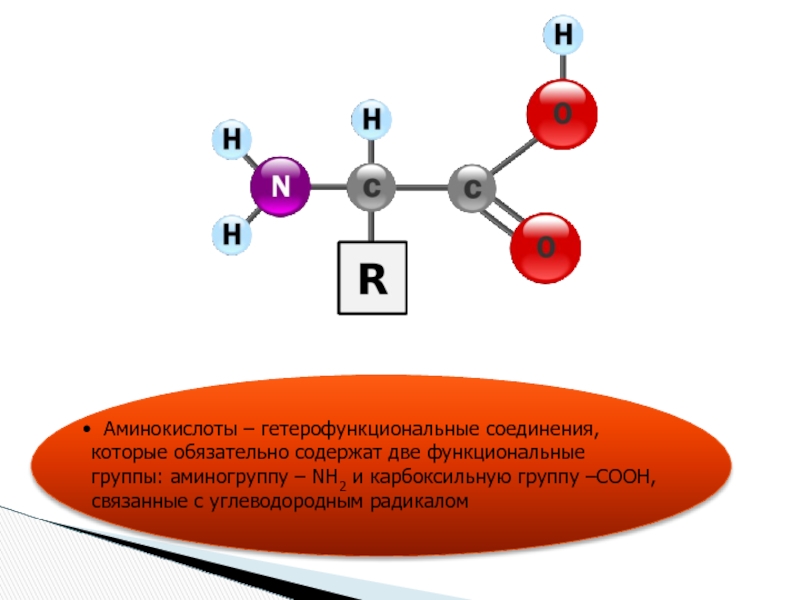
- 2. Аминокислоты – гетерофункциональные соединения, которые обязательно
- 3. Аминокислоты - строительные блоки, из которых строятся
- 4. 1. Аминокислоты могут проявлять как кислотные свойства,
- 5. Аминокислоты применяются в производстве косметики, лекарственных средств,
- 6. Оптическая изомерияОпти́ческая изомери́я (энантиомерия) — разновидность пространственной
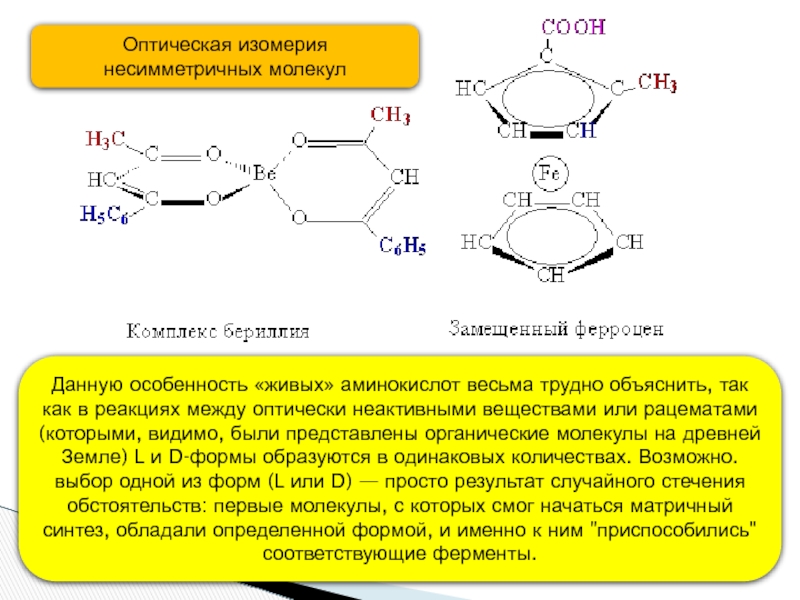
- 7. Данную особенность «живых» аминокислот весьма трудно объяснить,
- 8. Аминокислоты видов D и LКаждая аминокислота существует
- 9. Альфа-аминокислоты белковВ процессе биосинтеза белка в полипептидную
- 10. Классификация стандартных аминокислотНеполярные: аланин, валин, изолейцин, лейцин,
- 11. По функциональным группамАлифатические Моноаминомонокарбоновые: аланин, валин, глицин,
- 12. По аминоацил-тРНК-синтетазамлейцин, изолейцин, валин, цистеин, метионин, аргинин,
- 13. По способности человека синтезировать их из предшественниковНезаменимые:
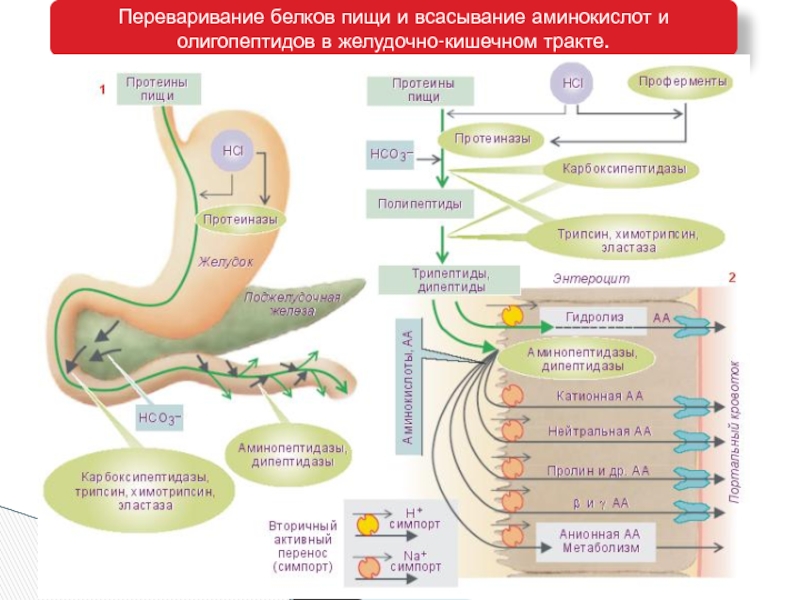
- 14. Переваривание белков пищи и всасывание аминокислот и олигопептидов в желудочно-кишечном тракте.
- 15. Аминокислоты в свободной формеАминокислоты в свободной форме
- 16. уксусная кислота →хлоруксусная кислота→аминоуксусная кислотаСН3-СООН + Сl2
Слайд 2
Аминокислоты – гетерофункциональные соединения, которые обязательно содержат две функциональные группы:
Слайд 3Аминокислоты - строительные блоки, из которых строятся белковые структуры, мышечные волокна,
Слайд 41. Аминокислоты могут проявлять как кислотные свойства, обусловленные наличием в их
Цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH3+, а карбоксигруппа — в виде -COO-. Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот.
Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп. Для этих аминокислот трудно говорить о каком-то конкретном цвиттер-ионе.
Общие химические свойства
Слайд 5Аминокислоты применяются в производстве косметики, лекарственных средств, напитков и пищевых добавок,
Примение
Слайд 6Оптическая изомерия
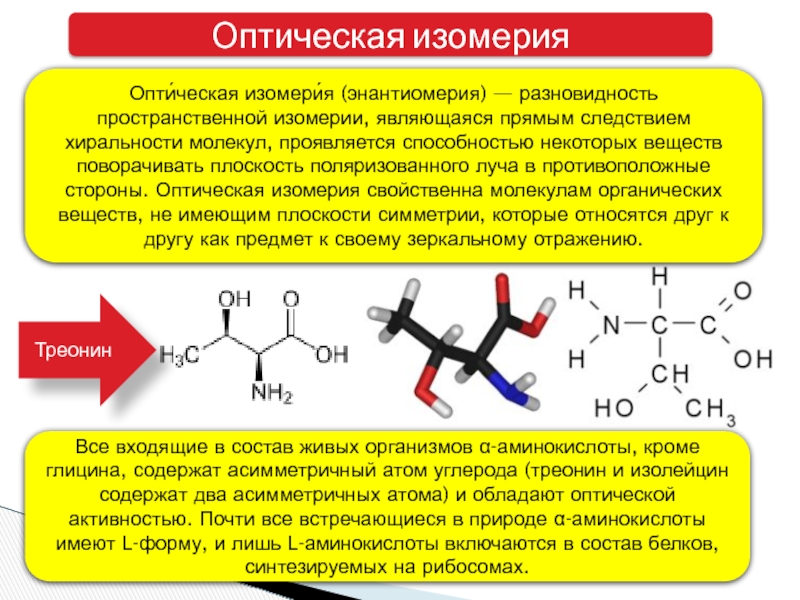
Опти́ческая изомери́я (энантиомерия) — разновидность пространственной изомерии, являющаяся прямым следствием
Все входящие в состав живых организмов α-аминокислоты, кроме глицина, содержат асимметричный атом углерода (треонин и изолейцин содержат два асимметричных атома) и обладают оптической активностью. Почти все встречающиеся в природе α-аминокислоты имеют L-форму, и лишь L-аминокислоты включаются в состав белков, синтезируемых на рибосомах.
Треонин
Слайд 7Данную особенность «живых» аминокислот весьма трудно объяснить, так как в реакциях
Оптическая изомерия несимметричных молекул
Слайд 8Аминокислоты видов D и L
Каждая аминокислота существует в двух формах: D
Эти формы, L и D, зеркально-симметричны: в них массивный боковой радикал (R) и Н-атом, стоящие при a-углероде (Сa) аминокислоты, меняются местами
Слайд 9Альфа-аминокислоты белков
В процессе биосинтеза белка в полипептидную цепь включаются 21 важнейших
Лейцин (Leu, L)
Лизин (Lys, K)
Метионин (Met, M)
Пролин (Pro, P)
Серин (Ser, S)
Тирозин (Tyr, Y)
Треонин (Thr, T)
Триптофан (Trp, W)
Фенилаланин (Phe,F)
Цистеин (Cys, C)
Cеленцистеиновая
Помимо этих аминокислот, называемых стандартными, в некоторых белках присутствуют специфические нестандартные аминокислоты, являющиеся производными стандартных. В последнее время к стандартным аминокислотам иногда причисляют селеноцистеин (Sec, U) и пирролизин (Pyl, O).
Слайд 10Классификация стандартных аминокислот
Неполярные: аланин, валин, изолейцин, лейцин, метионин, пролин, триптофан, фенилаланин,
Полярные незаряженные (заряды скомпенсированы) при pH=7: аспарагин, глутамин, серин, тирозин, треонин, цистеин
Полярные заряженные отрицательно при pH=7: аспарагиновая кислота, глутаминовая кислота
Полярные заряженные положительно при pH=7: аргинин, гистидин, лизин
По R-группам
Слайд 11По функциональным группам
Алифатические
Моноаминомонокарбоновые: аланин, валин, глицин, изолейцин, лейцин
Оксимоноаминокарбоновые: серин, треонин
Моноаминодикарбоновые:
Амиды Моноаминодикарбоновых: аспарагин, глутамин
Диаминомонокарбоновые: аргинин, гистидин, лизин, несут в растворе положительный заряд
Серосодержащие: цистеин (цистин), метионин
Ароматические: фенилаланин, тирозин
Гетероциклические: триптофан, гистидин, пролин (также входит в группу иминокислот)
Иминокислоты: пролин (также входит в группу гетероциклических)
Слайд 12По аминоацил-тРНК-синтетазам
лейцин, изолейцин, валин, цистеин, метионин, аргинин, глутаминовая кислота, глутамин, тирозин
Класс
Класс II
аланин, глицин, пролин, гистидин, треонин, серин, аспарагин, аспарагиновая кислота, лизин, фенилаланин
Слайд 13По способности человека синтезировать их из предшественников
Незаменимые: Триптофан Фенилаланин Лизин Треонин
Заменимые: Тирозин Цистеин Гистидин Аргинин Глицин Аланин Серин Глутамат Глутамин Аспартат Аспарагин Пролин
Некоторые заменимые аминокислоты синтезируются в организме человека в недостаточных количествах и должны поступать с пищей.
Слайд 14Переваривание белков пищи и всасывание аминокислот и олигопептидов в желудочно-кишечном тракте.
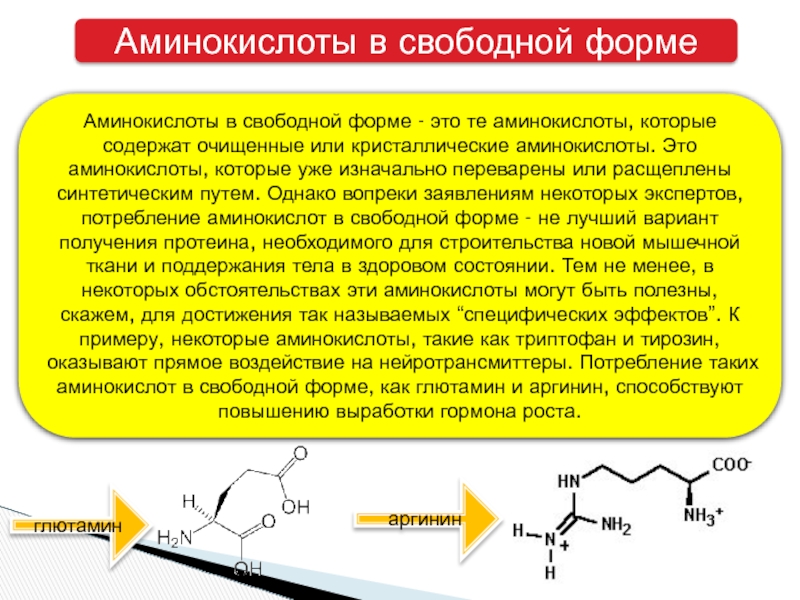
Слайд 15Аминокислоты в свободной форме
Аминокислоты в свободной форме - это те аминокислоты,
глютамин
аргинин
Слайд 16
уксусная кислота →хлоруксусная кислота→аминоуксусная кислота
СН3-СООН + Сl2 → СН2-СООН
Cl
СН2-СООН + NH3 → СН2-СООН
| |
Сl NH2
Способы получения
гидролиз белков
Промышленный:
Лабораторный