- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Альдегидтердің де, кетондардың да құрамында карбонил тобы болғандықтан, бұл екі қосылыс карбонилді қосылыстар деп аталады да, екеуін бірге қарайды.
Содержание
- 1. Альдегидтердің де, кетондардың да құрамында карбонил тобы болғандықтан, бұл екі қосылыс карбонилді қосылыстар деп аталады да, екеуін бірге қарайды.
- 2. Жоспар1.Карбонил тобының табиғаты 2.Химиялық қасиеттері
- 3. Альдегид және кетондарКарбонил тобы С=О
- 4. Алу жолдарыАльдегидпен кетондардың алу жолдарында біраз ұқсастықтар
- 5. Екіншілік спирттерді тотықтырып немесе тотықсыздандырып кетон алуға
- 6. Карбон қышқылдарының тұздарынан алу. Карбон қышқылдарының барий
- 7. 4.Альдегидтермен кетондарды, бу күйіндегі қышқылдарды 450-5000С –де
- 8. Дигалоген туындыларды гидролиздеу. Қолданылатын молекулада екі галоген
- 9. Слайд 9
- 10. Химиялық қасиеттері. Сонымен, карбонил тобында –көміртек отегімен
- 11. Кетондарға қарағанда, альдегидтер нуклеофильді қосылу реакциясына жеңіл
- 12. 2.Спирттердің қосылуы. Карбонилді қосылыстар спирттермен әрекеттесіп бір
- 13. Екінші саты-лимитирлеуші саты-түзілген күшті электрофильді орталық Льюис
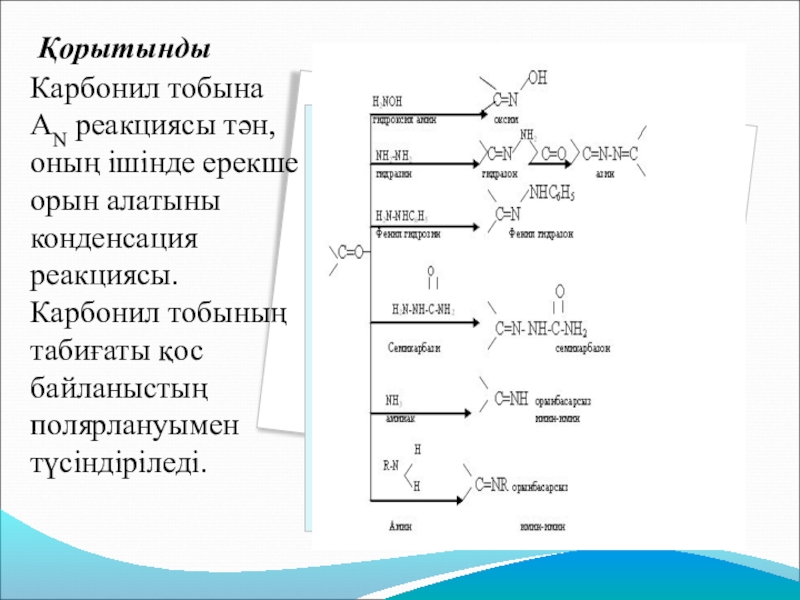
- 14. ҚорытындыКарбонил тобына АN реакциясы тән, оның
- 15. 1 - тапсырмаФормальдегидтің формуласы, кұрылысы?Формальдегидке анықтама?
- 16. Формальдегид (лат. formica - құмырсқа),
- 17. 2-тапсырмаФармалин формуласы?Медицинада пайдалануы?Ауыл шаруашылығында пайдасы?
- 18. Формалин, формаль — формальдегидтің судағы 37 — 40%-дық ерітіндісі. Формалинді
- 19. 3 – тапсырма Реакцияны ата?
- 20. Күміс айна реакциясы!
- 21. Назарларыңызға рахмет!!!
Жоспар1.Карбонил тобының табиғаты 2.Химиялық қасиеттері
Слайд 3Альдегид және кетондар
Карбонил тобы С=О екі қосылыста кездеседі. Егер
карбонил тобы бір көмірсутек қылдығымен және бір сутек атомымен байланысса, оны альдегид деп атайды, ал карбонил тобы көмірсутек қалдығының екеуімен байланысса- кетон дейді.
R-C=O немесе RCHO R-C=O немесе R2CO
H R
Альдегидтердің де, кетондардың да құрамында карбонил тобы болғандықтан, бұл екі қосылыс карбонилді қосылыстар деп аталады да, екеуін бірге қарайды. Химиялық қасиетін анықтайтын карбонил тобы болғандықтан, екеуінің қасиеттерінде де, алу әдістерінде де көп ұқсастықтар бар, бірақ карбонил тобының бір жағдайда бір органикалық радикалдармен және сутегімен байланысуы, екіншісінің екі органикалық радикалдармен байланысуы, екеуінің әр қайсысына әр түрлі ерекшеліктер береді.
R-C=O немесе RCHO R-C=O немесе R2CO
H R
Альдегидтердің де, кетондардың да құрамында карбонил тобы болғандықтан, бұл екі қосылыс карбонилді қосылыстар деп аталады да, екеуін бірге қарайды. Химиялық қасиетін анықтайтын карбонил тобы болғандықтан, екеуінің қасиеттерінде де, алу әдістерінде де көп ұқсастықтар бар, бірақ карбонил тобының бір жағдайда бір органикалық радикалдармен және сутегімен байланысуы, екіншісінің екі органикалық радикалдармен байланысуы, екеуінің әр қайсысына әр түрлі ерекшеліктер береді.
Слайд 4Алу жолдары
Альдегидпен кетондардың алу жолдарында біраз ұқсастықтар бар және әр қайсысының
өзіне тән айырмашылықтары да бар.
Спирттерді тотықтыру.
Біріншілік спирттерді тотықтырса альдегид түзіледі:
О
СН3 -СН2 -ОН +K2Cr2O7+H2SO4 СН3 -С
Н
Басқа органикалық қосылыстар класының ішінде ең жеңіл тотығны альдегид, сондықтан түзілген альдегид ары қарай тотығып карбон қышқылына айналу мүмкін. Сондықтан тотығу процесін өте сақтықпен жүргізу керек. Тотықтыру әдісінен гөрі дұрысырақ әдіс спиртті қыздырылған мас арқылы жіберіп, түзілген өнім ары қарай химиялық өзгеріске түспейді:
О
СН3 СН2 СН2СН2ОН СН,250-3000С СН3 СН2 СН2С
Н
Спирттерді тотықтыру.
Біріншілік спирттерді тотықтырса альдегид түзіледі:
О
СН3 -СН2 -ОН +K2Cr2O7+H2SO4 СН3 -С
Н
Басқа органикалық қосылыстар класының ішінде ең жеңіл тотығны альдегид, сондықтан түзілген альдегид ары қарай тотығып карбон қышқылына айналу мүмкін. Сондықтан тотығу процесін өте сақтықпен жүргізу керек. Тотықтыру әдісінен гөрі дұрысырақ әдіс спиртті қыздырылған мас арқылы жіберіп, түзілген өнім ары қарай химиялық өзгеріске түспейді:
О
СН3 СН2 СН2СН2ОН СН,250-3000С СН3 СН2 СН2С
Н
Слайд 5Екіншілік спирттерді тотықтырып немесе тотықсыздандырып кетон алуға болады. Түзілген кетон ары
қарай тотықпайды.
Спирттердің тотығып карбонилді қосылыстарды түзуін спирттердің химиялық қасиетін толық айтқанбыз.
Хлорангидридтерді тотықсыздандыру. Альдегшидтерді алуда бұл әдіс басқа әдістерденгөрі дұрысрақ, себебі түзілген альдегид ары қарай химиялық өзгеріске, яғни спиртке дейін тотықсызданбайды. Тотықсыздандырғаш-литийдің триүшіншілік бутоксиалюмогидриді, бұл арнайы тотықсыздандырғыш, темперетура төмен.
Спирттердің тотығып карбонилді қосылыстарды түзуін спирттердің химиялық қасиетін толық айтқанбыз.
Хлорангидридтерді тотықсыздандыру. Альдегшидтерді алуда бұл әдіс басқа әдістерденгөрі дұрысрақ, себебі түзілген альдегид ары қарай химиялық өзгеріске, яғни спиртке дейін тотықсызданбайды. Тотықсыздандырғаш-литийдің триүшіншілік бутоксиалюмогидриді, бұл арнайы тотықсыздандырғыш, темперетура төмен.
Слайд 6Карбон қышқылдарының тұздарынан алу. Карбон қышқылдарының барий немесе калций тұздарын пиролиздеп
альдегидте, кетонда алуға болады.
Альдегид алу үшін қышқыл тұздарының құрамындағы екі қышқыл қалдығының біреуі тек құмырсқа қышқылының қалдығы болу керек, кетон алу үшін мүндай шектеу қойылмайды:
құмырсқа май қышқылының кальций тұзы
Қышқылдардың аралас кальций тұзын түзудің керегі жоқ, әр түрлі екі қышқылдың тұздарынан үлкен сақтықпен қоспа даярласада болады, мысалы:
О
(СН3-СОО)2Са+(НСОО)2Са пиролиз 2СН3С +2СаСО3
кальций ацетаты калций формиаты Н
Альдегид алу үшін қышқыл тұздарының құрамындағы екі қышқыл қалдығының біреуі тек құмырсқа қышқылының қалдығы болу керек, кетон алу үшін мүндай шектеу қойылмайды:
құмырсқа май қышқылының кальций тұзы
Қышқылдардың аралас кальций тұзын түзудің керегі жоқ, әр түрлі екі қышқылдың тұздарынан үлкен сақтықпен қоспа даярласада болады, мысалы:
О
(СН3-СОО)2Са+(НСОО)2Са пиролиз 2СН3С +2СаСО3
кальций ацетаты калций формиаты Н
Слайд 7
4.Альдегидтермен кетондарды, бу күйіндегі қышқылдарды
450-5000С –де кейбір металдар тотығының (ThO2,
MnO2,CaO,ZnO) үстімен жүргізіп пиролиздеу арқылы да алуға болады, бұл өте ыңғайлы әдіс.
Слайд 8Дигалоген туындыларды гидролиздеу. Қолданылатын молекулада екі галоген бір көміртек (геминалды) орналасқан
болу керек.
Альдегидтер алу үшін геминалды дигалоген көміртек тізбегінің шетінде тұруы керек.
1,1-дихлорпропан пропандиол-1,1 пропаналь
Кетонды алу үшін геминалды дигалоген көміртек тізбегінің : ортасында орналасқан болу керек:
Альдегидтер алу үшін геминалды дигалоген көміртек тізбегінің шетінде тұруы керек.
1,1-дихлорпропан пропандиол-1,1 пропаналь
Кетонды алу үшін геминалды дигалоген көміртек тізбегінің : ортасында орналасқан болу керек:
Слайд 9 Физикалық қасиеті. Альдегиді —
өткір иісті газ, сірке альдегидінен бастап келесі мүшелері — сұйық, Ал жоғарғылары — қатты заттар. Молекулалық массалары өскен сайын балқу және қайнау температурасы артады. Спирттерден өзгешелігі — альдегидтерде молекулааралық сутектік байланыс түзілмейді, сондықтан сәйкес спирттермен салыстырғанда қайнау температуралары төмен болады.
"Альдегидтер"
Барлық альдегидтер органикалық еріткіштерде жақсы ериді. Химиялық қасиеттері. Құрамында еселі байланыс болғандық- тан, карбонилді қосылыстарға қосылу реакциясы тән. Қосылатын реагенттің теріс зарядталған бөлігі көміртек атомына, ал оң зарядталған бөлігі оттек атомына қосылады.
Слайд 10Химиялық қасиеттері. Сонымен, карбонил тобында –көміртек отегімен қос байланыспен байланысқан. Альдегид
пен кетондардың химиялық қасиетін анықтайтын осы карбонил тобы. Олай болса, альдегидтер мен кетондардың карбонил тобы қосылу реакциясына бейім деген қортынды жасалады. Біз қос байланысты қосылыстармен таныспыз, мысалы, алкендер. Тек айырмашылығы, алкендерде көміртек- көміртекті қос байланыс. Енді осы
екі қосылыстың қосылу реакцияларында қандай ерекшеліктер бар екенін білу үшін қос байланыстардың сипаттамаларын салыстырайық.
екі қосылыстың қосылу реакцияларында қандай ерекшеліктер бар екенін білу үшін қос байланыстардың сипаттамаларын салыстырайық.
Слайд 11Кетондарға қарағанда, альдегидтер нуклеофильді қосылу реакциясына жеңіл түседі. Реакциялық қабілеттерінің айырмашылығы
электрондық және кеңістіктегі фақторлардың қатар әрекеті болса керек. Кетон молекуласында екінші алкил тобы болса, альдегидте-сутегі. әрине, екі орынбасардың көлемдері әр түрлі. Кетонның екінші алкил тобы өткелді күйдегі кеңістіктегі кедергіні көбейтіп жібереді. Оған қосымша, алкил тобының электрон беруі нәтижесінде оттегінің теріс зарияды көбейеді де, аралық күйдің тұрақтылығын азайтады. Сол себепті кетон, альдегидке қарағанда реакцияға нашар түседі.
Альдегид пен кетондарға қосылатын нуклеофильдерді қосылу жағдайына, активтейтін катализаторына тағы да басқа сипаттамаларына қарай үшке топтауға болады.
1.Льюис негіздерін қосу.
2.Псевдоқышқылдарды(С-Н қышқылдарды) қосу.
3.Крипто негіздерін қосу.
Альдегид пен кетондарға қосылатын нуклеофильдерді қосылу жағдайына, активтейтін катализаторына тағы да басқа сипаттамаларына қарай үшке топтауға болады.
1.Льюис негіздерін қосу.
2.Псевдоқышқылдарды(С-Н қышқылдарды) қосу.
3.Крипто негіздерін қосу.
Слайд 122.Спирттердің қосылуы. Карбонилді қосылыстар спирттермен әрекеттесіп бір немесе екі алкокситоптарын (-ОR)
қосып алады. Альдегидтердің құрамына бір алкокси-қалдығы негенде-жартылай, екеуі енгенде-толық ацеталь түзілсе, кетондар жағдайында-жартылай кеталь немесе кеталь түзіледі.
Рекция механизмі. Гидаратациялау реакциясы және полуацеталь түзілуі-қышқылдық катализдің қатысуымен жүреді.
Бірінші саты-әлсіз электрофильді орталығы бар карбонил тобы негіз ретінде күшті қышқылмен әрекеттескенде күшті электрофильді орталық пайда болады:
Рекция механизмі. Гидаратациялау реакциясы және полуацеталь түзілуі-қышқылдық катализдің қатысуымен жүреді.
Бірінші саты-әлсіз электрофильді орталығы бар карбонил тобы негіз ретінде күшті қышқылмен әрекеттескенде күшті электрофильді орталық пайда болады:
Слайд 13
Екінші саты-лимитирлеуші саты-түзілген күшті электрофильді орталық Льюис негізімен әрекеттеседі.
Үшінші сатысы-түзілген аралық
қосылу өнімінен, қышқыл анионы протонды жұлып алып, соңғы өнім түзіледі.
4.Аммиак туындыларының қосылуы. Аммиактың кебір туындылары карбонил тобына қосылып, карбонилді қосылыстар (альдегид немесе кетон) құрамынан су бөлінеді де С=О байланысының орнына көміртек-азот қос байланысы түзіледі.
4.Аммиак туындыларының қосылуы. Аммиактың кебір туындылары карбонил тобына қосылып, карбонилді қосылыстар (альдегид немесе кетон) құрамынан су бөлінеді де С=О байланысының орнына көміртек-азот қос байланысы түзіледі.
Слайд 14 Қорытынды
Карбонил тобына АN реакциясы тән, оның ішінде ерекше орын алатыны
конденсация реакциясы. Карбонил тобының табиғаты қос байланыстың полярлануымен түсіндіріледі.
Слайд 16 Формальдегид (лат. formica - құмырсқа), халықаралық уағыздалатын аты - метаналь, ескіше - құмырсқа алдегиды. Екінші кластағы аса қауіпті
түссіз газ. Ол адамның тыныс алу жолдарына, көзге және теріге аса зиян. Және адамның жүйке жүйесін зақымдайды. Егер оның мөлшері ауадағы зиянды заттардың қауіпсіз мөлшерінен неше жүз есеге асып кетсе, барлық тірі жанды құртып жіберуі ғажап емес дейді мамандар. Формальдегид негізінен көлік газдарынан тарайды.
(CH2=O) — газсынды өткір иісті түссіз зат , гомологиялық қатардың алифатикалық альдегидтер болатын алғашқы мүшесі. Формальдегидтің 40%-тік ерітіндісін формалин деп атайды.
Слайд 18Формалин, формаль — формальдегидтің судағы 37 — 40%-дық ерітіндісі. Формалинді полимерленуден сақтау үшін 4 —
12%-дай метил спирті қосылады. Сондықтан 1%-дық метанол деп те атайды. Формалин түссіз, өткір иісті сұйықтық. Ұзақ сақталса (әсіресе суықта) ақ түсті тұнба параформальдегид (параформ) түзіп лайланады. Формалиннің микробтарға қарсы әсері және денені тітіркендіру қабілеті болғандықтан клетка протоплазмасындағы белокпен әрекеттесіп, оны ұйытады және клетканы өлтіреді. Формалин ауланы, киімдерді, ыдыстарды дезинфекциялау ісінде пайдаланылады. Ол зертханаларда анатомилық және микроскопиялық препараттарды сақтауда, ауыл шаруашылығында тұқымды дәрілеу үшін, парниктерді, әр түрлі құбырларды дезинфекциялауда, тері илеуде, фенол-фармальдегидті шайырлар алуда қолданылады.