- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Материалы урока: Ионная кристаллическая решетка
Содержание
- 1. Материалы урока: Ионная кристаллическая решетка
- 2. ВВЕДЕНИЕ. КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ. Твердые вещества, как
- 3. Точки, в которых размещены
- 4. ИОННАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Ионными называют кристаллические
- 5. Ионную связь (K+)−(I−) рассматривают как предельный
- 6. ПРИМЕРЫ ВЕЩЕСТВ Соли, оксиды и гидроксиды
- 7. ПРИМЕРЫ ВЕЩЕСТВ Рассмотрим строение кристалла
- 8. СВОЙСТВА ВЕЩЕСТВ Тугоплавкие, нелетучие, твердые, многие
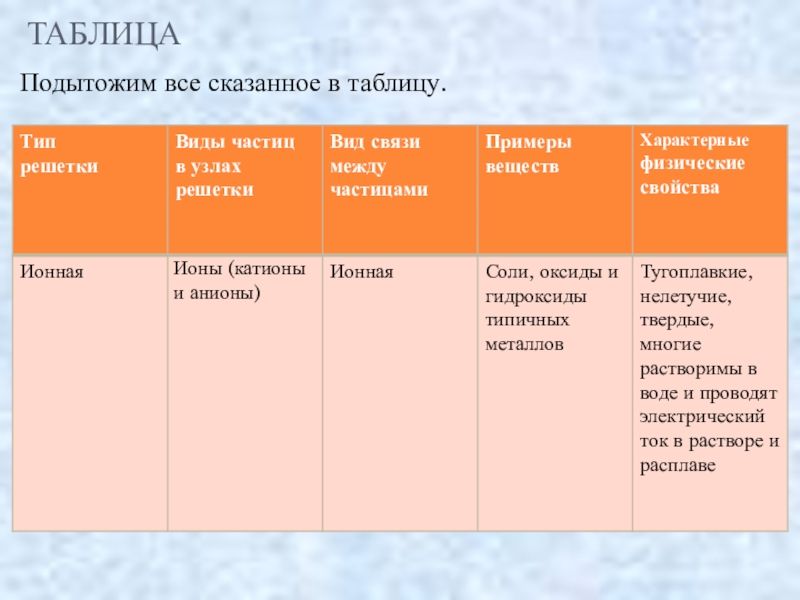
- 9. ТАБЛИЦАПодытожим все сказанное в таблицу.
- 10. МАТЕРИАЛ:http://www.alhimik.ru/teleclass/konspect/konsp3-10.shtmlhttp://www.himhelp.ru/section23/section3/section21/http://alhimikov.net/elektronbuch/Page-11.htmlСсылки на ресурсы
- 11. КАРТИНКИ:http://popnano.ruhttp://fisclub.ru/prim23/11/kris8.htmhttp://fiz.1september.ru/article.php?ID=200600409http://www.stfc.ac.uk/Public%20and%20Schools/1411.aspxhttp://him.1september.ru/articlef.php?ID=200403906http://www.catalogmineralov.ru/sample/5424.htmlhttp://him.1september.ru/articlef.php?ID=200403906http://www.hemi.nsu.ru/ucheb139.htmhttp://filinajewelry.ru/dragkamni.html
ВВЕДЕНИЕ. КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ. Твердые вещества, как правило, имеют кристаллическое строение. Оно характеризуется правильным расположением частиц в строго определенных точках пространства. При мысленном соединении этих точек пересекающимися прямыми линиями образуется пространственный каркас, который называют кристаллической решеткой.
Слайд 2ВВЕДЕНИЕ. КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ.
Твердые вещества, как правило, имеют кристаллическое строение.
Оно характеризуется правильным расположением частиц в строго определенных точках пространства. При мысленном соединении этих точек пересекающимися прямыми линиями образуется пространственный каркас, который называют кристаллической решеткой.
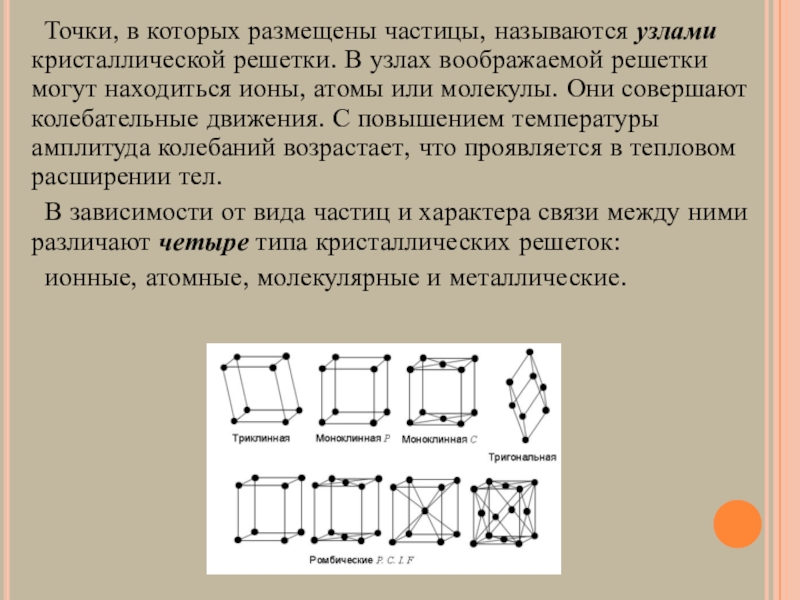
Слайд 3 Точки, в которых размещены частицы, называются узлами кристаллической решетки.
В узлах воображаемой решетки могут находиться ионы, атомы или молекулы. Они совершают колебательные движения. С повышением температуры амплитуда колебаний возрастает, что проявляется в тепловом расширении тел.
В зависимости от вида частиц и характера связи между ними различают четыре типа кристаллических решеток:
ионные, атомные, молекулярные и металлические.
В зависимости от вида частиц и характера связи между ними различают четыре типа кристаллических решеток:
ионные, атомные, молекулярные и металлические.
Слайд 4ИОННАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
Ионными называют кристаллические решетки, в узлах которых
находятся ионы. Их образуют вещества с ионной связью.
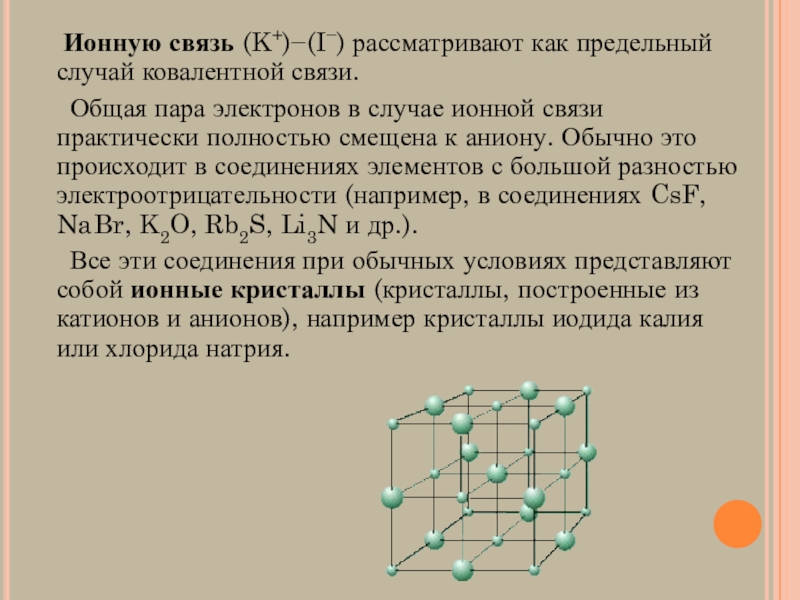
Слайд 5 Ионную связь (K+)−(I−) рассматривают как предельный случай ковалентной связи.
Общая пара электронов в случае ионной связи практически полностью смещена к аниону. Обычно это происходит в соединениях элементов с большой разностью электроотрицательности (например, в соединениях CsF, NaBr, K2O, Rb2S, Li3N и др.).
Все эти соединения при обычных условиях представляют собой ионные кристаллы (кристаллы, построенные из катионов и анионов), например кристаллы иодида калия или хлорида натрия.
Все эти соединения при обычных условиях представляют собой ионные кристаллы (кристаллы, построенные из катионов и анионов), например кристаллы иодида калия или хлорида натрия.
Слайд 6ПРИМЕРЫ ВЕЩЕСТВ
Соли, оксиды и гидроксиды типичных металлов.
Рассмотрим
кристалл хлорида натрия, в котором, как уже отмечалось, каждый ион натрия окружен шестью хлорид-ионами, а каждый хлорид-ион - шестью ионами натрия. Такому расположению соответствует наиболее плотная упаковка, если ионы представить в виде шаров, размещенных в кристалле.
Слайд 7ПРИМЕРЫ ВЕЩЕСТВ
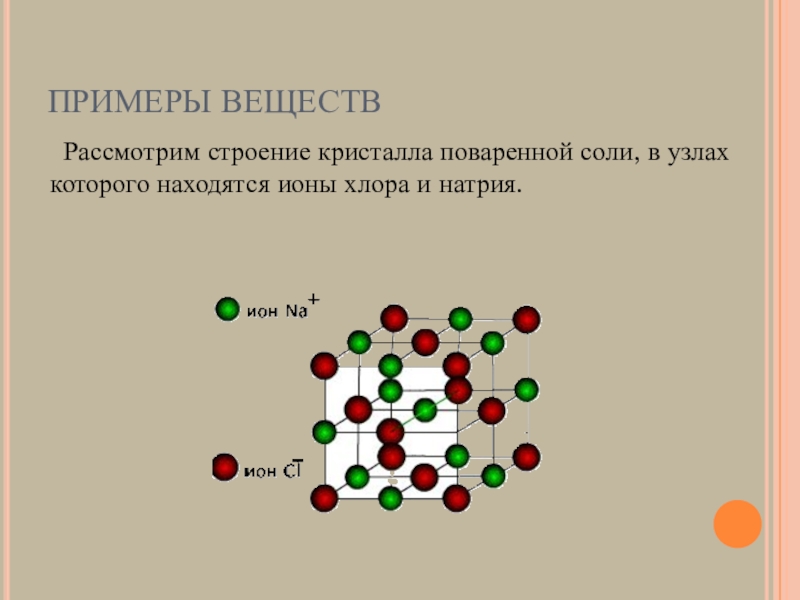
Рассмотрим строение кристалла поваренной соли, в узлах
которого находятся ионы хлора и натрия.
Слайд 8СВОЙСТВА ВЕЩЕСТВ
Тугоплавкие, нелетучие, твердые, многие растворимы в воде и
проводят электрический ток в растворе и расплаве.