- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по внеклассному занятию Последам химических элементов
Содержание
- 1. Презентация по внеклассному занятию Последам химических элементов
- 2. Внеклассное занятие «По следам химических элементов»Внеклассное занятие
- 3. Цель проведения занятия:Тип занятия: занятие практического приобретения
- 4. Этапы занятия: Актуализация знаний и формирование мотива
- 5. Этап 1. Актуализация знаний.Свойства химических элементов находятся
- 6. Ответ: Периодический закон, графическим изображением которого является Периодическая таблица Д.И. Менделеева.
- 7. Этап 1. Актуализация знаний.1.2. С какой целью
- 8. Этап 1. Актуализация знаний.1.3. Назовите химический элемент,
- 9. Ответ: В честь Д.И. Менделеева был назван 101 элемент, которому дали название Менделевий.
- 10. Этап 1. Актуализация знаний.1.4. Вы работаете в
- 11. Возможные варианты ответа: Данные соли содержат разные
- 12. Исследовательская работа № 2.1.Качественные реакции на катионы.Цель:
- 13. Исследовательская работа № 2.1. Качественные реакции на
- 14. Исследовательская работа № 2.2. Цель: наблюдение реакции
- 15. Результаты работы:
- 16. Исследовательская работа №2.3. Наблюдение реакции окрашивания пламени
- 17. Результаты работы:
- 18. Слайд 18
- 19. Исследовательская работа №2.4. Наблюдение спектральных линий пламени
- 20. Вывод (результаты работы): Атомы каждого химического элемента
- 21. Исследовательская работа № 2.5. Наблюдение спектров различных
- 22. Вывод (результаты работы):
- 23. Вывод (результаты работы):Вывод (результаты работы): Атомы каждого
- 24. Этап 3. Закрепление знаний.Задание 3.1. На рисунке
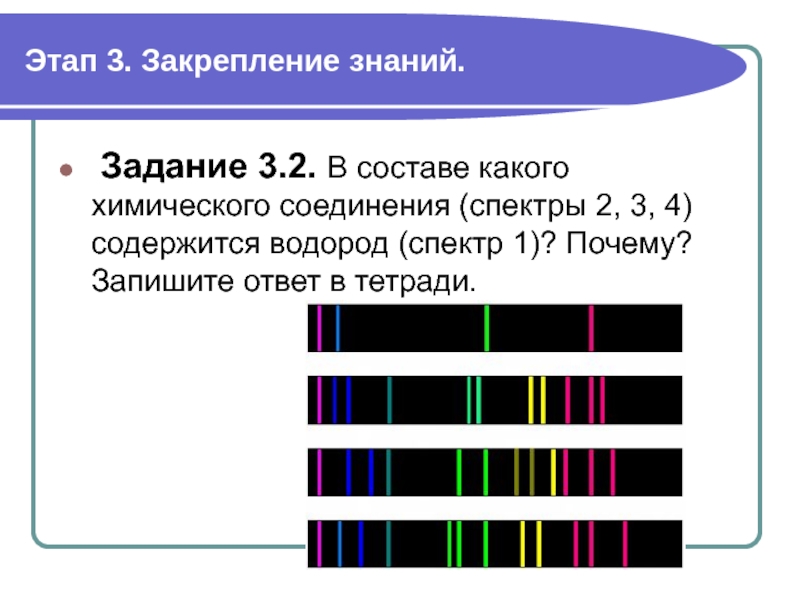
- 25. Этап 3. Закрепление знаний. Задание 3.2. В
- 26. Ответы:Ответ: 23 (задание 3.1)Ответ: 4 (задание 3.2)
- 27. Этап 3. Закрепление знаний.Задание 3.3. Рассмотрите таблицу
- 28. Этап 3. Закрепление знаний. Спектры химических элементов
- 29. Ответ: Линейчатые спектры излучения различных химических элементов
- 30. Этап 4. Оценочно-аналитический4.1. Сформулируйте общий вывод занятия,
- 31. Этап 4. Оценочно-аналитический.4.2. Перескажите русскую пословицу при помощи физических терминов. Каков пан, таков на нем и жупан.
- 32. 4.3. Игра «Правда или ложь». Мы выбрали несколько фактов о
- 33. Игра «Правда или ложь». С помощью спектрального анализа можно получить
- 34. 4.3. Игра «Правда или ложь». Основные преимущества спектроскопии перед другими
- 35. Спасибо за внимание! Сколько элементов в таблице
Слайд 2Внеклассное занятие
«По следам химических элементов»
Внеклассное занятие подготовили:
Малахов
Алексей Александрович,
учитель физики,
МАОУ СОШ № 22 города Тюмени
2019 г
Слайд 3Цель проведения занятия:
Тип занятия:
занятие практического приобретения и применения знаний.
познакомиться с
при определении химического состава вещества;
изучить спектры светящихся газов.
Слайд 4Этапы занятия:
Актуализация знаний и формирование мотива для углубления предметных знаний.
Углубление
Закрепление знаний.
Оценочно-аналитический этап.
Слайд 5Этап 1. Актуализация знаний.
Свойства химических элементов находятся в периодической зависимости от
зарядов ядер их
атомов
1.1.Назовите закон, формулировка которого звучит так:
Слайд 6Ответ:
Периодический закон, графическим изображением которого является Периодическая таблица Д.И. Менделеева.
Слайд 7Этап 1. Актуализация знаний.
1.2. С какой целью Организация Объединенных Наций назвала
Возможный вариант ответа: в целях повышения осведомленности мировой общественности о фундаментальных науках и расширения образования в области фундаментальных наук.
Слайд 8Этап 1. Актуализация знаний.
1.3. Назовите химический элемент, который синтезировали в 1955
Слайд 10Этап 1. Актуализация знаний.
1.4. Вы работаете в лаборатории и решили провести
Слайд 11Возможные варианты ответа:
Данные соли содержат разные анионы и разные
Катионы металлов при внесении их солей в пламя окрашивают его в определенный цвет.
Слайд 12Исследовательская работа № 2.1.
Качественные реакции на катионы.
Цель: использование качественных реакций для
Оборудование (экспериментальная установка): растворы солей LiCl и Na3PO4, химическая посуда.
Слайд 13Исследовательская работа № 2.1. Качественные реакции на катионы.
Порядок работы:
Смешать
Пронаблюдать химическую реакцию;
Записать уравнение химической реакции и сделать выводы.
Результаты работы:
катион лития с фосфат-ионом дает белый осадок: 3LiCl+ Na3PO4→ Li3PO4↓+3NaCl
Слайд 14Исследовательская работа № 2.2.
Цель: наблюдение реакции окрашивания пламени при помещении
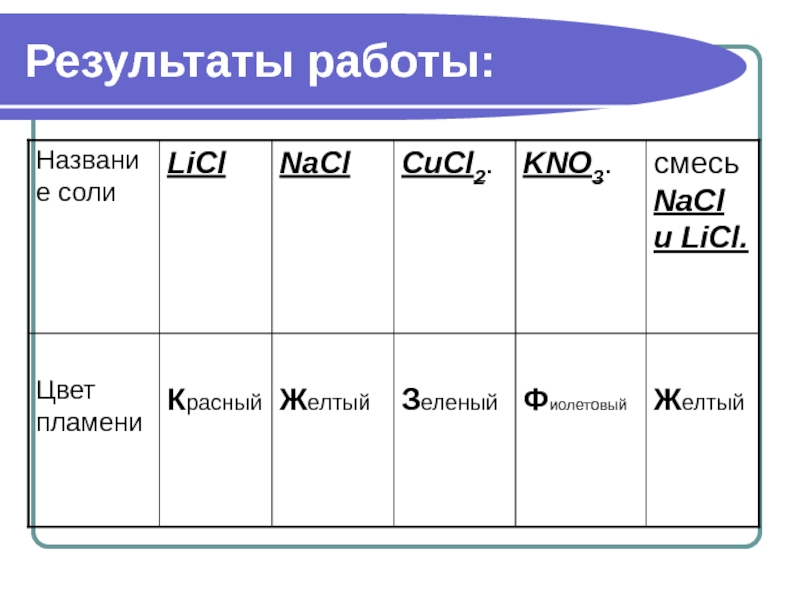
Наблюдение реакции окрашивания пламени некоторыми катионами.
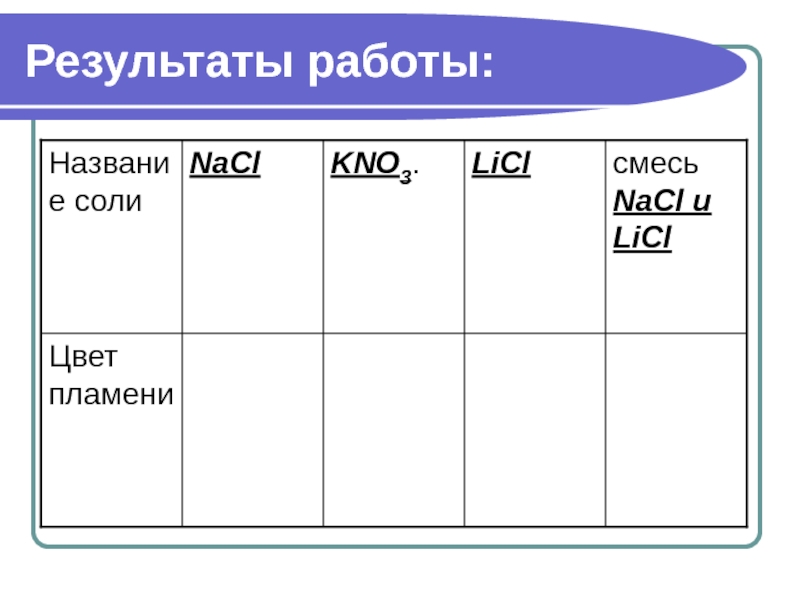
Слайд 16Исследовательская работа №2.3. Наблюдение реакции окрашивания пламени некоторыми катионами с использованием
Цель: наблюдение реакции окрашивания пламени при помещении в него некоторых солей через светофильтры и выдвижение гипотезы о применимости данного метода с целью отличия одних химических элементов от других.
Слайд 19Исследовательская работа №2.4. Наблюдение спектральных линий пламени солей
Цель: наблюдение спектра пламени
Оборудование (экспериментальная установка): спиртовка; спички; спектроскоп; плоскопараллельная пластинка; плоская щель; набор солей, содержащих соли лития и стронция, узкая щель; набор цветных карандашей; шаблоны для построения цветовых спектров.
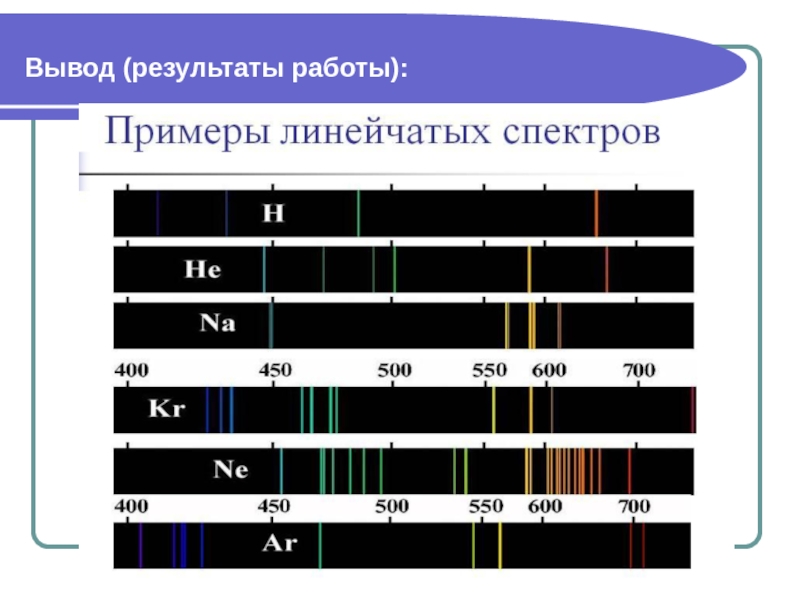
Слайд 20Вывод (результаты работы):
Атомы каждого химического элемента имеют спектр:
линейчатый;
спектр каждого
Слайд 21Исследовательская работа № 2.5. Наблюдение спектров различных газов.
Цель: провести наблюдения спектров
Оборудование (экспериментальная установка): спектроскоп двухтрубный, плоскопараллельная пластина, самодельный спектроскоп набор спектральных трубок, выпрямитель, прибор для зажигания спектральных трубок, соединительные провода, штатив, набор цветных карандашей, таблицы со спектрами излучения газов, находящихся в спектральных трубках, шаблоны для построения цветовых спектров.
Слайд 23Вывод (результаты работы):
Вывод (результаты работы): Атомы каждого из трех перечисленных химических
А) линейчатый/ полосатый/сплошной;
Б) спектр каждого газа имеет свой неповторимый линейчатый спектр/ спектры газов не имеют отличий;
В) в наблюдаемой последовательности, к основным цветам спектра водорода относят – красный, оранжевый, желтый, зеленый, голубой, синий, фиолетовый;
Г) в наблюдаемой последовательности, к основным цветам спектра гелия относят – красный, оранжевый, желтый, зеленый, голубой, синий, фиолетовый;
Д) в наблюдаемой последовательности, к основным цветам спектра неона относят – красный, оранжевый, желтый, зеленый, голубой, синий, фиолетовый;
Е) наблюдаемые спектры с примерно совпадают с эталонными/ наблюдаемые спектры абсолютно не совпадают с эталонными.
Слайд 24Этап 3. Закрепление знаний.
Задание 3.1. На рисунке изображены линейчатые спектры излучения
Слайд 25Этап 3. Закрепление знаний.
Задание 3.2. В составе какого химического соединения
Слайд 27Этап 3. Закрепление знаний.
Задание 3.3.
Рассмотрите таблицу спектров излучения различных химических
Слайд 29Ответ:
Линейчатые спектры излучения различных химических элементов отличаются:
а)количеством линий;
б)
в)цветом линий.
Сходство спектров химических элементов заключается в том, что они линейчаты.
Слайд 30Этап 4. Оценочно-аналитический
4.1. Сформулируйте общий вывод занятия, заполнив пропуски в предложении.
Вывод:
Слайд 31Этап 4. Оценочно-аналитический.
4.2. Перескажите русскую пословицу при
помощи физических
терминов.
Каков пан, таков на
нем и жупан.
Слайд 324.3. Игра «Правда или ложь».
Мы выбрали несколько фактов о спектроскопии. Некоторые из них
Слайд 33Игра «Правда или ложь».
С помощью спектрального анализа можно получить следующие характеристики:
Химический состав изучаемого
Температуру вещества;
Наличие магнитного поля и его напряженность;
Скорость движения объекта.
Слайд 344.3. Игра «Правда или ложь».
Основные преимущества спектроскопии перед другими методами анализа являются:
Высокая чувствительность
Малое количество анализируемого образца (до сотых долей грамма вещества);
Многокомпонентность – возможное определение 20 и более компонентов;
Документальность (фотографии спектров могут храниться длительное время);
Экспрессивность (затраты времени гораздо меньше, чем при других методах).
Слайд 35Спасибо за внимание!
Сколько элементов в таблице Менделеева?
Правильных ответа может быть два:
(8 элементов
являются лишь
гипотетическим
вариантами).